一种基于超声驱动压电材料的无线神经调控系统及方法
文献发布时间:2023-06-19 19:14:59
技术领域
本发明属于神经调控技术领域,具体涉及一种基于超声驱动压电材料的无线神经调控系统及方法。
背景技术
神经调控是利用电、磁、光、超声等物理性或腺相关病毒、化合物等化学性手段改变神经系统信号传递,调节神经元及其所在神经网络活性,最终引起特定脑功能改变的生物医学工程技术。借助不同的刺激手段,神经调控不但可以引发神经系统快速的、局部的功能改变,也可以诱导持续的、全面的神经网络和神经环路连接改变,促进神经元可塑性以及神经环路重塑。因此,神经调控技术既是解析脑功能的重要工具,又是治疗神经系统疾病的有效手段。
目前,神经调控技术广泛应用在功能假体、临床治疗和基础研究等方面。根据调控设备对机体的侵入程度,神经调控技术可分为侵入性和非侵入性两类。
常用的侵入性神经调控技术主要包括深部脑刺激(DBS)、脊髓电刺激(SCS)和侵入式迷走神经电刺激(iVNS)、骶神经电刺激(SNS);非侵入性技术主要包括经颅磁刺激(TMS)、经颅直流/交流电刺激(tDCS/tACS)、经皮迷走神经刺激(tVNS)、经皮神经电刺激(TENS)以及经颅超声波刺激(TUS)和光刺激等。整体来看,侵入性技术主要借助电刺激手段,均属于依靠电能的有源医疗器械,通常由微电极、导线和脉冲发射器(即电池)三部分组成;以DBS为例,通常治疗帕金森症状,需要手术暴露相应的功能脑区或神经丛以植入电极,而电极释放的微电流刺激依赖于同时植入的电池和导线;其电池使用寿命有限,平均5-9年即需手术更换;以上因素使得侵入性技术的手术过程复杂、创伤面积大,术后感染率高和并发症多,治疗成本高昂、适用群体有限。
虽然非侵入性技术使用的刺激手段更加多样且具有无创优势,但该技术的空间分辨率普遍较低(厘米级),且部分刺激设备庞大无法便携;以电、磁刺激为例,经过皮肤或颅骨传导,刺激能量存在极大损耗、难以刺激大脑皮层下组织,实际作用范围无法精确判别、治疗效果不稳定;即便是新近发展的经颅聚焦超声调控技术,更有更强的组织穿透性和更高空间分辨率(约数毫米),但其刺激位点准确性、刺激参数和治疗效果、作用机制和安全性仍有待研究。
综上所述,目前电刺激手段是主流的神经调控刺激手段,植入式神经电刺激器存在结构复杂、缺少可靠能量供给的技术问题,非植入式神经刺激存在调控位置不精确、效果不稳定,且依赖大型有线设备无法便携使用等技术问题。
发明内容
为了解决上述所存在的技术问题,提高一种具有自供电、损伤小且可以实现多靶点刺激的便携设备,为此,本发明提供了一种基于超声驱动压电材料的无线神经调控系统及方法。
所述具体方案如下:
一方面,本发明提供了一种基于超声驱动压电材料的无线神经调控系统,所述系统包括:
超声模块,用于产生可调节参数的超声波信号,并引导超声波信号的刺激方向和位置;
压电刺激模块,其为微型的生物相容性压电材料,用于植入待测对象的中枢或外周神经区域,所述超声模块设置于待测对象体外,其产生的超声波刺激通过所述换能器直接作用到所述压电刺激模块上;所述压电刺激模块与所述超声模块之间建立有超声波刺激参数与诱发压电材料放电响应间的映射关系。
优选地,所述超声模块所产生的超声波刺激方向与所述压电模块保持垂直设置。
优选地,所述超声模块包括超声发生器、示波器、功率放大器和换能器,所述超声发生器用于产生可调参的超声波信号,所述示波器与所述超声发生器连接,用于显示超声波波形,所述功率放大器与所述超声发生器连接,用于对所述超声发生器产生的超声波信号进行放大,所述换能器与所述功率放大器连接,用于引导超声波的刺激方向和位置。
进一步优选地,所述超声发生器所产生的超声波刺激频率<0.65MHz,声强<500mW/cm
所述压电刺激模块包括一块或多块微型的生物相容性压电材料,其大小与待植入的一个或多个目标神经刺激区域大小相适配,所述超声模块所产生的超声波刺激作用于一个或同时作用于多个植入目标神经刺激区域中的所述压电材料上。
进一步地,所述系统中还包括数据采集模块和处理模块,所述数据采集模块为电生理信号采集装置,用于提取调控后所述压电刺激模块所诱发的神经电生理信号,所述处理模块中内嵌有信号分析算法,用于自动进行电刺激特征的监控和神经特征的提取。
另一方面,本发明还提供了一种基于超声驱动压电材料的无线神经调控方法,所述方法包括:
步骤1,利用超声波改变压电材料产生电信号的属性,建立超声模块与压电刺激模块之间超声波刺激参数与诱发压电材料放电响应间的映射关系;
步骤2,通过微创手术将压电刺激模块植入目标神经刺激区域,在目标神经刺激区域的外部通过调节超声模块的超声波刺激参数对目标神经刺激区域的神经系统进行调控;
步骤3,根据调控目的及步骤1中所建立的映射关系,通过改变超声模块的超声信号特征对压电刺激模块的放电响应做出调节。
所述方法还包括:
步骤4,同步采集目标神经刺激区域所产生的电生理信号和机体行为数据,并自动进行电刺激特征的监控和神经特征的提取。
对生物相容性压电材料进行超声响应的测试后,所述步骤1中建立超声参数、超声模块与压电材料之间距离和角度对超声波刺激诱发压电材料的放电响应间的映射关系。
所述步骤2中,将压电刺激模块植入一个或多个目标神经刺激区域,通过超声模块对一个压电刺激模块或同步对多个压电刺激模块执行超声波刺激后产生放电响应。
所述的超声波刺激参数与诱发压电材料放电响应间的映射关系符合如下公式:V=I×d
其中V—压电材料的输出电压,
I—超声波声强,
d
t—压电材料厚度,
A—压电材料截面积,
并在此基础上考虑距离和频率等因素的干扰。
本发明技术方案具有如下优点:
A.本发明利用体外的超声模块对植入体内神经刺激区域的压电材料施加超声波刺激,超声波具有良好的组织穿透力和聚焦性,利用超声波这种非接触的能量源和压电材料的压电效应相结合,采用植入神经刺激区域的微型化、生物相容性压电材料,能够良好解决植入刺激压电材料的供电问题、精准调控神经刺激区域和设备便携化问题。
B.本发明在微创前提下,在体外利用超声波驱动植入体内的压电材料放电,将超声模块所产生的机械能转化成压电材料的电能,使压电材料具有自供电的特点,从而对神经刺激区域产生可控的神经电刺激信号;本发明以无线通讯方式实现对中枢和外周神经系统精准调控的方法,与传统神经调控方式相比,本发明具有空间分辨率高,不仅可以对单个靶点进行精准刺激调控,还可以实现多靶点(如多个脑区)的同步刺激,实现对神经系统精准且高效的刺激调控,并进一步摆脱有线调控手段的局限性,因此适用群体更为广泛,且简单易行。
C.本发明既可以实现中枢神经系统的调控(如大脑皮层、深部脑区和脊髓背角等),也可以实现外周神经系统的调控(如神经节、神经丛、肌肉等),具有损伤小、设备便携等优点。
附图说明
为了更清楚地说明本发明具体实施方式,下面将对具体实施方式中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
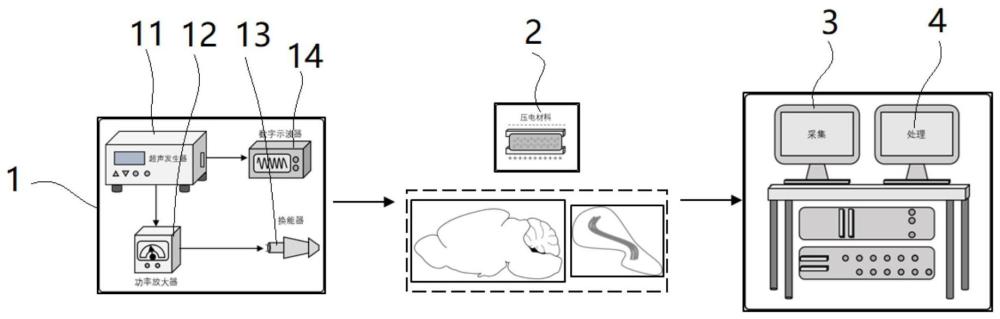
图1为本发明所提供的无线神经调控系统整体图示;
图2为本发明所提供的调控方法流程图;
图3为本发明以调控大鼠M1区域缓解疼痛为例所提供的调控方法流程图;
图4为实施例中提供的超声驱动海藻酸钙水凝胶的原始电压值信号;
图5为实施例中超声驱动海藻酸钙水凝胶的压电效应(差异包络电压值)
图6为实施例中指标一差异包络电压值受到超声刺激参数的调节图示;
图7为实施例中超声驱动海藻酸钙水凝胶的压电效应(差异频谱功率值)。
图中标识如下:
1-超声模块;11-超声发生器,12-功率放大器,13-换能器,14-示波器;2-压电刺激模块;3-数据采集模块;4-处理模块。
具体实施方式
下面将结合附图对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
如图1所示,本发明提供了一种基于超声驱动压电材料的无线神经调控系统,包括超声模块和压电刺激模块,其中超声模块用于产生可调节参数的超声波信号,并引导超声波信号的刺激方向和位置;压电刺激模块为微型的生物相容性压电材料,用于植入待测对象的中枢或外周神经区域,超声模块设置于待测对象体外,其产生的超声波刺激方向朝向压电刺激模块,并直接作用到压电刺激模块上,使其产生放电响应,压电刺激模块与超声模块之间建立有超声波刺激参数与诱发压电材料放电响应间的映射关系,根据对神经刺激区域的调控目的,经调节超声模块的超声波刺激参数,可以实现对压电材料不同放电电压的输出。本发明所采用的超声模块所产生的超声波刺激方向优选与压电模块保持垂直作用设置。
如图1所示,其中的超声模块包括超声发生器、示波器、功率放大器和换能器,超声发生器用于产生可调参的超声波信号,示波器用于显示超声波发生器所产生的超声波波形,功率放大器用于对超声发生器产生的超声波信号进行放大,换能器与功率放大器连接,用于引导超声波的刺激方向和位置,即其超声作用方向。这里所采用的超声发生器、示波器、功率放大器和换能器均为现有技术,具体产品型号可以从市场上购得,不再赘述。
为避免对机体组织造成损伤,控制超声模块所产生的所有超声波刺激均属于低频和低强度超声波刺激,即频率<0.65MHz,声强<500mW/cm
本发明不仅实现对单个靶点的精准调控,还可以实现同一超声模块对多靶点的同步超声刺激,即,本发明中的压电刺激模块包括一块或多块微型的生物相容性压电材料,其大小与待植入的一个或多个目标神经刺激区域大小相适配,通过换能器作用到一个或多个目标神经刺激区域,使该压电材料在超声波作用下产生放电响应,并产生强度、时长等可控的稳定电流,即实现了机械能到电能的转换,对中枢神经系统进行调控,比如大脑皮层、深部脑区和脊髓背角等,也可以实现外周神经系统的调控,比如神经节、神经丛、肌肉等,当然不限于上述举例所给出的神经部位进行超声波刺激。
超声模块对压电材料进行超声波作用时,为了方便检测神经调控效果,本发明还在系统中设置了数据采集模块和处理模块,数据采集模块为电生理信号采集装置,用于提取调控后压电刺激模块所诱发的神经电生理信号,此装置为现有技术。其中在处理模块中内嵌有信号分析算法,用于自动进行电刺激特征的监控和神经特征的提取。
其中,超声模块可集成为小体积一体式设备,更便于携带,结合数据采集模块与处理模块在实验室测试中使用。
如图2所示,本发明还提供了一种基于超声驱动压电材料的无线神经调控方法,包括如下步骤:
【S1】利用超声波改变压电材料产生电信号的属性,建立超声模块与压电刺激模块之间超声波刺激参数与诱发压电材料放电响应间的映射关系;
超声波刺激参数与诱发压电材料放电响应间的映射关系符合如下公式:V=I×d
其中V—压电材料的输出电压,
I—超声波声强,
d
t—压电材料厚度,
A—压电材料截面积,
同时,在上述公式的基础上还可以考虑超声距离、角度和频率等因素的干扰。
首先对现有生物相容性压电材料进行超声响应的测试,明确超声波发射与超声波接收位置之间的距离和角度,以及超声波本身参数(如刺激类型、刺激频率、刺激强度、刺激时长等)对超声波刺激诱发压电材料放电特征的影响;然后,建立二者之间的映射关系,以确保植入式压电材料在超声波的间歇刺激和持续刺激下会产生安全可控的神经电刺激信号。
【S2】通过微创手术将压电刺激模块植入目标神经刺激区域,在目标神经刺激区域的外部通过调节超声模块的超声波刺激参数对目标神经刺激区域的神经系统进行电刺激调控;以模式动物为例,利用手术将【S1】中性能明确的压电材料埋置到大鼠运动皮层M1区,脑部电信号记录电极植入同侧M1记录;或手术将压电材料埋置到大鼠后肢坐骨神经,将针状肌电记录电极埋置于附近肌肉。通过操控超声模块执行对压电材料的超声波刺激,实现对大鼠电极植入区域的神经刺激调控。再以镇痛应用为例,在对大鼠施加伤害性刺激(如热痛)诱发痛行为后,通过超声诱导埋置于疼痛感觉相关区域(如M1)或疼痛情绪相关区域(如前扣带回,ACC)的压电材料放电,实现对疼痛相关情绪的调控,从而减少大鼠的痛行为。
【S3】根据调控目的及步骤【S1】中所建立的映射关系,通过改变超声模块的超声信号特征(超声波参数)对压电刺激模块的放电响应做出调节。
具体而言,使用示波器显示超声波形,并利用功率放大器将超声波信号进行放大,再借由换能器引导超声波的刺激方向和位置,最终通过改变超声波刺激实现对压电材料放电响应的调控。
当然,还可以包括步骤【S4】,记录超声驱动压电材料放电情况下,并量化机体行为表现的改善和刺激位置电生理信号的变化,以明确调控效果。
以模式动物为例,直接将超声波导向目标脑区的头皮上方或后肢坐骨神经外表皮上方,记录脑部和肌肉等部位接受电刺激后的电生理信号,同步进行行为反应(如肌肉抽动、抬脚等)的视频记录。利用现有数据分析方法,对采集到的行为数据与电生理信号进行分析与统计,以客观量化本发明的调控效果。
综上,本发明采用超声驱动压电材料的植入式神经电刺激可以实现压电材料的自供电,且电刺激幅值、波形可随超声波的强度和频率调节,提供了一种作用位置精准、作用靶点多样的新型无线神经调控的解决方案。
下面以调控大鼠M1区域缓解疼痛为例,结合附图3对本发明的方法进行清晰、完整的描述,具体步骤如下:
【S01】将异氟烷麻醉诱导的Sprague-Dawley大鼠放置在脑立体定位仪上,通过脑微创手术暴露颅骨和M1皮层,将压电刺激模块植入左侧M1上肢代表区(bregma:0.24mm,lateral:-2mm,depth:1mm),在压电材料前后两端(±0.2mm)植入材料放电记录电极,用以记录压电材料的放电特性;在临近区域植入神经活动记录电极(lateral:-1.8mm,depth:1mm)并将硬膜外参考电极和接地电极安放于植入位点前侧2mm和后侧2mm处,用以记录和对比神经调控前后,脑电生理指标的变化情况,最后将电极保护装置安装在大鼠头部。
待大鼠术后恢复24小时后,用热板测痛仪测量其热痛阈值,确定诱发痛行为的热痛刺激强度;将其放入电磁屏蔽的行为箱中,把记录电极通过信号转接器和导线连接到放大器,再通过导线连接到对应数据采集模块与分析模块的电脑。电生理信号的采样率优选为40000Hz。
【S02】将超声模块中的换能器(中心频率为0.5Mhz)垂直固定于行为箱的顶部,施加不同参数的超声波刺激各50次;
【S03】通过对应数据采集模块与处理模块的电脑记录压电材料放电时的电信号,查看压电材料的放电情况,明确压电材料的放电特征,确保符合超声模块的预设。
【S04】进行行为学和电生理实验,以考察本发明提出的神经调控方法的应用效果。将大鼠放置在热板测痛仪上,记录大鼠的缩爪潜伏期,评估调控引起的行为变化,比较无超声波刺激和超声波刺激调控后大鼠热痛缩爪潜伏期的差异。
通过数据采集模块与处理模块中的电脑记录无超声波刺激阶段和超声波刺激阶段的电生理信号,并保存数据以备离线分析,以评估调控引起的神经元活性变化。以常用数据分析方法为例,使用上述保存的电生理数据进行分析,包括无超声波刺激阶段和超声波刺激阶段LFP信号的频谱功率谱密度的比较,以及Spike信号的群体神经元放电率比较,具体数据分析与处理步骤可以包括但不局限于以下内容:
首先,进行后续数据分析,先对采集的原始数据进行预处理,包括数据拆分(LFP:低通滤波300Hz,Spike:高通滤波300Hz)、LFP降采样(1000Hz)、LFP数据滤波(LFP:48-52Hz凹陷滤波)和分段(2s)、Spike聚类和分类挑拣。
其次,对无超声波刺激阶段和超声波刺激阶段LFP信号的功率谱密度分析:使用修正周期图功率谱密度估计方法将预处理后的LFP时域信号转换到频域,检测超声波刺激阶段信号中压电材料的放电频率是否在测试确定的调控作用范围内;而后运用主成分分析将其提取减除;然后将频谱划分为6个频带:delta(1-4Hz)、theta(4-8Hz)、alpha(8-12Hz)、beta(12-30Hz)、低频gamma(30-50Hz)、高频gamma(50-100Hz),比较各个频带LFP信号在无超声波刺激和超声波刺激条件下的功率谱密度差异。此外,使用时频分析算法计算LFP信号的时频响应,比较在无超声波刺激和超声波刺激条件下时频响应的特征差异。
再次对无超声波刺激阶段和超声波刺激阶段Spike信号的群体神经元放电率分析:将提取到的神经元放电时间序列转换为连续的放电频率直方图,然后运用修正周期图功率谱密度估计方法将其转换到频域,运用频率逐点分析比较放电频率在无超声波刺激和超声波刺激条件下的差异;并使用时频分析算法计算时频响应,比较在无超声波刺激和超声波刺激条件下时频响应的特征差异。此外,计算群体神经元的平均放电率放电率,比较在无超声波刺激和超声波刺激条件下的神经元平均放电率差异。
本实验预期在超声波刺激驱动压电材料调控M1区域后,大鼠的疼痛敏感性显著降低,而无超声波刺激时大鼠的疼痛敏感性无显著变化。这种疼痛敏感性降低在行为学上表现为大鼠的热痛缩爪潜伏期显著延长,电生理上表现为该皮层区域多频段神经振荡的能量变化(主要是alpha和beta频带振荡能量增加,gamma频带振荡能量降低)。该结果可表明,通过超声驱动中枢神经系统植入的压电材料,能够精准调节特定脑区的神经元活动,同时诱发动物的行为改变,具有缓解疼痛的积极作用,是一种可靠的无线神经调控方法。
【S05】根据【S03】和【S04】中所得数据结果,考察基于超声驱动压电材料的无线神经调控技术对行为的效果,建立超声压电材料放电特性、神经调控效果和脑响应信号之间的关联,在考察该神经调控有效性的同时,优化调控参数。
实施例
(1)超声模块的配置
为了降低配置复杂性、提高实用性和保障安全性,测试中使用的超声装置是获得医疗器械许可的市售超声理疗仪器(品牌:当代;型号:UT1021);该仪器具有1MHz和3MHz两个超声频率,输出强度和占空比均可多档位调节,输出模式有脉冲和连续两种,治疗探头的有效辐射面积为5.0cm
测试中使用的超声刺激参数如下:
1.超声频率:1MHz和3MHz;
2.超声波占空比:50%和100%,即产生脉冲波和连续波;
3.输出声强和功率均设置为最大输出值:50%占空比对应的最大输出声强为3W/cm
(2)压电刺激模块的材料选择
海藻酸钠(sodium alginate,SA)是从褐藻类的海带或马尾藻中提取碘和甘露醇之后的副产物,是一种天然多糖,具有药物制剂辅料所需的稳定性、溶解性、粘性和安全性,在食品工业和医药领域得到了广泛应用。氯化钙(calcium chloride)是一种由氯元素和钙元素组成的化学物质,化学式为CaCl
海藻酸钠高分子和氯化钙溶液化学交联形成的水凝胶(海藻酸钙水凝胶)为柔软有弹性的三维结构,凝胶的机械强度和力学性能稳定,具有生物相容性和安全性,且材料测试发现该凝胶具有一定的压电性能。因此,当前测试选择海藻酸钙水凝胶作为压电刺激模块,可在将来作为植入材料使用。
(3)超声驱动海藻酸钙水凝胶的压电效应测试
使用离子浓度为1%的海藻酸钙溶液与0.5mol/L的氯化钙溶液,按照3:1的比例制备海藻酸钙水凝胶;使用直径为35mm、厚度为0.18mm的铜片作为载物和导电平台,铜片两侧边缘焊接有两根27mm长的导线,将两根导线分别连接到示波器探头的正负极进行测试和电压信号记录;示波器的品牌为普源(Rigol),型号为DS1000Z-E。
测试中,超声仪器的治疗探头与铜片始终保持1cm的垂直距离,测试条件包括如下五个:水凝胶_基线条件(超声设备打开,但未激发超声)、水凝胶_50%占空比_1MHz、水凝胶_50%占空比_3MHz、水凝胶_100%占空比_1MHz、水凝胶_100%占空比_3MHz。
测试中使用两个指标对超声驱动海藻酸钙水凝胶的压电效应进行衡量。
指标一是差异包络电压值:通过提取各个条件原始电压值信号的上下包络电压值,分别求绝对值后相加得到总包络电压值;而后,将四个刺激条件的总包络电压值与基线条件的总包络电压值相减,得出差异包络电压值(mV)。
指标二是差异频谱功率值:通过maltab中的pwelch函数计算各个条件的频谱功率值,而后,将四个刺激条件的频谱功率值与基线条件的频谱功率值相减,得出差异频谱功率值(dB)。
(4)测试结果如下
1.示波器记录了五种测试条件的原始电压值信号,所有条件的原始电压值在-300mv~300mV范围内,见图4所示。
2.指标一的相关结果表明,相较于基线条件(水凝胶_基线条件),四种参数的超声刺激(50%占空比_1MHz/50%占空比_3MHz/100%占空比_1MHz/100%占空比_3MHz)均能够驱动海藻酸钙水凝胶产生压电效应,其测得的差异包络电压值在0~600mV范围内,见图5所示。
此外,结果显示这种压电效应受到超声刺激参数的调节,即随着超声占空比和频率的增加,产生的差异包络电压值越高(50%占空比_1MHz:209.7mV;50%占空比_3MHz:273.7mV;100%占空比_1MHz:495.5mV;100%占空比_3MHz:532.2mV);相对于50%占空比的脉冲波,100%占空比的连续波能够诱发更高的压电效应,约为50%占空比的两倍电压值,两者的最大值均值差异达到272.15mV([495.5+532.2)/2-(209.7+273.7)/2]),见图6所示。
3.指标二的相关结果表明,相较于基线条件(水凝胶_基线条件),四种参数的超声刺激(50%占空比_1MHz/50%占空比_3MHz/100%占空比_1MHz/100%占空比_3MHz)驱动海藻酸钙水凝胶产生压电效应也体现在频谱特征上;在与超声刺激频率相近的频率附近,超声波引起了水凝胶材料的同频共振。类似地,差异频谱功率值也受到超声刺激参数的调节,即随着超声占空比和频率的增加,产生的差异频谱功率值越高(50%占空比_1MHz:2.436*10
显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明的保护范围之中。
- 一种基于压电晶体自供电的抽油机井下信号测量与无线传输系统
- 基于低强度聚焦超声的便携式神经调控装置和调控方法
- 一种基于超声神经刺激的无创血压调控系统
