一种抗体Fab片段的二聚体、其制备方法及应用
文献发布时间:2024-04-18 20:01:30
技术领域
本发明涉及生物技术领域,具体地,本发明涉及一种抗体Fab片段的二聚体、其制备方法及应用。
背景技术
抗体由B细胞接受抗原刺激后增殖分化生成的浆细胞产生,具有与抗原特异性结合的功能。抗体结构由决定抗原结合能力的Fab区和诱导抗体依赖性细胞毒作用(ADCC)、补体依赖性细胞毒作用(CDC)的Fc区组成,但Fc片段容易引起非特异性的结合,对于临床诊断和治疗存在不利的影响。相比于完整抗体,无Fc片段的小分子抗体药物具有以下优势:特异性强;分子量较小,更容易进入肿瘤组织内部;可在大肠杆菌中表达,成本低,周期短;免疫原性弱等。常见的单价小分子抗体如抗原结合片段Fab、单链可变区片段scfv、可变区片段Fv、单域抗体等,但由于单价小分子抗体存在着分子量低,极易被清除,半衰期较短,且亲和力较低的缺点,在实际应用中有必要设计多价小分子抗体,如双链抗体(Diabody)、三链抗体(Triabody)等。多价抗体可以结合多个抗原表位,相比于单价抗体,有更高的亲和力和较慢的解离速度,并且有些抗体的多价结合还可引起受体交联,激发细胞内信号转导,激活细胞或者诱导细胞凋亡等生物学效应。多价抗体的形成可通过交联方式连接,如Fab段可通过基因工程Linker连接成二聚体、三聚体等,也可通过自聚化结构域而形成,最终增加抗体分子大小,提高抗体药物在体内的半衰期。随着小分子抗体药物深入研究,其在临床应用中愈加广泛,如连接毒素药物可用于肿瘤的治疗,另外在抗感染治疗、器官移植、变态反应性疾病等方面,小分子抗体药物也显示了较好的应用前景,因此将单价小分子抗体改建为多价抗体已成为抗体药物研发的趋势。
现有技术中对抗体Fab片段的改构策略为引入(CPP)
发明内容
解决的技术问题:
本发明的一个方面,是针对现有技术中抗体Fab片段二聚化方法的二聚体产率低,对靶细胞的亲和力弱的缺点,提供了一种抗体Fab片段的二聚体、其制备方法及应用。
具体地,本公开中的技术方案通过在抗体Fab段的C
本发明提供的技术方案:
一种抗体Fab片段的二聚体,所述抗体Fab片段包括V
其中,所述n=1、2、3、4或5。
作为优选,在本公开的某些实施方式中,上述n=1、2或3。更优选地,在本公开的一个实施方式中,上述n=3。在本公开中,所述氨基酸序列(CP)
在本公开的某些实施方式中,所述二聚体可以为同源二聚体,也可以为异源二聚体。所述同源二聚体或异源二聚体可以在单体Fab片段形成后,自发地或人工地组装成二聚体。可以利用现有技术中合适的方法实现上述组装,示例性的例子如,将包含不同单体Fab片段基因序列的载体在同一表达系统中进行表达,所获得的表达产物中包含有由不同单体Fab片段组装形成的异源二聚体。
在本公开中,由所述单体Fab片段形成的二聚体之间可以通过任意合适的共价键或非共价键连接。作为优选,在本公开的某些实施方式中,所述单体Fab片段之间通过二硫键连接。
在本发明的某些实施方式中,示例性的技术方案,例如:
一种抗CD19抗体Fab片段的二聚体,所述抗体Fab片段包括V
其中,所述n=1、2、3、4或5;优选地,所述n=3。
再例如:
一种抗CD20抗体Fab片段的二聚体,所述抗体Fab片段包括V
其中,所述n=1、2、3、4或5;优选地,所述n=3。
再例如:
一种抗BCMA抗体Fab片段的二聚体,所述抗体Fab片段包括V
其中,所述n=1、2、3、4或5;优选地,所述n=3。
在本公开中,通过上述技术方案能够实现抗体Fab片段的二聚化。为了更好地发挥Fab段二聚体的某些功效,在本公开的某些实施方式中,所述氨基酸序列(CP)
在本公开的某些实施方式中,所述效应分子可以为抗癌剂、抗炎剂、抗自身免疫性疾病剂、抗感染剂、毒素、放射治疗剂、核苷酸或细胞因子。作为优选,在本公开的一些实施方式中,所述效应分子为TNF家族成员或力达霉素中的辅基蛋白LDP。在本公开中,上述效应分子可以为蛋白质、核酸或小分子化合物,其与所述二聚体连接的手段可以为现有技术中合适的方法。所述效应分子示例性的例子如,TRAIL,肿瘤坏死因子相关的凋亡诱导配体TRAIL也称CD253或TNF10,是TNF超家族的成员。TRAIL是一种II型糖蛋白,由281个氨基酸组成,其中C端的241个氨基酸在胞外,胞外部分降解后形成有功能性的可溶性的TRAIL。TRAIL的第230位置为半胱氨酸,通过Zn
在本公开中,所述抗体Fab片段包括V
本发明的另一个方面,是提供了一种抗体Fab片段二聚化载体的构建方法,所述Fab片段包括设置于所述片段C末端的重链恒定区C
其中,所述n=1、2、3、4或5;
其中,所述间接地为经过编码至少一个连接体的核苷酸序列设置所述编码(CP)
本发明的另一个方面,是提供了一种抗体Fab片段二聚化的方法,包括:
步骤a)利用上述构建方法获得包含编码所述抗体Fab片段的核苷酸序列的载体;
步骤b)将步骤a)获得的载体在表达系统中表达并纯化。
本发明的另一个方面,是提供了上述二聚体在制备治疗肿瘤、炎症、自身免疫性疾病或感染的药物中的用途。
本发明的另一个方面,是提供了二聚体在制备抗体药物缀合物中的用途。
本发明的有益效果:
本发明提供的新型抗体二聚化改构方式,通过在抗体Fab段的C
附图说明
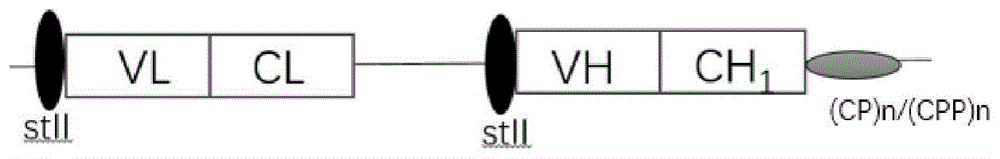
图1A~图1E为质粒构建示意图;其中,VL、VH分别为抗体轻、重链可变区,CL为人轻链恒定区CL部分,CH
图2A~图2F为改构二聚化蛋白的鉴定结果图;图2A和图2B为使用考马斯亮蓝法比较6种改构蛋白二聚体比例,其中,图2A为非还原条件,图2B为还原条件;泳道从左到右:Marker;CON;Anti-CD19Fab-LDP(对照);1号Anti-CD19Fab-(CPP)
图3A~图3D为Anti-CD19Fab-(CPP)
图4A~图4D为Anti-CD19Fab-(CPP)
图5A和图5B为Anti-CD20Fab-(CPP)
图6A~图6D为Anti-CD20Fab-(CPP)
图7A~图7D为Anti-CD20Fab-(CPP)
图8A和图8B为Anti-BCMA Fab-(CPP)
图9A~图9D为Anti-BCMA Fab-(CPP)
图10A~图10D为Anti-BCMA Fab-(CPP)
图11A和图11B为Anti-CD19Fab-(CPP)
图12A~图12D为Anti-CD19Fab-(CPP)
图13A~图13D为Anti-CD19Fab-(CPP)
图14A和图14B为质粒构建示意图;VL、VH分别为抗体轻、重链可变区。CL为人轻链恒定区CL部分,CH1为人重链恒定区CH1部分;其中,图14A为真核表达载体Anti-CD19Fab-(CP)
图15为Anti-CD19Fab-(CP)
图16为流式细胞术检测Anti-CD19Fab-(CP)
图17为体外CCK8法检测Anti-CD19Fab-(CP)
图18为体外CCK8法检测Anti-CD19Fab-(CP)
具体实施方式
本发明公开了一种抗体Fab片段的二聚体、其制备方法及应用,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。需要特别指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明,并且相关人员明显能在不脱离本发明内容、精神和范围的基础上对本文所述内容进行改动或适当变更与组合,来实现和应用本发明技术。
在本发明中,除非另有说明,否则本文中使用的科学和技术名词具有本领域技术人员所通常理解的含义。除非另有其它明确表示,否则在整个说明书和权利要求书中,术语“包括”或其变换如“包含”或“包括有”等等将被理解为包括所陈述的元件或组成部分,而并未排除其它元件或其它组成部分。术语“一个(一种)”(“a”、“an”和“the”)包括复数指示物。术语“多个(多种)”是指两个(种)或更多个(种)。术语“如”、“例如”等旨在指示例性实施方案,而不意图限制本公开的范围。
定义:
术语“Fab”、“Fab片段”或“Fab部分”是指包含VH、CH1、VL和CL免疫球蛋白结构域的多肽。通常来说,Fab片段包含抗体的整个轻链。可采用Fab片段来限定免疫球蛋白分子的“一个臂”。它包含该Ig的表位结合部分。天然免疫球蛋白的Fab区可通过木瓜蛋白酶消化作为蛋白水解片段获得。
术语“二聚体”广义地是指包含两个单体亚基的肽。在本公开中,所述二聚体包括同源二聚体或异源二聚体。二聚体的单体亚基可以在其C端或N端连接,或者可以经由内部氨基酸残基连接。二聚体的每个单体亚基可以通过相同位点连接,或者每个单体亚基可以通过不同位点(例如,C端、N端或内部位点)连接。
术语“二硫键”是指两个硫原子之间形成的共价键,一般指多肽链中的两个半胱氨酸残基侧链的硫原子之间形成的共价键。对于维持许多蛋白质分子的天然构象和稳定性十分重要。
术语“效应分子”是指任何天然或合成制备的分子,包括可由化学合成的小分子量分子或化学实体,和需要通过宿主细胞发酵来制备且可对标靶或抗原结合特异性免疫配体赋予新功能的较大分子或生物实体,和核酸分子(例如mRNA分子)。
术语“配体”是指特异性结合受体并导致受体变化的分子,其可以使得受体的活性发生改变或在表达受体的细胞中发生反应。配体可以作为受体的激动剂或拮抗剂的分子或其复合物。配体可包括天然和合成的配体,也包括小分子,细胞因子和抗体的肽模拟物。配体和受体的复合物被称为“配体-受体复合物”。配体可以包括多蛋白或融合蛋白的一个结构域(例如,或抗体/配体融合蛋白的结构域)。
术语“受体”是指生物体内一类能与细胞外专一信号分子(配体)结合引起细胞反应的蛋白质。在本公开中,受体主要行使其与配体结合的作用。
术语“scFv”即单链抗体,包括由一个轻链可变结构域(VL)或其部分和一个重链可变结构域(VH)或其部分组成的结合分子,其中每个可变结构域(或其部分)源自相同或不同抗体。
术语“Fv”是指作为抗体的Fab(抗原结合片段)区域的一部分的最小抗体片段,由重链可变区(VH)和轻链可变区(VL)组成。
术语“dAb”是指特异性结合抗原的单一免疫球蛋白可变结构域(VH或VL)多肽。“dAb”独立地结合其它V结构域的抗原;然而,“dAb”可以与其它VH或VL结构域以同型-或异型多聚体存在,其中对于通过dAb结合抗原,不需要其它的结构域,即,其中dAb独立地结合其它VH或VL结构域的抗原。
术语“多价体”是指包括两个或多个生物活性片段的重组分子。形成多价体分子的蛋白质片段可通过肽连接物连接,该肽连接物与组成部分相连又不影响其独立行使功能。
术语“载体”包括任何遗传元件,例如质粒、噬菌体、转座子、粘粒、染色体、人工染色体、病毒、病毒粒子等,其在与适当的控制元件相关联时能够复制,并且其可以在细胞之间转移基因序列。因此,该术语包括克隆媒介和表达媒介,以及病毒载体。
术语“抗体药物缀合物”也可称为“免疫缀合物”或ADCs(antibody drugconjugates),是与一种或多种异源分子缀合的抗体或Fab等抗体衍生物构成的缀合物,异源分子包括但不限于细胞毒性剂。异源分子可以为蛋白质、核苷酸或小分子化合物。
抗体Fab片段的二聚体:
本公开的一个方面,是提供了一种抗体Fab片段的二聚体。其优越性是可以更有效地实现抗体Fab片段的二聚化。基于免疫治疗的策略,抗体的多聚化能够增加抗体分子大小,提高抗体药物在体内的半衰期。同时,与完整的IgG相比,Fab片段缺少Fc段,能与抗原选择性结合但不会发生沉淀反应;由于自身免疫原性低,不会被活体的免疫细胞识别,因此能显著降低超敏性反应发生的概率,提高产品的安全性。Fab类抗体片段具有分子质量小、组织分布特异性强、免疫原型低、可基因工程操作等特点,使Fab成为了医药研究领域的重要成员之一,Fab类药物在预防、诊断、治疗等领域有着广泛的应用。
现有技术中,抗体Fab片段的制备方法可以包括酶解法、利用表达系统制备以及Fab抗体文库制备方法。酶解法通常是在单抗的基础之上,通过木瓜蛋白酶或胃蛋白酶对人免疫球蛋白G进行降解,得到F(ab’)
本公开中提供的抗体Fab片段二聚化策略可以适用于针对不同疾病靶点的任意合适的抗体。上述疾病可以为,例如,肿瘤、自身免疫性疾病、炎性疾病、感染,等。上述靶点的例子,如,CD19、CD20、BCMA、CD56、CD17、CD123、CD52、CD22、HER2、EGFR、VEGFR1、VEGFR2、FLT3、CD38、FGFR3、CD7、PD-1、PD-L1、CTLA4、PTK7、Notch3、FGF2、TNF-α、IL-1、IL-2、IL-6、IL-7、IL-17A、IL-12、IL-23、IL-36、TSLP、TSLPR、GRP78、整合蛋白、黏连蛋白-4、SDC1、AGS-16、MUC1。在本公开的某些实施方式中,所述二聚体可以为单特异性的,也可以为双特异性的。
为了实现某些功能,在本公开的一些实施方式中,上述单体Fab片段还可以携带有某些标签/标记物,例如,荧光标记物、放射标记物、酶标记物。示例性的例子如,His标记,CBP标记,CYD标记,链球菌II标记,FLAG标记,HPC标记,以及GST和MBP蛋白融合标记。
本公开中提供的抗体Fab片段的二聚体的V
抗体Fab片段的二聚体缀合物:
本公开的一个方面,是提供了一种抗体Fab片段的二聚体的缀合物。基于本公开中抗体Fab片段的二聚化策略,所形成的二聚化抗体对靶细胞/靶蛋白的亲和力显著增强。因此,可以通过本公开中的抗体Fab片段的二聚体将效应分子递送到靶细胞/靶蛋白,实现效应分子对靶细胞/靶蛋白的更有效识别。
在本公开的某些实施方式中,上述缀合物中的效应分子可以直接连接在所述氨基酸序列(CP)
所述效应分子可以为任意合适的效应分子,例如,抗癌剂、抗炎剂、抗自身免疫性疾病剂、抗感染剂、毒素、放射治疗剂、核苷酸或细胞因子。
在本公开的某些实施方式中,上述效应分子可用于治疗实体瘤,如肺癌、黑色素瘤、肝癌、胃癌、前列腺癌或乳腺癌。本公开中使用的“实体瘤的治疗”或“治疗实体瘤”包括,抑制肿瘤或肿瘤细胞的生长、缩小肿瘤的体积、杀死肿瘤细胞,或防止肿瘤细胞扩散(转移)。在本公开的另一些实施方式中,上述效应分子可用于治疗血液瘤,如骨髓瘤、淋巴癌、白血病。
在本公开的某些实施方式中,上述效应分子可用于治疗自身免疫性疾病,例如,类风湿性关节炎、全身性红斑狼疮、全身性进行性硬化症及其变型、多发性肌炎和皮肌炎、恶性贫血、自身免疫性血小板减少症。
在本公开的某些实施方式中,上述效应分子可用于治疗炎性疾病,例如,类风湿性关节炎、骨关节炎、过敏性气道疾病(例如哮喘)、慢性阻塞性肺病(COPD)和炎性肠病(例如克罗恩病、溃疡性结肠炎)。
在本公开的某些实施方式中,上述效应分子可用于治疗感染性疾病,包括但不限于,感染性生物体所引起的任何疾病。感染性生物体可以包括病毒,(例如,单链RNA病毒,单链DNA病毒,人类免疫缺陷病毒(HIV),肝炎A、B和C病毒,单纯疱疹病毒(HSV),巨细胞病毒(CMV),EB病毒(EBV),人乳头状瘤病毒(HPV)),寄生虫(例如,原生动物病原体和后生动物病原体如疟原虫物种,利什曼原虫属物种,血吸虫物种,锥虫物种),细菌(例如,分枝杆菌,特别是结核分枝杆菌,沙门氏菌,链球菌,大肠杆菌,葡萄球菌),真菌(例如,念珠菌属,曲霉属物种),卡氏肺囊虫,以及朊病毒。溶血素、Vero细胞毒素、CNF1、CNF2或PMT。
在本公开的某些实施方式中,上述效应分子可以为毒素,包括蛋白质毒素、细菌毒素或植物毒素。例如,凋亡蛋白、志贺毒素、志贺样毒素、铜绿假单胞菌外毒素(PE)或PE的外毒素A、全长或截短的白喉毒素(DT)、霍乱毒素、α-帚曲菌素、石竹素或皂草素。
在本公开的某些实施方式中,上述效应分子可以为放射治疗剂。放射治疗剂是指不依靠药物本身的药理作用,而是通过射线电离辐射生物效应产生治疗作用的一类放射性药物。具有靶向治疗作用,全身影响小等优势。常用发射β射线的放射性核素标记,α射线和俄歇电子具有潜在的治疗优势。
在本公开的某些实施方式中,上述效应分子可以为核苷酸。例如,载体、基因、诱导细胞自杀的转基因、脱氧核糖核酸(DNA)、核糖核酸(RNA)、反义寡核苷酸(ASO,AON)、短干扰RNA(siRNA)、微小RNA(miRNA)、DNA适配体、RNA适配体、mRNA、微环DNA、肽核酸(PNA)、氨基磷酸酯吗啉代寡聚物(PMO)、锁核酸(LNA)、桥接核酸(BNA)、2’-脱氧-2’-氟阿拉伯糖核酸(FANA)、2’-O-甲氧基乙基-RNA(MOE)、2’-O,4’-氨基亚乙基桥接核酸、3’-氟己糖醇核酸(FHNA)、质粒、二醇核酸(GNA)和苏糖核酸(TNA)、或它们的衍生物。
在本公开的某些实施方式中,上述效应分子可以为细胞因子,例如,TNF家族成员,如,肿瘤坏死因子-α(TNF-α)、肿瘤坏死因子-β(TNF-β)、TNF-α相关凋亡诱导配体(TRAIL)、TNF-α相关激活诱导的细胞因子(TRANCE)、TNF-α相关凋亡弱诱导物(TWEAK)、CD40配体(CD40L)、LT-α、LT-β、OX40L、CD40L、FasL、CD27L、CD30L、4-1BBL、APRIL、LIGHT、TL1、TNFSF16、TNFSF17或AITR-L。
作为优选,在本公开的某些实施方式中,提供了一种抗体二聚偶联药物,即在Anti-CD19-Fab尾端通过(CP)
实施例:
为了使本领域的技术人员更好地理解本发明的技术方案,下面结合具体实施例对本发明作进一步的详细说明。
实施例1:构建Anti-CD19Fab-(CP)
本公开所用原核表达载体表达框示意图见图1A、图1B、图1C、图1D、图1E。基于本申请人原有Anti-CD19单克隆抗体可变区序列,轻重链可变区分别连接至人源抗体恒定区CL、CH
SEQ ID No.1:Anti-CD19Fab(VL+CL)
DIVLTQSPKFMSTSVGDRVSVTCKASQNVGTNVAWYQQKPGQSPKPLIYSAT
YRNSGVPDRFTGSGSGTDFTLTITNVQSKDLADYFCQQYNRYPYTSGGGTKV
EIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSG
NSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFN
RGEC
SEQ ID No.2:Anti-CD19Fab(VH+CH1)
QVQLQQSGAELVRPGSSVKISCKASGYAFSSYWMNWVKQRPGQGLEWIGQI
YPGDGDTNYNGKFKGQATLTADKSSSTAYMQLSGLTSEDSAVYFCARKTISSV
VDFYFDYWGQGTTLTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPE
PVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHK
PSNTKVDKKVEPKSCDKTHT
实施例2:Anti-CD19Fab-(CP)
取实施例1中构建的表达质粒PAYZ-Anti-CD19Fab-(CP)
实施例3:Anti-CD19Fab-(CP)
本实施例采用考马斯亮蓝染色法、分子排阻色谱法、液相色谱串联质谱法鉴定改构后抗体蛋白的组分及组分比例。
考马斯亮蓝染色法鉴定蛋白组分:
取实施例2纯化后的改构蛋白各10μg分别与上样缓冲液混合后于95-100℃金属浴中10min,其中还原性的样品中另加入了终浓度2%的巯基乙醇,经12%SDS-PAGE,考马斯亮蓝R250染色5min,脱色液脱色16h以上,显示出清晰的条带。结果见图2A和图2B。由图2A可见,六种改构蛋白中,4号Anti-CD19Fab-(CP)
取纯化后蛋白Anti-CD19Fab-(CP)
采用分子排阻色谱法检测Anti-CD19Fab-(CP)
具体方法为:取Anti-CD19Fab-(CP)
表1分子排阻色谱鉴定结果
采用液相色谱串联质谱法精确分离蛋白样品中各组分并打质谱,以获得各组分精确分子量及在总样品中的含量比例:
具体方法为:取Anti-CD19Fab-(CP)
设置超高效液相色谱条件为:色谱柱:ACQUITY UPLC Protein BEH C4Column(
表2液相色谱条件设置
表3液相色谱串联质谱法鉴定结果
/>
通过以上结果可得出结论,本实施例提供的在抗体Fab片段C
实施例4:流式细胞术比较Anti-CD19Fab-(CP)
1、Anti-CD19Fab-(CPP)
2、Anti-CD19Fab-(CP)
表5竞争管设计表
实施例1-4证明本发明提供的在抗体Fab片段C
实施例5:构建Anti-CD20Fab-(CP)
构建方法同实施例1。如图1B所示,基于本申请人原有Anti-CD20单克隆抗体可变区序列,轻重链可变区分别连接至人源抗体恒定区CL、CH
SEQ ID No.3:Anti-CD20Fab(VL+CL)
DIELTQSPAILSASPGEKVTMTCRANSSVSYMLWYQQKPGSSPKPWIYATSHLASGVPTRFSGSGSGTSYSLTISRVEAEDAATYYCQQWTSNPPTFGAGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID No.4:Anti-CD20Fab(VH+CH1)
QVKLQQSGAELVKPGASVKMSCKASGYTFISYNMHWVKQTPGQGLEWIGGIYPGNGDTSYNQKFKGKATLTADKSSSAAYMQLSSLTSEDSAVYYCARWNYGNFGGGTMDYWGQGITVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHT
实施例6:Anti-CD20Fab-(CP)
取实施例5中构建的表达质粒PAYZ-Anti-CD20Fab-(CPP)
实施例7:Anti-CD20Fab-(CPP)
考马斯亮蓝染色法鉴定蛋白组分。
取纯化后蛋白Anti-CD20Fab-(CPP)
实施例8:流式细胞术比较Anti-CD20Fab-(CP)
1、Anti-CD20Fab-(CPP)
2、Anti-CD20Fab-(CP)
实施例9:构建Anti-BCMAFab-(CP)
构建方法同实施例1:如图1B所示,基于本实验室原有Anti-BCMA单克隆抗体可变区序列,轻重链可变区分别连接至人源抗体恒定区CL、CH
SEQ ID No.5:Anti-BCMAFab(VL+CL)
DIVLTQSPASLTVSLGQRATISCRASKSVSTSGYSYMHWYQQKPRQPPKLLIYLASNLESGVPARFSGSGSGTDFTLNIHPVEEEDAATYYCQHSRDLPYTFGGGTKLEIKRAVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID No.6:Anti-BCMAFab(VH+CH1)
QVQLQQSGAEVVRPGTSVKVSCKASGYAFTNYLIEWVKQRPGQGPEWIGVITPGRGDTKYNAKFAGKATLTADKSSSTAYMQLSSLTFDDSAVYFCARGTTAWFPYWGQGTLVTVSAASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHT
实施例10:Anti-BCMA Fab-(CP)
取实施例9中构建的表达质粒PAYZ-Anti-BCMAFab-(CPP)
实施例11:Anti-BCMAFab-(CP)
考马斯亮蓝染色法鉴定蛋白组分。
取纯化后蛋白Anti-BCMA Fab-(CPP)
实施例12:流式细胞术比较Anti-BCMAFab-(CPP)
1、Anti-BCMAFab-(CPP)
2、Anti-BCMAFab-(CPP)
实施例1-12证明本发明提供的在抗体Fab片段C
抗体偶联药物是抗体药物研究的重要分支,其偶联药物的位置常设置在CH1尾端,为验证本发明在抗体偶联药物二聚化中的应用前景,实施例13-16构建了一种抗体偶联药物的蛋白部分,即在Anti-CD19Fab的CH1尾端已连接(CP)
实施例13:构建Anti-CD19Fab-(CP)
如图1A所示,基于构建的Anti-CD19Fab-(CP)
SEQ ID No.7:Anti-CD19Fab-(CPP)3-G4S-LDP(VL+CL)
DIVLTQSPKFMSTSVGDRVSVTCKASQNVGTNVAWYQQKPGQSPKPLIYSATYRNSGVPDRFTGSGSGTDFTLTITNVQSKDLADYFCQQYNRYPYTSGGGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID No.8:Anti-CD19Fab-(CPP)3-G4S-LDP(VH+CH1+cpcpcp+G4S+LDP)
QVQLQQSGAELVRPGSSVKISCKASGYAFSSYWMNWVKQRPGQGLEWIGQIYPGDGDTNYNGKFKGQATLTADKSSSTAYMQLSGLTSEDSAVYFCARKTISSVVDFYFDYWGQGTTLTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPCPCPGGGGSAPAFSVSPASGLSDGQSVSVSVSGAAAGETYYIAQCAPVGGQDACNPATATSFTTDASGAASFSFVVRKSYTGSTPEGTPVGSVDCATAACNLGAGNSGLDLGHVALTFG
实施例14:Anti-CD19Fab-(CP)
取实施例13中构建的表达质粒Anti-CD19Fab-(CPP)
实施例15:Anti-CD19Fab-(CP)
考马斯亮蓝染色法鉴定蛋白组分。
取纯化后蛋白Anti-CD19Fab-(CPP)
实施例16:流式细胞术比较Anti-CD19Fab-(CPP)
1、Anti-CD19Fab-(CPP)
2、Anti-CD19Fab-(CPP)
实施例17:构建真核表达质粒Anti-CD19Fab-(CP)
本实施例所用真核表达载体表达框示意图如图14A和图14B所示。基于本申请人原有的具有内化能力的Anti-CD19单克隆抗体可变区序列,轻重链可变区分别连接至人源抗体恒定区CL、CH
实施例18:Anti-CD19Fab-(CP)
取实施例17中构建的表达质粒Anti-CD19Fab-(CP)
转染前一天,取对数生长期293T细胞6x10
实施例19:Anti-CD19Fab-(CP)
本实施例采用Western Blot鉴定。
取纯化后蛋白Anti-CD19Fab-(CP)
Anti-CD19Fab-(CP)
实施例20:流式细胞术检测Anti-CD19Fab-(CP)
采用流式细胞术检测目的蛋白对hCD19高表达细胞系Raji的结合能力。取等量(1μg)Anti-CD19Fab-(CP)
实施例21:CCK8法检测Anti-CD19Fab-(CP)
1、对CD19阳性细胞株Raji的体外杀伤实验:
取对数生长期Raji细胞(CD19阳性、TRAIL耐受细胞系)8x10
结果如图17所示。首先未偶联TRAIL蛋白的Anti-CD19Fab-(CP)
表6五种蛋白浓度梯度设置
2、对CD19阴性细胞株Jurkat细胞的体外杀伤:
选择对Trail敏感且CD19表达阴性的Jurkat细胞检测Anti-CD19Fab-(CP)
表7浓度设置
综合本实施例的结果说明,与TRAIL对照品相比,TRAIL与Anti-CD19-Fab偶联后的抗体-TRAIL药物能有效介导针对CD19阳性细胞的杀伤,且显著提高了靶细胞对TRAIL蛋白的敏感性,并降低TRAIL蛋白对于CD19阴性细胞Jurkat的毒副作用。其中引入(CP)
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 一种体育训练用肌肉放松装置
- 一种体育训练用肌肉放松装置
