鉴定γ/δT细胞调节剂的方法
文献发布时间:2024-04-18 19:58:21
技术领域
当前公开涉及癌症的治疗。
优先权
本申请要求2020年11月19日提交的美国临时申请号63/116,058和2021年4月9日提交的63/173,063的权益和优先权,其内容通过引用整体并入本文。
以电子方式提交的文本文件的描述
以电子方式一并提交的下述文本文件的内容通过引用以其整体并入本文:序列表的计算机可读格式副本(文件名:SHK-037PC_116981-5037_ST25;创建日期:2021年11月11日;文件大小:77,920字节)。
发明背景
癌症是世界范围内的一个重大健康问题。尽管最近取得了进展,但目前还没有普遍成功的预防或治疗方法。目前的治疗通常基于化疗或手术和放疗的组合,但对于许多患者来说仍然不够。
当前癌症治疗的主要限制是为患者选择合适的活性剂。常见的是向患者提供次优化疗,导致治疗不成功,包括死亡、疾病进展、不必要的毒性和更高的医疗费用。此外,检查点抑制剂虽然很有前景,但对许多患者无效。
因此,仍然需要可用于评估癌症和相关疾病以及开发新治疗的方法。本公开满足了这些需求并进一步提供了其他相关优点。
发明内容
因此,本发明部分提供了用于选择癌症治疗的患者的方法和癌症治疗的方法,其基于例如某些γ/δT细胞的丰度(例如,通过特定γ/δT细胞受体(TCR)的表达和/或嗜乳脂蛋白家族蛋白的表达来判断)进行。
在一个方面,本公开涉及一种鉴定癌症治疗物(cancertherapy)的方法,所述方法包括:(a)获得生物样品,所述样品包含一种或多种γ/δT细胞;(b)评估样品中一种或多种γ/δT细胞受体(TCR)链的存在、不存在或水平;和(c)选择具有在γ/δTCR处发出信号的能力(havinganabilitytosignalatthe gamma/deltaTCR)的癌症治疗物,所述癌症治疗物包含一个或多个嗜乳脂蛋白或其片段。在多个实施方案中,所述评估包括测量选自Vγ2、Vγ3、Vγ4、Vγ5、Vγ8、Vγ9、Vγ11、Vδ1、Vδ2、Vδ3、Vδ4、Vδ5、Vδ6、Vδ7和Vδ8的一种或多种γ/δT细胞受体(TCR)链的存在、不存在或水平。
在一个方面,本发明涉及一种选择癌症治疗的患者的方法,所述方法包括:(a)获得生物样品,所述样品包含一种或多种γ或δT细胞;(b)评估样品中一种或多种γ/δT细胞受体(TCR)链的存在、不存在或水平;和(c)选择具有在γ/δTCR处发出信号的能力的癌症治疗物,所述癌症治疗物包含一个或多个嗜乳脂蛋白或其片段。在多个实施方案中,所述评估包括测量选自Vγ2、Vγ3、Vγ4、Vγ5、Vγ8、Vγ9、Vγ11、Vδ1、Vδ2、Vδ3、Vδ4、Vδ5、Vδ6、Vδ7和Vδ8的一种或多种γ/δT细胞受体(TCR)链的存在、不存在或水平。
在一个方面,本公开涉及一种制备用于治疗癌症患者的癌症的药剂的方法,包括:(a)获得用于治疗癌症的药剂,所述获得包括:(i)评估来自癌症患者的生物样品中一种或多种γ/δT细胞受体(TCR)链的存在、不存在或水平;和(ii)选择具有在所述一种或多种γ/δTCR处发出信号的能力的癌症治疗物,所述癌症治疗物包含一个或多个嗜乳脂蛋白或其片段;(b)配制所鉴定的药剂,用于施用于癌症患者。在多个实施方案中,所述评估包括测量选自Vγ2、Vγ3、Vγ4、Vγ5、Vγ8、Vγ9、Vγ11、Vδ1、Vδ2、Vδ3、Vδ4、Vδ5、Vδ6、Vδ7和Vδ8的一种或多种γ/δT细胞受体(TCR)链的存在、不存在或水平。
在一个方面,本公开涉及一种鉴定针对肿瘤的癌症治疗的方法,所方法包括:(a)获得生物样品,所述样品包含一种或多种γ/δT细胞;(b)评估样品中一种或多种嗜乳脂蛋白的存在、不存在或水平;和(c)选择具有在γ/δTCR处发出信号的能力的癌症治疗物,所述癌症治疗物包含一个或多个嗜乳脂蛋白或其片段。在多个实施方案中,所述评估包括测量选自BTN1A1、BTN2A1、BTN2A2、BTN2A3、BTN3A1、BTN3A2、BTN3A3、BTNL2、BTNL3、BTNL8、BTNL9、BTNL10和SKINTL的一种或多种嗜乳脂蛋白的存在、不存在或水平。在多个实施方案中,所述评估包括测量选自人BTN1A1、人BTN2A1、人BTN2A2、人BTN2A3、人BTN3A1、人BTN3A2、人BTN3A3、人BTNL2、人BTNL3、人BTNL8、人BTNL9、人BTNL10和人SKINTL的一种或多种嗜乳脂蛋白的存在、不存在或水平。
在一个方面,本发明涉及一种选择癌症治疗的患者的方法,所述方法包括:(a)获得生物样品,所述样品包含一种或多种γ/δT细胞;(b)评估样品中一种或多种嗜乳脂蛋白的存在、不存在或水平;和(c)选择具有在γ/δTCR处发出信号的能力的癌症治疗物,所述癌症治疗物包含一个或多个嗜乳脂蛋白或其片段。在多个实施方案中,所述评估包括测量选自BTN1A1、BTN2A1、BTN2A2、BTN2A3、BTN3A1、BTN3A2、BTN3A3、BTNL2、BTNL3、BTNL8、BTNL9、BTNL10和SKINTL的一种或多种嗜乳脂蛋白的存在、不存在或水平。在多个实施方案中,所述评估包括测量选自人BTN1A1、人BTN2A1、人BTN2A2、人BTN2A3、人BTN3A1、人BTN3A2、人BTN3A3、人BTNL2、人BTNL3、人BTNL8、人BTNL9、人BTNL10和人SKINTL的一种或多种嗜乳脂蛋白的存在、不存在或水平。
在一个方面,本公开涉及一种制备用于治疗癌症患者的癌症的药剂的方法,包括:(a)获得用于治疗癌症的药剂,所述获得包括:(i)评估来自癌症患者的生物样品中一种或多种嗜乳脂蛋白的存在、不存在或水平;和(ii)选择具有在γ/δTCR处发出信号的能力的癌症治疗物,所述癌症治疗物包含一个或多个嗜乳脂蛋白或其片段;(b)配制所鉴定的药剂,用于施用于癌症患者。在多个实施方案中,所述评估包括测量选自Vγ2、Vγ3、Vγ4、Vγ5、Vγ8、Vγ9、Vγ11、Vδ1、Vδ2、Vδ3、Vδ4、Vδ5、Vδ6、Vδ7和Vδ8的一种或多种γ/δT细胞受体(TCR)链的存在、不存在或水平。
在多个实施方案中,生物样品可以是组织样品。例如,组织样品可以选自新鲜组织样品、冷冻肿瘤组织标本、培养细胞、循环肿瘤细胞和福尔马林固定的石蜡包埋的肿瘤组织标本。在多个实施方案中,组织样品是活检样品。在多个实施方案中,活检样品选自内窥镜活检、骨髓活检、内窥镜活检(例如膀胱镜检查、支气管镜检查和结肠镜检查)、针吸活检(例如细针抽吸、空心针活检、真空辅助活检)、X射线辅助活检、计算机断层扫描(CT)辅助活检、磁共振成像(MRI)辅助活检和超声辅助活检)、皮肤活检(例如削切活检、穿刺活检和切取活检)和手术活检。在多个实施方案中,组织样品选自骨、骨髓、肺、脑、肝、肾上腺、结肠、肠、食道、胰腺、膀胱、乳房、淋巴结和皮肤。在多个实施方案中,生物样品包含体液。
在多个实施方案中,生物样品通过选自刮取、拭子和活检的技术获得。在多个实施方案中,生物样品通过使用刷子、(棉)拭子、抹刀、冲洗/洗涤液、穿刺活检装置、用针穿刺腔室或手术器械来获得。
在多个实施方案中,生物样品是肿瘤样品。在多个实施方案中,肿瘤是转移性的。在多个实施方案中,肿瘤已转移至组织或器官。在多个实施方案中,组织或器官选自骨、骨髓、肺、脑、肝、肾上腺、结肠、肠、食道、胰腺、膀胱、乳房、淋巴结和皮肤。
在多个实施方案中,所述评估通过DNA测序、RNA测序、免疫组织化学染色、蛋白质印迹、细胞内蛋白质印迹、免疫荧光染色、ELISA和荧光激活细胞分选(FACS)或其组合来进行。
在多个实施方案中,所述评估通过使样品与特异性结合选自Vγ2、Vγ3、Vγ4、Vγ5、Vγ8、Vγ9、Vγ11、Vδ1、Vδ2、Vδ3、Vδ4、Vδ5、Vδ6、Vδ7和Vδ8的一种或多种γ/δT细胞受体(TCR)链的药剂接触来进行。在多个实施方案中,特异性结合一种或多种TCR的药剂是抗体或其片段。在多个实施方案中,抗体是重组抗体、单克隆抗体、多克隆抗体或其片段。
在多个实施方案中,所述评估通过使样品与特异性结合一种或多种嗜乳脂蛋白的药剂接触来进行。在多个实施方案中,特异性结合一种或多种嗜乳脂蛋白的药剂是抗体或其片段。在多个实施方案中,抗体是重组抗体、单克隆抗体、多克隆抗体或其片段。在多个实施方案中,所述评估通过使样品与特异性结合选自人BTN1A1、人BTN2A1、人BTN2A2、人BTN2A3、人BTN3A1、人BTN3A2、人BTN3A3、人BTNL2、人BTNL3、人BTNL8、人BTNL9、人BTNL10和人SKINTL的一种或多种嗜乳脂蛋白的药剂接触来进行。
在多个实施方案中,通过使样品与特异性结合一种或多种所述核酸的药剂接触来测量一种或多种嗜乳脂蛋白的水平和/或活性。在多个实施方案中,特异性结合一种或多种所述核酸的药剂是核酸引物或探针。
在多个实施方案中,一种或多种TCR的水平和/或活性通过使样品与特异性结合一种或多种所述核酸的药剂接触来测量。在多个实施方案中,特异性结合一种或多种所述核酸的药剂是核酸引物或探针。
在多个实施方案中,当与周围健康组织相比在肿瘤中检测到TCRVγ9δ2的存在或更高水平时,选择包含人BTN2A1、BTN3A1、BTN2A2和/或BTN2A3嗜乳脂蛋白或其片段的癌症治疗物;和/或当与周围健康组织相比在肿瘤中检测到TCRVδ4的存在或更高水平时,选择包含人BTNL3嗜乳脂蛋白或其片段的癌症治疗物。
在多个实施方案中,当与周围健康组织相比在肿瘤中检测到嗜乳脂蛋白的存在或更高水平时,选择包含嗜乳脂蛋白或其片段的癌症治疗物。例如,当与周围健康组织相比在肿瘤中检测到人BTN1A1的存在或更高水平时,选择包含人BTN1A1嗜乳脂蛋白或其片段的癌症治疗物;当与周围健康组织相比在肿瘤中检测到人BTNL2的存在或更高水平时,选择包含人BTNL2嗜乳脂蛋白或其片段的癌症治疗物;当与周围健康组织相比在肿瘤中检测到人BTN2A1的存在或更高水平时,选择包含人BTN2A1嗜乳脂蛋白或其片段的癌症治疗物。
在多个实施方案中,癌症治疗物包含异二聚体蛋白,所述异二聚体蛋白包含:(a)第一结构域,其包含一个或多个嗜乳脂蛋白家族蛋白或其片段;(b)第二结构域,其包含靶向结构域,所述靶向结构域选自(i)抗体、抗体样分子或其抗原结合片段,和(ii)胞外结构域;和(c)接头,其连接第一结构域和第二结构域。在多个实施方案中,第一结构域包含两个相同的嗜乳脂蛋白家族蛋白。在多个实施方案中,第一结构域包含两个不同的嗜乳脂蛋白家族蛋白。在多个实施方案中,嗜乳脂蛋白家族蛋白或其片段包含Ig样V型结构域。在多个实施方案中,嗜乳脂蛋白家族蛋白或其片段衍生自天然全长蛋白。
在多个实施方案中,癌症治疗物包含异二聚体蛋白,所述异二聚体蛋白包含α链和β链,其中α链和β链各自独立地包含(a)第一结构域,其包含嗜乳脂蛋白家族蛋白或其片段;(b)第二结构域,其包含靶向结构域,所述靶向结构域选自(i)抗体、抗体样分子或其抗原结合片段,和(ii)胞外结构域;和(c)接头,其连接第一结构域和第二结构域。在多个实施方案中,第一结构域包含两个相同的嗜乳脂蛋白家族蛋白。在多个实施方案中,第一结构域包含两个不同的嗜乳脂蛋白家族蛋白。在多个实施方案中,嗜乳脂蛋白家族蛋白或其片段包含Ig样V型结构域。在多个实施方案中,嗜乳脂蛋白家族蛋白或其片段衍生自天然全长蛋白。在多个实施方案中,第一结构域包含具有以下氨基酸序列的多肽:(a)SEQ ID NO:24至45中的任一个或其片段;(b)SEQ ID NO:24至45中的任一个或其片段。在多个实施方案中,接头包含具有SEQ ID NO:1-14中一个或多个的氨基酸序列的多肽。在多个实施方案中,接头包含具有SEQ ID NO:15-22的氨基酸序列的多肽。
在多个实施方案中,靶向结构域是抗体或其抗原结合片段。在多个实施方案中,靶向结构域是抗体样分子或其抗原结合片段。在多个实施方案中,抗体样分子是scFv分子。在多个实施方案中,靶向结构域是胞外结构域。
在多个实施方案中,靶向结构域能够结合癌细胞表面上的抗原。在多个实施方案中,靶向结构域特异性结合CD19。在多个实施方案中,靶向结构域特异性结合PSMA。在多个实施方案中,靶向结构域特异性结合CD33。在多个实施方案中,靶向结构域特异性结合CD20。在多个实施方案中,靶向结构域特异性结合CLL-1。
在多个实施方案中,接头包含(a)与嗜乳脂蛋白家族蛋白连接的第一电荷极化核心结构域,任选在羧基末端连接,和(b)与嗜乳脂蛋白家族蛋白连接的第二电荷极化核心结构域,任选在羧基末端连接。在多个实施方案中,接头通过第一和第二电荷极化核心结构域上带正电荷的氨基酸残基和带负电荷的氨基酸残基之间的静电相互作用形成异二聚体。在多个实施方案中,第一和/或第二电荷极化核心结构域包含多肽接头,其任选地选自柔性氨基酸序列、IgG铰链区或抗体序列。
在多个实施方案中,第一和/或第二电荷极化核心结构域还包含在电荷极化核心结构域的氨基和/或羧基末端具有带正电荷和/或带负电荷的氨基酸残基的肽。
在多个实施方案中,第一结构域和/或异二聚体蛋白调节或能够调节γδ(gammadelta)T细胞。在多个实施方案中,γδT细胞选自表达Vγ4、Vγ9δ2或Vγ7δ4的细胞。在多个实施方案中,调节γδT细胞是激活γδT细胞。在多个实施方案中,异二聚体蛋白能够在γδT细胞和肿瘤细胞之间形成突触,和/或异二聚体蛋白能够同时激活γδT细胞并将其靶向肿瘤细胞。
附图简要说明
图1A至图1C显示了在来自癌症患者的匹配的外周血和解离的肿瘤组织中的γ和δ链配对。图1A显示了用于对前列腺癌患者进行单细胞测序以确定外周血单核细胞(PBMC,图1B)和解离的肿瘤组织(图1C)中的γ和δ链配对的方法的示意图。简言之,从前列腺腺癌患者获得PBMC和解离的肿瘤组织。通过流式细胞术将样品中的γδT细胞单细胞分选到96孔板中,然后对γδTCR进行抗体染色。制备RNA并使用iPAIRPCR技术(iRepertoire)对γ和δ链进行测序。使用iPair分析仪软件在单细胞水平上鉴定γ和δ链的序列和配对。图1B的图显示了患者PBMC中的γ和δ链配对。图1C的图显示了患者的解离肿瘤样品中的γ和δ链配对。
图2显示了用于对癌症患者进行单细胞测序以确定肿瘤组织和肿瘤浸润淋巴细胞(TIL)中的γ和δ链配对的方法的示意图。简言之,将新鲜切除的肿瘤组织(图中显示的是结直肠癌)机械解离,以产生肿瘤和肿瘤浸润淋巴细胞(TIL)的单细胞悬浮液。将样品中的γδT细胞用泛γδTCR抗体染色,并通过流式细胞术将其单细胞分选到96孔板中。从细胞中提取RNA,并使用iPAIR PCR技术(iRepertoire)扩增TCRγ链和TCRδ链并对它们进行测序。使用iPair分析仪软件在单细胞水平上鉴定γ和δ链的序列和配对。
图3A和图3B显示了肿瘤与PBMC中γ链使用的CDR3树图比较。图3A显示了解离肿瘤中γ链CDR3序列的多样性。前10种CDR3的序列列于CDR3树图下方。图3B了显示PBMC中γ链CDR3序列的多样性。前10种CDR3的序列列于CDR3树图下方。
图4A和图4B显示了肿瘤与PBMC中δ链使用的CDR3树图比较。图4A显示了解离肿瘤中δ链CDR3序列的多样性。前10种CDR3的序列列于CDR3树图下方。图4B显示了PBMC中δ链CDR3序列的多样性。前10种CDR3的序列列于CDR3树图下方。
图5A至图5D显示了选择的癌症基因组图谱(TCGA)肿瘤类型中的γδTCR(TRGV和TRDV)组成。显示了结直肠腺癌(图5A)、弥漫性大B细胞淋巴瘤(图5B)、肉瘤(图5C)和胃腺癌(图5D)的γδTCR(TRGV和TRDV)组成。
图6A至图6F显示了外周血和肿瘤中γδTCR的CDR3序列分析。图6A显示了来自结直肠肿瘤的Vγ链的单细胞RNA测序。图6B显示了来自结直肠肿瘤的Vδ链的单细胞RNA测序。图6C显示了来自匹配的外周血的Vγ链的单细胞RNA测序。图6D显示了来自匹配的外周血的Vδ链的单细胞RNA测序。图6E显示了结直肠癌肿瘤中Vγ和Vδ链的CDR3序列分析。图6F显示了外周血中Vγ和Vδ链的CDR3序列分析。
图7A至图7F显示了结直肠腺癌中BTN/L和γδTCR表达的关联性。通过TCGA数据集的分析,对在结直肠腺癌肿瘤中检测到的选择的BTN/L蛋白(BTN3A1(图7A)、BTN2A1(图7B)、BTNL3(图7C)和BTNL8(图7D)、γ链(TRGV9)(图7E)和δ链(TRDV1)(图7F)的RNA表达进行Spearman相关分析。
图8A至图8B显示了基于Jurkat-76细胞系的体外测定的开发,该测定用于筛选可激活使用单细胞RNA测序所检测的特定γδTCR的BTN/L配对。图8A显示了所述测定的示意图。显示了Jurkat-76报告细胞系开发的图示(上图),该细胞系在γδT细胞激活后表现出CD69表达(下图)。图8B显示了来自Jurkat-76报告系统之一(表达Vγ9δ2TCR)的代表性数据。
图9显示了GADLEN治疗剂的产生的非限制性示意图。不受理论的束缚,GADLEN治疗剂通过BTN/L异二聚体结构域激活γδTCR并引起肿瘤细胞的靶向杀伤。
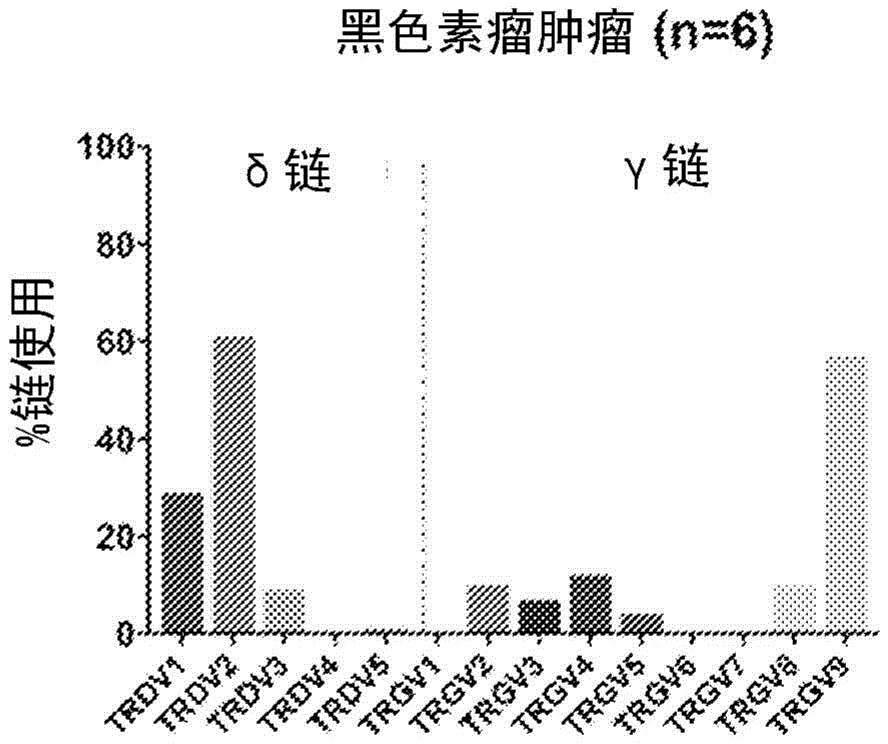
图10A至图10C显示了在黑色素瘤肿瘤(图10A)、非小细胞肺肿瘤(图10B)和结直肠癌肿瘤(图10C)中γ(TRGV)和δ(TRDV)链T细胞受体的使用。
发明详述
本公开部分基于以下发现:在包括黑色素瘤、前列腺癌和结肠癌患者在内的人类癌症患者中,对个体γ/δT细胞TCR的组织特异性偏好以及相应的对个体嗜乳脂蛋白的组织特异性偏好;以及,特定的γ/δT细胞群优先被特定的嗜乳脂蛋白异二聚体以锁和钥匙(lock-and-key)的方式激活。因此,本公开涉及选择患者用嵌合蛋白进行抗癌治疗,所述嵌合蛋白尤其能够靶向组织特异性γδT细胞并引起其激活,同时还与肿瘤细胞形成突触(synapse)。
免疫检查点抑制的获得性抵抗的一个主要机制涉及抗原呈递的下调,包括主要组织相容性复合物(MHCI)本身。MHCI上抗原呈递的下调可以使肿瘤细胞看不见α/β(αβ)T细胞引导的治疗。γ/δ(γδ)T细胞是整体T细胞库的一个小的亚组,但其特征却在于相对于αβT细胞具有增加的溶细胞能力。γδT细胞不是通过MHCI,而是通过异二聚体化的嗜乳脂蛋白(BTN)的复合物来识别靶细胞。因此,在肿瘤细胞表面的展示BTN异二聚体可以增强对MHC I下调的肿瘤或对表达低丰度或低亲和力抗原的肿瘤的免疫力。
本文提供的数据尤其鉴定了个体γδT细胞TCR的组织特异性富集,以及对个体BTN蛋白的相应组织特异性偏好。基于此信息,生成了一组独特的异二聚体BTN蛋白。数据尤其表明,不受理论的束缚,特异的γδT细胞群优先被特异的BTN异二聚体以锁和钥匙的方式激活。因此,在一些方面,本公开涉及一种鉴定癌症治疗物的方法,所述方法包括:(a)获得生物样品,所述样品包含一种或多种γ/δT细胞;(b)评估样品中一种或多种γ/δT细胞受体(TCR)链和/或一种或多种嗜乳脂蛋白的存在、不存在或水平;和(c)选择具有在γ/δTCR、一种或多种嗜乳脂蛋白或其片段处发出信号的能力的癌症治疗物。
适用于癌症治疗物的异二聚体蛋白
在一个方面,本公开涉及使用异二聚体蛋白的癌症治疗物,所述异二聚体蛋白包含:(a)第一结构域,其包含一个或多个嗜乳脂蛋白家族蛋白或其片段;(b)第二结构域,其包含靶向结构域,所述靶向结构域选自(i)抗体、抗体样分子或其抗原结合片段,和(ii)胞外结构域;和(c)接头,其连接第一结构域和第二结构域。在多个实施方案中,所述异二聚体蛋白包含两条多肽链,其中第一多肽链和第二多肽链包含(a)第一结构域,其包含一个或多个嗜乳脂蛋白家族蛋白或其片段;(b)第二结构域,其包含靶向结构域,所述靶向结构域选自(i)抗体、抗体样分子或其抗原结合片段,和(ii)胞外结构域;和(c)接头,其连接第一结构域和第二结构域。在多个实施方案中,异二聚体蛋白包含自结合的两条单独的多肽链。在多个实施方案中,第一多肽链和第二多肽链的包含一个或多个嗜乳脂蛋白家族蛋白或其片段的第一结构域是相同的。在多个实施方案中,第一和第二多肽链的包含靶向结构域的第二结构域是相同的。在多个实施方案中,连接第一和第二结构域的接头是相同的。
在一个方面,本公开涉及使用包含α链和β链的异二聚体蛋白的癌症治疗物,其中所述α链和β链各自独立地包含:(a)第一结构域,其包含一个或多个嗜乳脂蛋白家族蛋白或其片段;(b)第二结构域,其包含靶向结构域,所述靶向结构域选自(i)抗体、抗体样分子或其抗原结合片段,和(ii)胞外结构域;和(c)接头,其连接第一结构域和第二结构域。在多个实施方案中,异二聚体蛋白包含自结合(self-associate)的α链和β链。在多个实施方案中,α链和β链的包含一个或多个嗜乳脂蛋白家族蛋白或其片段的第一结构域是相同的。在多个实施方案中,α链和β链的包含靶向结构域的第二结构域是相同的。在多个实施方案中,连接α链和β链的第一结构域和第二结构域的接头是相同的。
适用于本文公开的方法的示例性异二聚体蛋白公开于PCT国际专利申请公开号WO2020146393和PCT国际专利申请公开号PCT/US2021/027294中,其全部内容通过引用并入本文。
嗜乳脂蛋白家族蛋白或其片段
本文公开的适合于癌症治疗的异二聚体蛋白包含第一结构域,所述第一结构域包含一个或多个嗜乳脂蛋白家族蛋白或其片段。在多个实施方案中,嗜乳脂蛋白家族蛋白选自BTN1A1、BTN2A1、BTN2A2、BTN2A3、BTN3A1、BTN3A2、BTN3A3、BTNL2、BTNL3、BTNL8、BTNL9、BTNL10和SKINTL。在多个实施方案中,第一结构域包括:(a)BTN1A1、BTN2A1、BTN2A2、BTN2A3、BTN3A1、BTN3A2、BTN3A3、BTNL2、BTNL3、BTNL8、BTNL9、BTNL10和SKINTL中的任一种;(b)BTN1A1、BTN2A1、BTN2A2、BTN2A3、BTN3A1、BTN3A2、BTN3A3、BTNL2、BTNL3、BTNL8、BTNL9、BTNL10和SKINTL中的任一种。在多个实施方案中,第一结构域包含:(a)人BTN1A1、人BTN2A1、人BTN2A2、人BTN2A3、人BTN3A1、人BTN3A2、人BTN3A3、人BTNL2、人BTNL3、人BTNL8、人BTNL9、人BTNL10和人SKINTL中的任一种,和(b)人BTN1A1、人BTN2A1、人BTN2A2、人BTN2A3、人BTN3A1、人BTN3A2、人BTN3A3、人BTNL2、人BTNL3、人BTNL8、人BTNL9、人BTNL10和人SKINTL中的任一种。
在多个实施方案中,第一结构域包含嗜乳脂蛋白家族蛋白的片段,其中所述片段能够结合γδT细胞受体并且任选地是胞外结构域,任选地包含一种或多种免疫球蛋白V(IgV)样结构域和IgC样结构域。在多个实施方案中,第一结构域包含嗜乳脂蛋白家族蛋白的片段,其中所述片段能够结合选自Vγ2、Vγ3、Vγ4、Vγ5、Vγ8、Vγ9、Vγ11、Vδ1、Vδ2、Vδ3、Vδ4、Vδ5、Vδ6、Vδ7和Vδ8的γδT细胞受体。
在多个实施方案中,第一结构域包含两个相同的嗜乳脂蛋白家族蛋白。在多个实施方案中,其中第一结构域包含两个不同的嗜乳脂蛋白家族蛋白。在多个实施方案中,嗜乳脂蛋白家族蛋白包含V型结构域。合适的嗜乳脂蛋白家族蛋白或其片段衍生自天然嗜乳脂蛋白家族蛋白,其包含在全长蛋白的胞质尾部的B30.2结构域。
在多个实施方案中,第一结构域是嗜乳脂蛋白亚家族2成员A1(BTN2A1)的部分。在多个实施方案中,第一结构域包含BTN2A1的基本上全部的胞外结构域。在多个实施方案中,第一结构域能够结合γδT细胞受体(例如Vγ9δ2)。BTN2A1也称为BT2.1,BTF1。在多个实施方案中,所述BTN2A1的部分是BTN2A1胞外结构域的部分。在多个实施方案中,本发明的嵌合蛋白还包含结构域,例如BTN2A1胞外结构域。
人BTN2A1的胞外结构域的氨基酸序列(其是适合于本公开的人BTN2A1的示例性氨基酸序列)如下:
QFIVVGPTDPILATVGENTTLRCHLSPEKNAEDMEVRWFRSQFSPAVFVYKGGRERTEEQMEEYRGRTTFVSKDISRGSVALVIHNITAQENGTYRCYFQEGRSYDEAILHLVVAGLGSKPLISMRGHEDGGIRLECISRGWYPKPLTVWRDPYGGVAPALKEVSMPDADGLFMVTTAVIIRDKSVRNMSCSINNTLLGQKKESVIFIPESFMPSVSPCA(SEQ ID NO:24)
在多个实施方案中,适合于本公开的人BTN2A1的胞外结构域的片段是Ig样V型结构域,其具有以下序列:
QFIVVGPTDPILATVGENTTLRCHLSPEKNAEDMEVRWFRSQFSPAVF VYKGGRERTEEQMEEYRGRTTFVSKDISRGSVALVIHNITAQENGTYRCY FQEGRSYDEAILHLV(SEQ ID NO:25)
在多个实施方案中,适合于癌症治疗的异二聚体蛋白包含人BTN2A1的胞外结构域,其具有SEQ ID NO:24或SEQ ID NO:25的氨基酸序列。在多个实施方案中,本发明的嵌合蛋白可包含如本文所述的BTN2A1的胞外结构域或其变体或功能片段。例如,嵌合蛋白可包含如上文所提供的BTN2A1的胞外结构域的序列,或与本文所述的BTN2A1的胞外结构域的氨基酸序列具有至少约60%、或至少约61%、或至少约62%、或至少约63%,或至少约64%、或至少约65%、或至少约66%、或至少约67%、或至少约68%、或至少约69%、或至少约70%、或至少约71%、或至少约72%、或至少约73%、或至少约74%、或至少约75%、或至少约76%、或至少约77%、或至少约78%、或至少约79%、或至少约80%、或至少约81%、或至少约82%、或至少约83%、或至少约84%、或至少约85%、或至少约86%、或至少约87%、或至少约88%、或至少约89%、或至少约90%、或至少约91%、或至少约92%、或至少约93%、或至少约94%、或至少约95%、或至少约96%、或至少约97%、或至少约98%、或至少约99%序列同一性的变体或功能片段。
BTN2A1衍生物可以从可用的结构数据构建,所述数据包括Karunakaran等,Butyrophilin-2A1 Directly Binds Germline-Encoded Regions of the Vγ9Vδ2TCRand Is Essential for Phosphoantigen Sensing,Immunity.52(3):487-498(2020)描述的同源模型。此外,不希望受到理论的束缚,BTN2A1的蛋白结构同源模型可在SWISS-MODEL存储库中获得。Bienert等,“The SWISS-MODEL Repository-new features andfunctionality.”Nucleic Acids Research,45(D1):D313-D319(2017)。从诱变中获得的额外结构见解。Rigau等,Butyrophilin 2A1 is essential for phosphoantigenreactivity byγδT cells.Science 367(6478):eaay5516(2020).
在多个实施方案中,第一结构域是嗜乳酪蛋白亚家族3成员A1(BTN3A1)的部分。在多个实施方案中,第一结构域包含BTN3A1的基本上全部的胞外结构域。在多个实施方案中,第一结构域能够结合γδT细胞受体(例如Vγ9δ2)。BTN3A1也称为BTF5。在多个实施方案中,所述BTN3A1的部分是BTN3A1的胞外结构域的部分。在多个实施方案中,本发明的嵌合蛋白还包含结构域,例如BTN3A1胞外结构域。
人BTN3A1的胞外结构域的氨基酸序列(其是适合于本公开的人BTN3A1的示例性氨基酸序列)如下:
QFSVLGPSGPILAMVGEDADLPCHLFPTMSAETMELKWVSSSLRQVVNVYADGKEVEDRQSAPYRGRTSILRDGITAGKAALRIHNVTASDSGKYLCYFQDGDFYEKALVELKVAALGSDLHVDVKGYKDGGIHLECRSTGWYPQPQIQWSNNKGENIPTVEAPVVADGVGLYAVAASVIMRGSSGE
GVSCTIRSSLLGLEKTASISIADPFFRSAQRWIAALAG(SEQ ID NO:26)
在一些实施方案中,人BTN3A1的胞外结构域的片段是Ig样V-1型结构域,其具有以下序列:
QFSVLGPSGPILAMVGEDADLPCHLFPTMSAETMELKWVSSSLRQ VVNVYADGKEVEDRQSAPYRGRTSILRDGITAGKAALRIHNVTASDSG KYLCYFQDGDFYEKALVELKVA(SEQ ID NO:27)
在多个实施方案中,适合于癌症治疗的异二聚体蛋白包含人BTN3A1的胞外结构域,其具有SEQ ID NO:26或SEQ ID NO:27的氨基酸序列。在多个实施方案中,本发明的嵌合蛋白可包含如本文所述的BTN3A1的胞外结构域或其变体或功能片段。例如,嵌合蛋白可包含如上文所提供的BTN3A1的胞外结构域的序列,或与本文所述的BTN3A1的胞外结构域的氨基酸序列具有至少约60%、或至少约61%、或至少约62%、或至少约63%,或至少约64%、或至少约65%、或至少约66%、或至少约67%、或至少约68%、或至少约69%、或至少约70%、或至少约71%、或至少约72%、或至少约73%、或至少约74%、或至少约75%、或至少约76%、或至少约77%、或至少约78%、或至少约79%、或至少约80%、或至少约81%、或至少约82%、或至少约83%、或至少约84%、或至少约85%、或至少约86%、或至少约87%、或至少约88%、或至少约89%、或至少约90%、或至少约91%、或至少约92%、或至少约93%、或至少约94%、或至少约95%、或至少约96%、或至少约97%、或至少约98%、或至少约99%序列同一性的变体或功能片段。
BTN3A1衍生物可以从可用的结构数据构建,所述数据包括以下:Palakodeti等,Themolecularbasisformodulationofhuman V(gamma)9V(delta)2TcellresponsesbyCD277/Butyrophilin-3(BTN3A)-specific antibodies,J Biol Chem 287:32780-32790(2012);Vavassori等,Butyrophilin 3A1 binds phosphorylated antigens and stimulateshuman gamma delta T cells.Nat Immunol 14:908-916(2013);Sandstrom等,TheIntracellular B30.2 Domain of Butyrophilin 3A1 Binds Phosphoantigens toMediate Activation of Human V gamma 9V delta 2 T Cells.Immunity 40:490-500(2014);Rhodes等,Activation of Human Gammadelta T Cells by CytosolicInteractions of Btn3A1 with Soluble Phosphoantigens and the CytoskeletalAdaptor Periplakin.J Immunol 194:2390(2015);Gu等,Phosphoantigen-inducedconformational change of butyrophilin 3A1(BTN3A1)and its implication on Vgamma 9V delta 2 T cell activation.Proc Natl Acad Sci U S A 114:E7311-E7320(2017);Salim等,BTN3A1 Discriminates gamma delta T Cell Phosphoantigens fromNonantigenic Small Molecules via a Conformational Sensor in Its B30.2Domain.ACS Chem Biol 12:2631-2643(2017);Yang等,A Structural Change inButyrophilin upon Phosphoantigen Binding Underlies Phosphoantigen-Mediated Vgamma 9V delta 2 T Cell Activation.Immunity 50:1043(2019)。
在多个实施方案中,第一结构域包括BTN2A1的部分。在多个实施方案中,所述BTN2A1的部分是BTN2A1的胞外结构域或其γδT细胞受体(例如γ9δ2)结合片段。
在多个实施方案中,第一结构域包括BTN3A1的部分。在多个实施方案中,所述BTN3A1的部分是BTN3A1的胞外结构域或其γδT细胞受体(例如γ9δ2)结合片段。
适合于本公开的小鼠BTNL1的示例性氨基酸序列是:
EVSWFSVKGPAEPITVLLGTEATLPCQLSPEQSAARMHIRWYRAQPTPAVLVFHNGQEQGEVQMPEYRGRTQMVRQAIDMGSVALQIQQVQASDDGLYHCQFTDGFTSQEVSMELRVIGLGSAPLVHMTGPENDGIRVLCSSSGWFPKPKVQWRDTSGNMLLSSSELQTQDREGLFQVEVSLLVTDRAIGNVICSIQNPMYDQEKSKAILLPEPFFPKTCPWK(SEQ ID NO:28)
适用于本公开的小鼠BTNL6的示例性氨基酸序列:
EQLPEYSQRTSLVKEQFHQGTAAVRILNVQAPDSGIYICHFKQGVFYEEAILELKVAAMGSVPEVYIKGPEDGGVCVVCITSGWYPEPQVHWKDSRGEKLTASLEIHSEDAQGLFRTETSLVVRDSSVRNVTCSTFNPILGQEKAMAMFLPEPFFPKVSPWKP(SEQ ID NO:29)
适用于本公开的人BTNL3的示例性氨基酸序列如下:
QWQVTGPGKFVQALVGEDAVFSCSLFPETSAEAMEVRFFRNQFHAVVHLYRDGEDWESKQMPQYRGRTEFVKDSIAGGRVSLRLKNITPSDIGLYGCWFSSQIYDEEATWELRVAALGSLPLISIVGYVDGGIQLLCLSSGWFPQPTAKWKGPQGQDLSSDSRANADGYSLYDVEISIIVQENAGSILCSIHLAEQSHEVESKVLIGETFFQPSPWRLAS(SEQ ID NO:30)
适合于本公开的人BTN3A2的示例性氨基酸序列:
QFSVLGPSGPILAMVGEDADLPCHLFPTMSAETMELKWVSSSLRQVVNVYADGKEVEDRQSAPYRGRTSILRDGITAGKAALRIHNVTASDSGKYLCYFQDGDFYEKALVELKVAALGSNLHVEVKGYEDGGIHLECRSTGWYPQPQIQWSNAKGENIPAVEAPVVADGVGLYEVAASVIMRGGSGEGVSCIIRNSLLGLEKTASISIADPFFRSAQPW(SEQ ID NO:31)
适合于本公开的人BTNL8的示例性氨基酸序列如下:
QWQVFGPDKPVQALVGEDAAFSCFLSPKTNAEAMEVRFFRGQFSSVVHLYRDGKDQPFMQMPQYQGRTKLVKDSIAEGRISLRLENITVLDAGLYGCRISSQSYYQKAIWELQVSALGSVPLISITGYVDRDIQLLCQSSGWFPRPTAKWKGPQGQDLSTDSRTNRDMHGLFDVEISLTVQENAGSISCSMRHAHLSREVESRVQIGDTFFEPISWHLATK(SEQ ID NO:32)
在多个实施方案中,适合于癌症治疗的异二聚体蛋白可包含人BTN2A1、BTN3A1、BTNL1、BTNL3、BTN3A2、BTNL8的一个或多个胞外结构域,其分别具有SEQ ID NO:24、SEQ IDNO:26、SEQ ID NO:28、SEQ ID NO:30、SEQ ID NO:31和SEQ ID NO:32的氨基酸序列。在多个实施方案中,本发明的嵌合蛋白可包含如本文所述的人BTN2A1、BTN3A1、BTNL1、BTNL3、BTN3A2、BTNL8的胞外结构域中的一个或多个的胞外结构域或其变体或功能片段。在多个实施方案中,所述片段是来自SEQ ID NO:24、SEQ ID NO:26、SEQ ID NO:28、SEQ ID NO:30、SEQ ID NO:31和SEQ ID NO:32中的一个或多个的Ig样V型结构域。例如,嵌合蛋白可以包含如上提供的BTN3A1的胞外结构域的序列,或与本文所述的人BTN2A1、BTN3A1、BTNL1、BTNL3、BTN3A2、BTNL8的胞外结构域中的一个或多个的胞外结构域的氨基酸序列具有至少约60%、或至少约61%、或至少约62%、或至少约63%,或至少约64%、或至少约65%、或至少约66%、或至少约67%、或至少约68%、或至少约69%、或至少约70%、或至少约71%、或至少约72%、或至少约73%、或至少约74%、或至少约75%、或至少约76%、或至少约77%、或至少约78%、或至少约79%、或至少约80%、或至少约81%、或至少约82%、或至少约83%、或至少约84%、或至少约85%、或至少约86%、或至少约87%、或至少约88%、或至少约89%、或至少约90%、或至少约91%、或至少约92%、或至少约93%、或至少约94%、或至少约95%、或至少约96%、或至少约97%、或至少约98%、或至少约99%序列同一性的其变体或功能片段。
在多个实施方案中,本发明的异二聚体蛋白包含两个独立的结合结构域,每个结合结构域来自异二聚体人类蛋白的一个亚基。下表中提供了可以作为本发明异二聚体蛋白的一部分而形成的示例性蛋白。在多个实施方案中,本发明的异二聚体蛋白具有一种下表中提供的示例性蛋白。在多个实施方案中,本发明的异二聚体蛋白具有两种下表中提供的示例性蛋白。
可以并入本发明组合物和方法中的其他示例性嗜乳脂蛋白样(BTNL)家族蛋白包括以下蛋白(如本文所用,“条目”是指Uniprot数据库中的蛋白条目,“条目名称”是指Uniprot数据库中的蛋白条目):
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
在多个实施方案中,适合于癌症治疗的异二聚体蛋白可包含存在于SEQ ID NO:24、SEQ ID NO:26和SEQ ID NO:28至SEQ ID NO:45的氨基酸中的胞外结构域的一个或多个。在多个实施方案中,本发明的嵌合蛋白可以包含存在于如本文所述的SEQ ID NO:24、SEQ ID NO:26和SEQ ID NO:28至SEQ ID NO:45的氨基酸中的胞外结构域或其变体或功能片段。在多个实施方案中,所述片段是来自SEQ ID NO:24、SEQ ID NO:26和SEQ ID NO:28至SEQ ID NO:45中的一个或多个的Ig样V型结构域。例如,嵌合蛋白可包含如上文所提供的BTN3A1的胞外结构域的序列,或与存在于本文所述的SEQ ID NO:24、SEQ ID NO:26和SEQID NO:28至45的氨基酸中的氨基酸序列具有至少约60%、或至少约61%、或至少约62%、或至少约63%,或至少约64%、或至少约65%、或至少约66%、或至少约67%、或至少约68%、或至少约69%、或至少约70%、或至少约71%、或至少约72%、或至少约73%、或至少约74%、或至少约75%、或至少约76%、或至少约77%、或至少约78%、或至少约79%、或至少约80%、或至少约81%、或至少约82%、或至少约83%、或至少约84%、或至少约85%、或至少约86%、或至少约87%、或至少约88%、或至少约89%、或至少约90%、或至少约91%、或至少约92%、或至少约93%、或至少约94%、或至少约95%、或至少约96%、或至少约97%、或至少约98%、或至少约99%序列同一性的其变体或功能片段,和/或其中存在的一种或多种Ig样V型结构域。
包含靶向结构域的第二结构域
本文公开的任何实施方案的异二聚体蛋白包含含有靶向结构域的第二结构域。在多个实施方案中,靶向结构域是抗体样分子或其抗原结合片段。在多个实施方案中,抗体样分子选自单域抗体、重组仅重链抗体(VHH)、单链抗体(scFv)、鲨鱼仅重链抗体(VNAR)、微蛋白(半胱氨酸结蛋白,打结素(knottin))、DARPin、Tetranectin、Affibody、Transbody、Anticalin、AdNectin、Affilin、Affimer、Microbody、适体、alterase、塑料抗体(plasticantibody)、phylomer、stradobody、maxibody、evibody、fynomer、犰狳重复蛋白、Kunitz结构域、avimer、atrimer、probody、immunobody、triomab、troybody、pepbody、vaccibody、UniBody、DuoBody、Fv、Fab、Fab'和F(ab')
连接第一结构域和第二结构域的接头
在多个实施方案中,连接第一结构域和第二结构域的接头包含电荷极化核心结构域(charge polarized core domain)。在多个实施方案中,第一和第二电荷极化核心结构域各自包含在所述核心结构域的氨基和羧基末端具有带正电荷或带负电荷的氨基酸残基的蛋白。在示例性实施方案中,第一电荷极化核心结构域可包含在氨基末端具有带正电荷的氨基酸的蛋白,其通过接头(例如,稳定结构域)连接在羧基末端具有带负电荷的氨基酸残基的蛋白。第二电荷极化核心结构域可包含在氨基末端具有带负电荷的氨基酸的蛋白,其通过接头(例如,稳定结构域)连接在羧基末端具有带正电荷的氨基酸残基的蛋白。
在另一个示例性实施方案中,第一电荷极化核心结构域可以包含在氨基末端具有带负电荷的氨基酸的蛋白,其通过接头(例如,稳定结构域)连接在羧基末端具有带正电荷的氨基酸残基的蛋白。第二电荷极化核心结构域可包含在氨基末端具有带正电荷的氨基酸的蛋白,其通过接头(例如,稳定结构域)连接在羧基末端具有带负电荷的氨基酸残基的蛋白。
在多个实施方案中,异二聚体蛋白的形成是由位于第一和第二电荷极化核心结构域的氨基和羧基末端的带正电荷和带负电荷的氨基酸残基之间的静电相互作用驱动的。此外,通过位于第一和第二电荷极化核心结构域的氨基和羧基末端的带正电荷的氨基酸残基或带负电荷的氨基酸残基之间的排斥来防止同二聚体蛋白的形成。
在多个实施方案中,在电荷极化核心结构域的氨基或羧基末端包含带正电和/或带负电荷的氨基酸残基的所述蛋白的长度为约2至约50个氨基酸。例如,在电荷极化核心结构域任一末端包含带正电荷和/或带负电荷的氨基酸残基的所述蛋白可以是约50、约45、约40、约35、约30、约25、约20、约19、约18、约17、约16、约15、约14、约13、约12、约11、约10、约9、约8、约7、约6、约5、约4、约3或约2个氨基酸长。
在多个实施方案中,包含带正电荷的氨基酸残基的所述蛋白可包含选自His、Lys和Arg的一个或多个氨基酸。在多个实施方案中,包含带负电荷的氨基酸残基的所述蛋白可包含选自Asp和Glu的一个或多个氨基酸。
在多个实施方案中,第一和/或第二电荷极化核心结构域中的每一个可包含含有如下表中提供的氨基酸序列或与其具有至少90%、或93%、或95%、或97%、或98%、或99%同一性的氨基酸序列的蛋白。
/>
例如,在一个实施方案中,第一和第二电荷极化核心结构域中的每一个可包含含有序列YY
在另一个示例性实施方案中,第一和第二电荷极化核心结构域中的每一个可包含含有序列YY
在一个方面,本公开提供了一种异二聚体蛋白,其包含(a)第一结构域,其包含一个或多个嗜乳脂蛋白家族蛋白或其片段;(b)第二结构域,其包含靶向结构域,所述靶向结构域选自(i)抗体、抗体样分子或其抗原结合片段,和(ii)胞外结构域;和(c)接头,其连接第一和第二结构域。在多个实施方案中,异二聚体蛋白包含自结合的两条单独的多肽链。在多个实施方案中,接头促进异二聚化。在多个实施方案中,异二聚体蛋白包含两个相同的嗜乳脂蛋白家族蛋白或两个不同的嗜乳脂蛋白家族蛋白。在多个实施方案中,嗜乳脂蛋白家族蛋白包含V型结构域和/或B30.2结构域。在多个实施方案中,第一结构域是嗜乳脂蛋白样(BTNL)家族蛋白,例如BTN1A1、BTN2A1、BTN2A2、BTN2A3、BTN3A1、BTN3A2、BTN3A3、BTNL2、BTNL3、BTNL8、BTNL9、BTNL10和SKINTL。
下面提供了连接第一结构域和第二结构域的接头(在本文中也称为核心结构域)的示例性序列:
在多个实施方案中,核心结构域具有以下序列:
在多个实施方案中,核心结构域具有以下序列:
/>
在多个实施方案中,核心结构域是具有以下序列的KIHT22Y蛋白(T至Y突变以下划线、粗体字体表示):
在多个实施方案中,核心结构域是具有以下序列的KIHY86T蛋白(Y至T突变以下划线、粗体字体表示):
在多个实施方案中,核心结构域是具有以下序列的KIHY86T蛋白:
下面提供了示例性电荷极化核心结构域(正-负)的序列(带正电荷的肽以下划线字体显示,带负电荷的肽以粗体、下划线字体表示):
下面提供了示例性电荷极化核心结构域(负-正)的序列(带正电荷的肽以下划线字体显示,带负电荷的肽以粗体、下划线字体表示):
下面提供了示例性电荷极化核心结构域(负-正)的序列:
在多个实施方案中,包含带电荷的氨基酸残基的蛋白还可包含一个或多个半胱氨酸残基以促进带静电核心结构域之间的二硫键键合,作为稳定异二聚体的另一种方法。
在多个实施方案中,第一和第二电荷极化核心结构域各自包含可任选地充当稳定结构域的接头序列。在多个实施方案中,接头可以衍生自天然存在的多结构域蛋白或者是实证的接头,如例如Chichili等,(2013),ProteinSci.22(2):153-167、Chen等,(2013),AdvDrugDelivRev.65(10):1357-1369中所描述,其全部内容通过引用并入本文。在多个实施方案中,可以使用接头设计数据库和计算机程序如Chen等,(2013),AdvDrugDelivRev.65(10):1357-1369和Crasto等,(2000),ProteinEng.13(5):309-312(其全部内容通过引用并入本文)中描述的那些来设计接头。
在多个实施方案中,接头(例如,稳定结构域)是合成接头,例如PEG。
在其他实施方案中,接头(例如稳定结构域)是多肽。在多个实施方案中,接头(例如,稳定结构域)的长度小于约500个氨基酸、小于约450个氨基酸、小于约400个氨基酸、小于约350个氨基酸、小于约300个氨基酸、小于约250个氨基酸、小于约200个氨基酸长、小于约150个氨基酸长或小于约100个氨基酸长。例如,接头(例如,稳定结构域)的长度可以少于约100、约95、约90、约85、约80、约75、约70、约65、约60、约55、约50、约45、约40、约35、约30、约25、约20、约19、约18、约17、约16、约15、约14、约13、约12、约11、约10、约9、约8、约7、约6、约5、约4、约3或约2个氨基酸。
在多个实施方案中,接头(例如,稳定结构域)基本上包含甘氨酸和丝氨酸残基(例如,约30%、或约40%、或约50%、或约60%、或约70%、或约80%、或约90%、或约95%、或约97%甘氨酸和丝氨酸)。
在多个实施方案中,接头(例如,稳定结构域)是抗体(例如,IgG、IgA、IgD和IgE,包括亚类(例如,IgGl、IgG2、IgG3和IgG4,以及IgA1和IgA2))的铰链区。IgG、IgA、IgD和IgE类抗体中的铰链区充当柔性间隔区,允许Fab部分在空间中自由移动。与恒定区相比,铰链结构域结构多样,各免疫球蛋白类别和亚类之间的序列和长度各不相同。例如,铰链区的长度和柔性在IgG亚类之间不同。IgG1的铰链区包含氨基酸216-231,并且由于它具有自由柔性,因此Fab片段可以绕其对称轴旋转,并在以两个重链间二硫桥中的第一个桥为中心的球体内移动。IgG2的铰链比IgG1短,有12个氨基酸残基和4个二硫桥。IgG2的铰链区缺乏甘氨酸残基,相对较短,并包含刚性的聚脯氨酸双螺旋,通过额外的重链间二硫键稳定。这些特性限制了IgG2分子的柔性。IgG3与其他亚类的不同之处在于其独特的延伸铰链区(大约是IgG1铰链长度的四倍),含有62个氨基酸(包括21个脯氨酸和11个半胱氨酸),形成非柔性的聚脯氨酸双螺旋。在IgG3中,Fab片段距离Fc片段相对较远,赋予分子更大的柔性。与其他亚类相比,IgG3中延伸的铰链也是其分子量较高的原因。IgG4的铰链区比IgG1的铰链区短,并且其柔性介于IgG1和IgG2之间。据报道,铰链区的柔性按照IgG3>IgG1>IgG4>IgG2的顺序降低。在其他实施方案中,接头可衍生自人IgG4并含有一个或多个突变以增强二聚化(包括S228P)或FcRn结合。
根据晶体学研究,免疫球蛋白铰链区在功能上可进一步细分为三个区域:上铰链区、核心区和下铰链区。参见Shin等,1992Immunological Reviews130:87。上铰链区包括从C
在多个实施方案中,接头(例如,稳定结构域)包含抗体(例如,IgG、IgA、IgD和IgE,包括亚类(例如,IgGl、IgG2、IgG3和IgG4,和IgA1和IgA2))的Fc结构域。在多个实施方案中,接头(例如稳定结构域)包含衍生自人IgG4抗体的铰链-CH2-CH3Fc结构域。在多个实施方案中,接头(例如稳定结构域)包含衍生自人IgG1抗体的铰链-CH2-CH3Fc结构域。在多个实施方案中,Fc结构域表现出对新生儿Fc受体(FcRn)的亲和力增加和结合增强。在多个实施方案中,Fc结构域包括增加对FcRn的亲和力并增强与FcRn的结合的一个或多个突变。不希望受到理论的束缚,认为对FcRn的亲和力的增加和与FcRn的结合的增强提高了本发明的异二聚体蛋白的体内半衰期。
在多个实施方案中,Fc结构域在氨基酸残基250、252、254、256、308、309、311、428、433或434(根据Kabat编号)或其等同物处含有一个或多个氨基酸取代。在一个实施方案中,氨基酸残基250处的氨基酸取代是用谷氨酰胺取代。在一个实施方案中,氨基酸残基252处的氨基酸取代是用酪氨酸、苯丙氨酸、色氨酸或苏氨酸取代。在一个实施方案中,氨基酸残基254处的氨基酸取代是用苏氨酸取代。在一个实施方案中,氨基酸残基256处的氨基酸取代是用丝氨酸、精氨酸、谷氨酰胺、谷氨酸、天冬氨酸或苏氨酸取代。在一个实施方案中,氨基酸残基308处的氨基酸取代是用苏氨酸取代。在一个实施方案中,氨基酸残基309处的氨基酸取代是用脯氨酸取代。在一个实施方案中,氨基酸残基311处的氨基酸取代是用丝氨酸取代。在一个实施方案中,氨基酸残基385处的氨基酸取代是用精氨酸、天冬氨酸、丝氨酸、苏氨酸、组氨酸、赖氨酸、丙氨酸或甘氨酸取代。在一个实施方案中,氨基酸残基386处的氨基酸取代是用苏氨酸、脯氨酸、天冬氨酸、丝氨酸、赖氨酸、精氨酸、异亮氨酸或甲硫氨酸取代。在一个实施方案中,氨基酸残基387处的氨基酸取代是用精氨酸、脯氨酸、组氨酸、丝氨酸、苏氨酸或丙氨酸取代。在一个实施方案中,氨基酸残基389处的氨基酸取代是用脯氨酸、丝氨酸或天冬酰胺取代。在一个实施方案中,氨基酸残基428处的氨基酸取代是用亮氨酸取代。在一个实施方案中,氨基酸残基433处的氨基酸取代是用精氨酸、丝氨酸、异亮氨酸、脯氨酸或谷氨酰胺取代。在一个实施方案中,氨基酸残基434处的氨基酸取代是用组氨酸、苯丙氨酸或酪氨酸取代。
在多个实施方案中,Fc结构域(例如,包含IgG恒定区)包含一个或多个突变,例如氨基酸残基252、254、256、433、434或436(根据Kabat编号)处的取代。在一个实施方案中,IgG恒定区包括三重M252Y/S254T/T256E突变或YTE突变。在另一个实施方案中,IgG恒定区包括三重H433K/N434F/Y436H突变或KFH突变。在进一步的实施方案中,IgG恒定区包括YTE和KFH突变的组合。
在多个实施方案中,本发明的修饰的人源化抗体包含IgG恒定区,其含有氨基酸残基250、253、307、310、380、428、433、434和435处的一个或多个突变。示例性突变包括T250Q、M428L、T307A、E380A、I253A、H310A、M428L、H433K、N434A、N434F、N434S和H435A。在一个实施方案中,IgG恒定区包含M428L/N434S突变或LS突变。在另一个实施方案中,IgG恒定区包含T250Q/M428L突变或QL突变。在另一个实施方案中,IgG恒定区包含N434A突变。在另一个实施方案中,IgG恒定区包含T307A/E380A/N434A突变或AAA突变。在另一个实施方案中,IgG恒定区包含I253A/H310A/H435A突变或IHH突变。在另一个实施方案中,IgG恒定区包含H433K/N434F突变。在另一个实施方案中,IgG恒定区包含M252Y/S254T/T256E和H433K/N434F突变的组合。
在多个实施方案中,引入突变以增加Fc结构域的稳定性和/或半衰期。示例性的Fc稳定突变体是S228P。另外的示例性的Fc半衰期延长突变体是T250Q、M428L、V308T、L309P和Q311S,并且本发明的接头(例如,稳定结构域)可以包含这些突变的1、或2、或3、或4、或5个。
IgG恒定区中的其他示例性突变描述在例如Robbie等,Antimicrobial Agentsand Chemotherapy(2013),57(12):6147-6153、Dall’Acqua等,JBC(2006),281(33):23514-24、Dall’Acqua等,Journal of Immunology(2002),169:5171-80、Ko等,Nature(2014)514:642-645、Grevys等,Journal of Immunology.(2015),194(11):5497-508和美国专利号7,083,784中,其全部内容通过引用并入本文。
在多个实施方案中,接头可以是柔性的,包括但不限于高度柔性。在多个实施方案中,接头可以是刚性的,包括但不限于刚性α螺旋。
在多个实施方案中,接头可以是有功能的。例如但不限于,接头可以起到改善本发明异二聚体蛋白的折叠和/或稳定性、改善表达、改善药代动力学和/或改善生物活性的作用。在另一个实例中,接头可以起到将异二聚体蛋白靶向特定细胞类型或位置的作用。
异二聚体蛋白
在一个方面,本发明提供了一种异二聚体蛋白,其适合于本发明的癌症治疗,所述异二聚体蛋白包含:(a)第一结构域,其包含一个或多个嗜乳脂蛋白家族蛋白或其片段;(b)第二结构域,其包含靶向结构域,所述靶向结构域选自(i)抗体、抗体样分子或其抗原结合片段,和(ii)胞外结构域;和(c)接头,其连接第一和第二结构域。
在多个实施方案中,异二聚体蛋白是两条多肽链的复合物。
在一个方面,本发明提供了一种异二聚体蛋白,其适合于本发明的癌症治疗,所述异二聚体蛋白包含α链和β链,其中所述α链和β链各自独立地包含(a)第一结构域,其包含嗜乳脂蛋白家族蛋白或其片段;(b)第二结构域,其包含靶向结构域,所述靶向结构域选自(i)抗体、抗体样分子或其抗原结合片段,和(ii)胞外结构域;和(c)接头,其连接第一和第二结构域。
在多个实施方案中,α链和β链自结合,以形成异二聚体。
在多个实施方案中,第一结构域包含两个相同的嗜乳脂蛋白家族蛋白。在多个实施方案中,其中第一结构域包含两个不同的嗜乳脂蛋白家族蛋白。在多个实施方案中,嗜乳脂蛋白家族蛋白包含V型结构域。在多个实施方案中,嗜乳脂蛋白家族蛋白或其片段衍生自天然嗜乳脂蛋白家族蛋白,其在胞质尾部包含B30.2结构域。
在多个实施方案中,嗜乳脂蛋白家族蛋白选自BTN1A1、BTN2A1、BTN2A2、BTN2A3、BTN3A1、BTN3A2、BTN3A3、BTNL2、BTNL3、BTNL8、BTNL9、BTNL10和SKINTL。在多个实施方案中,第一结构域包括:(a)BTN1A1、BTN2A1、BTN2A2、BTN2A3、BTN3A1、BTN3A2、BTN3A3、BTNL2、BTNL3、BTNL8、BTNL9、BTNL10和SKINTL中的任一种;和(b)BTN1A1、BTN2A1、BTN2A2、BTN2A3、BTN3A1、BTN3A2、BTN3A3、BTNL2、BTNL3、BTNL8、BTNL9、BTNL10和SKINTL中的任一种。在多个实施方案中,第一结构域包含:(a)人BTN1A1、人BTN2A1、人BTN2A2、人BTN2A3、人BTN3A1、人BTN3A2、人BTN3A3、人BTNL2、人BTNL3、人BTNL8、人BTNL9、人BTNL10和人SKINTL中的任一种,和(b)人BTN1A1、人BTN2A1、人BTN2A2、人BTN2A3、人BTN3A1、人BTN3A2、人BTN3A3、人BTNL2、人BTNL3、人BTNL8、人BTNL9、人BTNL10和人SKINTL中的任一种。
在多个实施方案中,第一结构域包含嗜乳脂蛋白家族蛋白的片段,其中所述片段能够结合γδT细胞受体并且任选地是胞外结构域,任选地包含一个或多个免疫球蛋白V(IgV)样结构域和IgC样结构域。在多个实施方案中,第一结构域包含嗜乳脂蛋白家族蛋白的片段,其中所述片段能够结合选自Vγ2、Vγ3、Vγ4、Vγ5、Vγ8、Vγ9、Vγ11、Vδ1、Vδ2、Vδ3、Vδ4、Vδ5、Vδ6、Vδ7和Vδ8的γδT细胞受体。
在多个实施方案中,第一结构域包含具有以下的氨基酸序列的多肽:(a)具有选自氨基酸序列SEQ ID NO:24至45的氨基酸序列的多肽或其片段;(b)具有选自氨基酸序列SEQID NO:24至45的氨基酸序列的多肽或其片段。在多个实施方案中,接头包含具有选自氨基酸序列SEQ ID NO:1-14的氨基酸序列的多肽。在多个实施方案中,接头包含具有选自氨基酸序列SEQ ID NO:15-22的氨基酸序列的多肽。
另外或可选地,在多个实施方案中,靶向结构域是抗体或其抗原结合片段。在多个实施方案中,靶向结构域是抗体样分子或其抗原结合片段。在多个实施方案中,抗体样分子选自单域抗体、重组仅重链抗体(VHH)、单链抗体(scFv)、鲨鱼仅重链抗体(VNAR)、微蛋白(半胱氨酸结蛋白,打结素)、DARPin、Tetranectin、Affibody、Transbody、Anticalin、AdNectin、Affilin、Affimer、Microbody、适体、alterase、塑料抗体、phylomer、stradobody、maxibody、evibody、fynomer、犰狳重复蛋白、Kunitz结构域、avimer、atrimer、probody、immunobody、triomab、troybody、pepbody、vaccibody、UniBody、DuoBody、Fv、Fab、Fab'和F(ab')
在多个实施方案中,接头包含(a)第一电荷极化核心结构域,其与嗜乳脂蛋白家族蛋白连接,任选在羧基末端连接,和(b)第二电荷极化核心结构域,其与嗜乳脂蛋白家族蛋白连接,任选在羧基末端连接。在多个实施方案中,接头通过第一和第二电荷极化核心结构域上带正电荷的氨基酸残基和带负电荷的氨基酸残基之间的静电相互作用形成异二聚体。在多个实施方案中,第一和/或第二电荷极化核心结构域包含多肽接头,任选地选自柔性氨基酸序列、IgG铰链区或抗体序列。在多个实施方案中,接头是合成接头,任选地是PEG。在多个实施方案中,接头包含衍生自IgG1,任选地衍生自人IgG1的铰链-CH2-CH3Fc结构域。在多个实施方案中,接头包含衍生自IgG4,任选地衍生自人IgG4的铰链-CH2-CH3Fc结构域。在多个实施方案中,第一和/或第二电荷极化核心结构域还包含在电荷极化核心结构域的氨基和/或羧基末端具有带正电荷和/或带负电荷的氨基酸残基的肽。在多个实施方案中,带正电荷的氨基酸残基包括选自His、Lys和Arg的一个或多个氨基酸。在多个实施方案中,带正电荷的氨基酸残基存在于在第一和/或第二电荷极化核心结构域中包含带正电荷的氨基酸残基的肽中。
在多个实施方案中,包含带正电荷的氨基酸残基的所述肽包含选自以下的序列:Y
另外或可选地,在多个实施方案中,第一结构域和/或异二聚体蛋白调节或能够调节γδ(gammadelta)T细胞。在多个实施方案中,γδT细胞选自表达Vγ4、Vγ9δ2或Vγ7δ4的细胞。在多个实施方案中,第一结构域包含BTNL3和BTNL8,并且其调节表达Vγ4的T细胞。在多个实施方案中,第一结构域包含BTNL2A1和BTNL3A1,并且其调节表达Vγ9δ2的T细胞。在多个实施方案中,第一结构域包含BTNL3A1和BTNL3A2,并且其调节表达Vγ9δ2的T细胞。在多个实施方案中,第一结构域包含BTNL3A1和BTNLA3,并且其调节表达Vγ9δ2的T细胞。在多个实施方案中,第一结构域包含BTNL1和BTNL6,并且其调节表达Vγ7δ4的T细胞。在多个实施方案中,γδT细胞的调节是γδT细胞的激活。
另外或可选地,在多个实施方案中,异二聚体蛋白能够在γδT细胞和肿瘤细胞之间形成突触。在多个实施方案中,异二聚体蛋白能够同时激活γδT细胞并将其靶向肿瘤细胞。
在多个实施方案中,本发明的异二聚体蛋白包含嗜乳脂蛋白样(BTNL)蛋白的部分。在示例性实施方案中,第一结构域是嗜乳脂蛋白样(BTNL)家族蛋白。BTNL家族蛋白的实例包括BTNL1、BTNL3、BTNL8、BTN3A1、BTN3A2和BTN3A3。在多个实施方案中,异源三聚体蛋白调节γδT细胞的功能。在多个实施方案中,除了BTNL家族蛋白之外,异二聚体蛋白还包含LAG-3、PD-1或TIGIT的胞外结构域的部分,并且其能够结合癌细胞表面上的其受体/配体。在多个实施方案中,除了BTNL家族蛋白之外,异二聚体蛋白还包含抗体或其片段(例如,包含抗体的抗原结合结构域的一部分和/或CDR3,其结合肿瘤表位)并且其能够结合癌细胞表面的抗原。
在多个实施方案中,本发明的异二聚体蛋白包含嗜乳脂蛋白样(BTNL)蛋白的部分。在示例性实施方案中,第一结构域是嗜乳脂蛋白样(BTNL)家族蛋白。BTNL家族蛋白的实例包括BTNL1、BTNL3、BTNL8、BTN3A1、BTN3A2和BTN3A3。在多个实施方案中,异三聚体蛋白调节γδT细胞的功能。在多个实施方案中,除了BTNL家族蛋白之外,异二聚体蛋白还包含LAG-3、PD-1、TIGIT、CD19、PSMA的胞外结构域的一部分或靶向肿瘤抗原(例如CD19或PSMA)的抗体衍生的结合结构域(例如CDR3、Fab、scFv结构域等),并且其能够结合癌细胞表面上的其受体/配体。在多个实施方案中,除了BTNL家族蛋白之外,异二聚体蛋白还包含抗体或其片段(例如,包含抗体的抗原结合结构域的部分),并且其能够结合癌细胞表面上的抗原。
在多个实施方案中,第二结构域是LAG-3蛋白。
在多个实施方案中,第二结构域是PD-1蛋白。
在多个实施方案中,第二结构域是TIGIT蛋白。
在多个实施方案中,第二结构域是CD19蛋白结合结构域,例如scFv、CDR3或Fab。在多个实施方案中,第二结构域是CD19蛋白,并且异二聚体蛋白进一步包含抗体或其片段(例如,包含抗体的抗原结合结构域的部分),并且其能够结合癌细胞表面上的抗原。
在多个实施方案中,第二结构域是PSMA蛋白结合结构域,例如scFv、CDR3或Fab。在多个实施方案中,第二结构域是PSMA蛋白,并且异二聚体蛋白进一步包含抗体或其片段(例如,包含抗体的抗原结合结构域的部分),并且其能够结合癌细胞表面上的抗原。
在示例性实施方案中,第二结构域是EGP的受体,例如EGFR(ErbB1)、ErbB2、ErbB3和ErbB4。
在示例性实施方案中,第二结构域是胰岛素或胰岛素类似物的受体,例如胰岛素受体和/或IGF1或IGF2受体。
在示例性实施方案中,第二结构域是EPO的受体,例如EPO受体(EPOR)受体和/或蝶素(ephrin)受体(EphR)。
在多个实施方案中,异二聚体蛋白可包含可溶性(例如,非膜相关的)蛋白的结构域。在多个实施方案中,异二聚体蛋白可以包含参与信号传导的可溶性蛋白的片段(例如,与受体相互作用的可溶性蛋白的部分)。
在多个实施方案中,异二聚体蛋白可包含跨膜蛋白的胞外结构域。在多个实施方案中,胞外结构域之一转导免疫抑制信号并且胞外结构域之一转导免疫刺激信号。
在多个实施方案中,胞外结构域是指能够与胞外环境相互作用的跨膜蛋白的部分。在多个实施方案中,胞外结构域是指跨膜蛋白的部分,其足以结合配体或受体并有效将信号传递至细胞。在多个实施方案中,胞外结构域是细胞或细胞膜外部的跨膜蛋白的完整氨基酸序列。在多个实施方案中,胞外结构域是跨膜蛋白的氨基酸序列的部分,其在细胞或细胞膜的外部并且是信号转导和/或配体结合所需要的,这可以使用本领域已知的方法进行测定(例如,体外配体结合和/或细胞激活测定)。
在多个实施方案中,免疫刺激信号是指增强免疫应答的信号。例如,在肿瘤学背景下,此类信号可以增强抗肿瘤免疫力。例如但不限于,可以通过直接刺激白细胞的增殖、细胞因子产生、杀伤活性或吞噬活性来鉴定免疫刺激信号。具体实例包括使用编码此类受体的配体(分别为IL-2、IL-7、IL-15、IL-17或IL-21)的融合蛋白直接刺激细胞因子受体,例如IL-2R、IL-7R、IL-15R、IL-17R或IL-21R。来自这些受体中任何一种的刺激都可能直接刺激单独的T细胞亚群的增殖和细胞因子产生。
在多个实施方案中,胞外结构域或抗体结合结构域(例如CDR3、Fab、scFv结构域等)可用于产生可溶性蛋白以竞争性抑制该受体的配体的信号传导。例如但不限于,可以使用PD-1来实现PD-L1或PD-L2的竞争性抑制,或者可以使用TIGIT来实现PVR的竞争性抑制。在多个实施方案中,胞外结构域或抗体结合结构域(例如CDR3、Fab、scFv结构域等)可用于提供人工信号传导。
在多个实施方案中,本发明的异二聚体蛋白递送或掩蔽免疫抑制信号。在多个实施方案中,本发明的异二聚体蛋白递送或掩蔽免疫刺激信号。
在多个实施方案中,本发明的异二聚体蛋白可被工程化以靶向驻留在人类白细胞上的一种或多种分子,包括但不限于:SLAMF4、IL-2Rα、IL-2Rβ、ALCAM、B7-1、IL-4R、B7-H3、BLAME/SLAMFS、CEACAM1、IL-6R、IL-7Rα、IL-10Rα、IL-l0Rβ、IL-12Rβ1、IL-12Rβ2、CD2、IL-13Rα1、IL-13、CD3、CD4、ILT2/CDS5j、ILT3/CDS5k、ILT4/CDS5d、ILT5/CDS5a、整合蛋白α4/CD49d、CDS、整合蛋白αE/CD103、CD6、整合蛋白αM/CD11b、CDS、整合蛋白αX/CD11c、整合蛋白β2/CDlS、KIR/CD15S、KIR2DL1、CD2S、KIR2DL3、KIR2DL4/CD15Sd、CD31/PECAM-1、KIR2DS4、LAG-3、CD43、LAIR1、CD45、LAIR2、CDS3、白三烯B4-R1、CDS4/SLAMF5、NCAM-L1、CD94、NKG2A、CD97、NKG2C、CD229/SLAMF3、NKG2D、CD2F-10/SLAMF9、NT-4、CD69、NTB-A/SLAMF6、常见γ链/IL-2Rγ、骨桥蛋白(Osteopontin)、CRACC/SLAMF7、PD-1、CRTAM、PSGL-1、CTLA-4、CX3CR1、CX3CL1、L-选择素(L-Selectin)、SIRPβ1、SLAM、TCCR/WSX-1、DNAM-1、促胸腺生成素(Thymopoietin)、EMMPRIN/CD147、TIM-1、EphB6、TIM-2、TIM-3、TIM-4、FcγRIII/CD16、TIM-6、溶粒素(Granulysin)、ICAM-1/CD54、ICAM-2/CD102、IFN-γR1、IFN-γR2、TSLP、IL-1R1和TSLP R的胞外结构域(如果适用的话)。
在多个实施方案中,本发明的异二聚体蛋白可被工程化以靶向参与免疫抑制的一种或多种分子,包括例如:CTLA-4、PD-L1、PD-L2、PD-1、BTLA、HVEM、TIM3、GAL9、LAG3、VISTA/VSIG8、KIR、2B4、TIGIT、CD160(也称为BY55)、CHK1和CHK2激酶、A2aR、CEACAM(例如,CEACAM-1、CEACAM-3和/或CEACAM-5)以及各种B-7家族配体(包括但不限于B7-1、B7-2、B7-DC、B7-H1、B7-H2、B7-H3、B7-H4、B7-H5、B7-H6和B7-H7)。
在多个实施方案中,本发明的异二聚体蛋白包含免疫抑制剂的胞外结构域。在多个实施方案中,本发明的异二聚体蛋白包含针对免疫抑制剂的抗体结合结构域(例如CDR3、Fab、scFv结构域等)。
在多个实施方案中,本发明的异二聚体蛋白包含可溶性蛋白或膜蛋白的胞外结构域,其具有免疫抑制特性。在多个实施方案中,本发明的异二聚体蛋白包含具有免疫抑制特性的抗体结合结构域(例如CDR3、Fab、scFv结构域等)。
在多个实施方案中,本发明的异二聚体蛋白模拟抑制信号配体与其同源受体的结合,但抑制抑制信号传递至免疫细胞(例如,T细胞、巨噬细胞或其他白细胞)。
在多个实施方案中,异二聚体蛋白包含免疫抑制受体胞外结构域或抗体结合结构域(例如CDR3、Fab、scFv结构域等)和免疫刺激配体胞外结构域或抗体结合结构域(例如CDR3、Fab、scFv结构域等),其能够但不限于向T细胞递送免疫刺激,同时掩蔽肿瘤细胞的免疫抑制信号。在多个实施方案中,异二聚体蛋白递送具有T细胞激活的最终结果的信号。
在多个实施方案中,本发明的异二聚体蛋白包含可溶性蛋白或膜蛋白的胞外结构域,其具有免疫刺激特性。在多个实施方案中,本发明的异二聚体蛋白包含具有免疫刺激特性的抗体结合结构域(例如CDR3、Fab、scFv结构域等)。
在多个实施方案中,本发明的异二聚体蛋白可包含任何已知细胞因子、生长因子和/或激素的变体。在多个实施方案中,本发明的异二聚体蛋白可以包含任何已知的细胞因子、生长因子和/或激素受体的变体。在多个实施方案中,本发明的异二聚体蛋白可包含任何已知胞外结构域的变体,例如,与已知的氨基酸或核酸序列具有至少约60%、或至少约61%、或至少约62%、或至少约63%,或至少约64%、或至少约65%、或至少约66%、或至少约67%、或至少约68%、或至少约69%、或至少约70%、或至少约71%、或至少约72%、或至少约73%、或至少约74%、或至少约75%、或至少约76%、或至少约77%、或至少约78%、或至少约79%、或至少约80%、或至少约81%、或至少约82%、或至少约83%、或至少约84%、或至少约85%、或至少约86%、或至少约87%、或至少约88%、或至少约89%、或至少约90%、或至少约91%、或至少约92%、或至少约93%、或至少约94%、或至少约95%、或至少约96%、或至少约97%、或至少约98%、或至少约99%序列同一性的序列。
在多个实施方案中,本发明的异二聚体蛋白可包含相对于任何已知蛋白序列具有一个或多个氨基酸突变的氨基酸序列。在多个实施方案中,所述一个或多个氨基酸突变可以独立地选自取代、插入、缺失和截短。
在多个实施方案中,氨基酸突变是氨基酸取代,并且可以包括保守和/或非保守取代。
“保守取代”可以例如基于所涉及的氨基酸残基的极性、电荷、大小、溶解度、疏水性、亲水性和/或两亲性质的相似性来进行。20种天然存在的氨基酸可分为以下六个标准氨基酸组:(1)疏水性:Met、Ala、Val、Leu、Ile;(2)中性亲水性:Cys、Ser、Thr;Asn、Gln;(3)酸性:Asp、Glu;(4)碱性:His、Lys、Arg;(5)影响链定向的残基:Gly、Pro;和(6)芳族:Trp、Tyr、Phe。
如本文所用,“保守取代”定义为一个氨基酸被在上述六个标准氨基酸组的同一组中列出的另一个氨基酸所交换。例如,用Glu交换Asp在如此修饰的多肽中保留一个负电荷。此外,甘氨酸和脯氨酸可以根据其破坏α-螺旋的能力而相互取代。
如本文所用,“非保守取代”定义为一个氨基酸被在上述六个标准氨基酸组(1)至(6)的不同组中列出的另一个氨基酸所交换。
在多个实施方案中,取代还可以包括非经典氨基酸(例如,硒代半胱氨酸、吡咯赖氨酸、N-甲酰甲硫氨酸、β-丙氨酸、GABA和δ-氨基乙酰丙酸、4-氨基苯甲酸(PABA)、常见氨基的D-异构体酸、2,4-二氨基丁酸、α-氨基异丁酸、4-氨基丁酸、Abu、2-氨基丁酸、γ-Abu、ε-Ahx、6-氨基己酸、Aib、2-氨基异丁酸、3-氨基丙酸、鸟氨酸、正亮氨酸、正缬氨酸、羟脯氨酸、sarcosme、瓜氨酸、高瓜氨酸、磺基丙氨酸、叔丁基甘氨酸、叔丁基丙氨酸、苯基甘氨酸、环己基丙氨酸、β-丙氨酸、氟代氨基酸、设计者氨基酸如β甲基氨基酸、Cα-甲基氨基酸、Nα-甲基氨基酸和一般氨基酸类似物)。
还可以参考遗传密码,包括考虑密码子简并性,对所述异二聚体蛋白的核苷酸序列进行突变。
在任何这些序列中,核心结构域具有的氨基酸序列是以下氨基酸序列或包含以下氨基酸序列:与选自氨基酸序列SEQ ID NO:15-22的氨基酸序列具有至少90%、或至少91%、或至少92%、或至少93%、或至少94%、或至少95%、或至少96%、或至少97%、或至少98%、或至少98%、或至少99%(例如,约90%、或约91%、或约92%、或约93%、或约94%、或约95%、或约96%、或约97%、或约98%、或约98%、或约99%)序列同一性的氨基酸序列。
在多个实施方案中,本发明的异二聚体蛋白能够并且可以用于包括促进免疫激活(例如,针对肿瘤的免疫激活)的方法中。在多个实施方案中,本发明的异二聚体蛋白能够并且可以用于包括阻抑免疫抑制(例如,允许肿瘤存活的免疫抑制)的方法中。在多个实施方案中,本发明的异二聚体蛋白提供改善的免疫激活和/或改善的对免疫抑制的阻抑。
在多个实施方案中,本发明的异二聚体蛋白能够或可以用于包括调节免疫应答的幅度,例如调节效应子输出水平的方法中。在多个实施方案中,例如,当用于治疗癌症时,与免疫抑制相比,本发明的异二聚体蛋白改变免疫刺激的程度,以增加T细胞应答的幅度,包括但不限于刺激细胞因子生产、增殖或靶标杀伤潜力的水平增加。
在多个实施方案中,向受试者进一步施用离体扩增的自体或同种异体γδT细胞。
在多个实施方案中,向受试者进一步施用表达嵌合抗原受体的自体或同种异体T细胞(即,CAR-T细胞)。CAR-T细胞描述于例如例如,Eshhar等,PNASUSA.90(2):720-724,1993;Geiger等,JImmunol.162(10):5931-5939,1999;Brentjens等,NatMed.9(3):279-286,2003;Cooper等,Blood101(4):1637-1644,2003;Imai等,Leukemia.18:676-684,2004;Pang等,Mol Cancer.2018;17:91和Schmidts等,Front.Immunol2018;9:2593中;其全部内容通过引用并入本文。
在多个实施方案中,当与嵌合抗原受体(CAR)T细胞治疗组合使用时,异二聚体蛋白发挥协同作用。在示例性实施方案中,当与CART细胞治疗组合使用以治疗肿瘤或癌症时,异二聚体蛋白发挥协同作用。在一个实施方案中,当与CART细胞治疗组合使用以治疗基于血液的肿瘤时,异二聚体蛋白发挥协同作用。在一个实施方案中,当与CART细胞治疗组合使用以治疗实体瘤时,异二聚体蛋白发挥协同作用。例如,异二聚体蛋白和CART细胞的使用可以协同作用以减少或消除肿瘤或癌症,或减缓肿瘤或癌症的生长和/或进展和/或转移。在多个实施方案中,本发明的异二聚体蛋白诱导CART细胞分裂。在多个实施方案中,本发明的异二聚体蛋白诱导CART细胞增殖。在多个实施方案中,本发明的异二聚体蛋白防止CART细胞的无反应性。
在多个实施方案中,CART细胞治疗包括靶向抗原(例如,肿瘤抗原)的CART细胞,所述抗原例如但不限于碳酸酐酶IX(CAIX)、5T4、CD19、CD20、CD22、CD30、CD33、CD38、CD47、CS1、CD138、Lewis-Y、L1-CAM、MET、MUC1、MUC16、ROR-1、IL13Rα2、gp100、前列腺干细胞抗原(PSCA)、前列腺特异性膜抗原(PSMA)、B细胞成熟抗原(BCMA)、人乳头瘤病毒16型E6(HPV-16E6)、CD171、叶酸受体α(FR-α)、GD2、GPC3、人表皮生长因子受体2(HER2)、κ轻链、间皮素、EGFR、EGFRvIII、ErbB、成纤维细胞激活蛋白(FAP)、癌胚抗原(CEA)、PMSA、受体酪氨酸激酶样孤儿受体1(ROR1)、TAG72和血管内皮生长因子受体2(VEGF-R2)以及本领域公知的其他肿瘤抗原。另外的示例性肿瘤抗原包括但不限于MART-1/Melan-A、gp100、二肽基肽酶IV(DPPIV)、腺苷脱氨酶结合蛋白(ADAbp)、亲环蛋白b、结直肠相关抗原(CRC)-0017-1A/GA733、癌胚抗原(CEA)及其免疫原性表位CAP-1和CAP-2、etv6、aml1、前列腺特异性抗原(PSA)及其免疫原性表位PSA-1、PSA-2和PSA-3、T细胞受体/CD3-zeta链、肿瘤抗原的MAGE家族(例如,MAGE-A1、MAGE-A2、MAGE-A3、MAGE-A4、MAGE-A5、MAGE-A6、MAGE-A7、MAGE-A8、MAGE-A9、MAGE-A10、MAGE-A11、MAGE-A12、MAGE-Xp2(MAGE-B2)、MAGE-Xp3(MAGE-B3)、MAGE-Xp4(MAGE-B4)、MAGE-C1、MAGE-C2、MAGE-C3、MAGE-C4、MAGE-C5)、肿瘤抗原的GAGE家族(例如,GAGE-1、GAGE-2、GAGE-3、GAGE-4、GAGE-5、GAGE-6、GAGE-7、GAGE-8、GAGE-9)、BAGE、RAGE、LAGE-1、NAG、GnT-V、MUM-1、CDK4、酪氨酸酶、p53、MUC家族、HER2/neu、p21ras、RCAS1、甲胎蛋白、E-钙粘蛋白、α-连环蛋白、β-连环蛋白和γ-连环蛋白、p120ctn、gp100Pmel117、PRAME、NY-ESO-1、cdc27、腺瘤性息肉病杆菌蛋白(APC)、胞衬蛋白(fodrin)、连接蛋白37(Connexin37)、Ig-独特型(Ig-idiotype)、p15、gp75、GM2和GD2神经节苷脂、病毒产物如人乳头瘤病毒蛋白、肿瘤抗原的Smad家族、lmp-1、NA、EBV编码核抗原(EBNA)-1、脑糖原磷酸化酶、SSX-1、SSX-2(HOM-MEL-40)、SSX-1、SSX-4、SSX-5、SCP-1CT-7、c-erbB-2、CD19、CD37、CD56、CD70、CD74、CD138、AGS16、MUC1、GPNMB、Ep-CAM、PD-L1和PD-L2。
示例性的CART细胞治疗包括但不限于JCAR014(Juno Therapeutics)、JCAR015(Juno Therapeutics)、JCAR017(Juno Therapeutics)、JCAR018(Juno Therapeutics)、JCAR020(Juno Therapeutics)、JCAR023(Juno Therapeutics)、JCAR024(JunoTherapeutics)、CTL019(Novartis)、KTE-C19(Kite Pharma)、BPX-401(BellicumPharmaceuticals)、BPX-501(Bellicum Pharmaceuticals)、BPX-601(BellicumPharmaceuticals)、bb2121(Bluebird Bio)、CD-19睡美人细胞(Ziopharm Oncology)、UCART19(Cellectis)、UCART123(Cellectis)、UCART38(Cellectis)、UCARTCS1(Cellectis)、OXB-302(Oxford BioMedica,MB-101(Mustang Bio)和Innovative CellularTherapeutics开发的CART细胞。
在多个实施方案中,CAR-T细胞是自体或同种异体的γδT细胞。
在多个实施方案中,本发明的异二聚体蛋白在多个实施方案中能够或可用于涉及掩蔽肿瘤细胞表面上的抑制性配体并用免疫刺激配体取代该免疫抑制配体的方法。因此,在多个实施方案中,本发明的异二聚体蛋白能够或可用于涉及减少或消除抑制性免疫信号和/或增加或激活免疫刺激信号的方法。例如,携带抑制信号(从而逃避免疫应答)的肿瘤细胞可以被结合在T细胞上的阳性信号所替换,然后T细胞可以攻击肿瘤细胞。因此,在多个实施方案中,抑制性免疫信号被本发明的异二聚体蛋白掩蔽并且刺激性免疫信号被激活。通过本发明的异二聚体蛋白的单一构建体方法增强了此类有益特性。例如,信号替换可以几乎同时实现,并且信号替换被定制为在具有临床重要性的部位(例如,肿瘤微环境)处局部进行。
在多个实施方案中,本发明的异二聚体蛋白能够或可用于包括刺激或增强免疫刺激受体/配体对的结合的方法。
在其他实施方案中,本发明的异二聚体蛋白能够或可用于涉及增强、恢复、促进和/或刺激免疫调节的方法。在多个实施方案中,本文所述的异二聚体蛋白恢复、促进和/或刺激针对肿瘤细胞的一种或多种免疫细胞的活性或激活,所述免疫细胞包括但不限于:T细胞、细胞毒性T淋巴细胞、T辅助细胞、自然杀伤(NK)细胞、自然杀伤T(NKT)细胞、抗肿瘤巨噬细胞(例如M1巨噬细胞)、B细胞和树突细胞。在多个实施方案中,本发明的异二聚体蛋白增强、恢复、促进和/或刺激T细胞的活性和/或激活,包括,作为非限制性实例,激活和/或刺激一种或多种T细胞内在信号,包括有利于生存的信号;自分泌或旁分泌生长信号;p38MAPK、ERK、STAT、JAK、AKT或PI3K介导的信号;抗凋亡信号;和/或促进促炎细胞因子产生或T细胞迁移或T细胞肿瘤浸润中的一个或多个的信号和/或对促炎细胞因子产生或T细胞迁移或T细胞肿瘤浸润中的一个或多个来说必需的信号。
在多个实施方案中,本发明的异二聚体蛋白能够或可用于涉及引起进入肿瘤或肿瘤微环境的T细胞(包括但不限于细胞毒性T淋巴细胞、T辅助细胞、自然杀伤T(NKT)细胞)、B细胞、自然杀伤(NK)细胞、自然杀伤T(NKT)细胞、树突细胞、单核细胞和巨噬细胞(例如,M1和M2中的一种或多种)中的一种或多种的增加的方法。在多个实施方案中,本发明的异二聚体蛋白能够或可用于涉及抑制和/或引起减少募集至肿瘤和/或肿瘤微环境(TME)的免疫抑制细胞(例如,骨髓源性抑制细胞(MDSC)、调节性T细胞(Treg)、肿瘤细胞相关嗜中性粒细胞(TAN)、M2巨噬细胞和肿瘤相关巨噬细胞(TAM))的方法。在多个实施方案中,本发明的治疗可以改变肿瘤部位和/或TME中M1与M2巨噬细胞的比率以有利于M1巨噬细胞。
在多个实施方案中,异三聚体蛋白调节γδT细胞的功能。
在多个实施方案中,本发明的异二聚体蛋白能够并且可用于包括抑制和/或减少T细胞失活和/或对肿瘤的免疫耐受的方法,所述方法包括向受试者施用有效量的本文所述的异二聚体蛋白。在多个实施方案中,本发明的异二聚体蛋白能够增加多种细胞因子的血清水平,所述细胞因子包括但不限于IFNγ、IL-2、IL-4、IL-5、IL-6、IL-9、IL-10、IL-13、IL-17A、IL-17F和IL-22中的一种或多种。在多个实施方案中,本发明的异二聚体蛋白能够增强所治疗的受试者血清中的IL-2、IL-4、IL-5、IL-10、IL-13、IL-17A、IL-22或IFNγ。
在多个实施方案中,本发明的异二聚体蛋白抑制、阻断和/或减少抗肿瘤CD8+和/或CD4+T细胞的细胞死亡;或刺激、诱导和/或增加促肿瘤T细胞的细胞死亡。T细胞耗竭(Tcellexhaustion)是T细胞功能障碍的一种状态,其特征是增殖和效应功能逐渐丧失,最终导致克隆缺失。因此,促肿瘤T细胞是指在癌症期间出现的T细胞功能障碍的状态。这种功能障碍的定义是增殖和/或效应功能差、持续表达抑制性受体以及转录状态与功能性效应或记忆T细胞不同。耗竭会阻碍肿瘤的最佳控制。另外,抗肿瘤CD8+和/或CD4+T细胞是指能够引起对肿瘤的免疫应答的T细胞。示例性促肿瘤T细胞包括但不限于Treg、表达一种或多种检查点抑制性受体的CD4+和/或CD8+T细胞、Th2细胞和Th17细胞。检查点抑制性受体是指免疫细胞上表达的受体(例如CTLA-4、B7-H3、B7-H4、TIM-3),其可防止或抑制不受控制的免疫应答。
在多个实施方案中,本发明的异二聚体蛋白能够并且可用于包括增加效应T细胞与调节性T细胞的比率的方法中。示例性效应T细胞包括ICOS
在多个实施方案中,本发明的异二聚体蛋白能够并且可用于包括瞬时刺激效应T细胞不超过约12小时、不超过约24小时、不超过约48小时、不超过约72小时或不超过约96小时或不超过约1周或不超过约2周的方法中。在多个实施方案中,本发明的异二聚体蛋白能够并且可用于包括瞬时耗减或抑制调节性T细胞不超过约12小时、不超过约24小时、不超过约48小时、不超过约72小时或不超过约96小时或不超过约1周或不超过约2周的方法中。在多个实施方案中,效应T细胞的瞬时刺激和/或调节性T细胞的瞬时耗减或抑制基本上发生在患者的血流中或特定的组织/位置中,包括淋巴组织,例如骨髓、淋巴结、脾脏、胸腺、粘膜相关淋巴组织(MALT)、非淋巴组织或肿瘤微环境中。
在多个实施方案中,本发明的异二聚体蛋白提供的优点包括但不限于易于使用和易于生产。这是因为将两种不同的免疫治疗剂组合成单个产品,从而允许进行单个制造方法而不是两个独立的制造方法。此外,施用单个药剂而不是两种单独的药剂使得施用更容易并且患者依从性更高。此外,与例如单克隆抗体(单克隆抗体是含有大量二硫键和翻译后修饰如糖基化的大的多聚体蛋白)相比,本发明的异二聚体蛋白的制造更容易且更具成本效益。
在多个实施方案中,本发明的异二聚体蛋白提供协同治疗效果,因为它允许改善两种免疫治疗剂的位点特异性相互作用。在多个实施方案中,本发明的异二聚体蛋白提供了减少脱位(off-site)和/或全身毒性的潜力。
疾病
在一个方面,本公开提供了治疗癌症的方法,其包括向有需要的受试者施用有效量的本文公开的任何实施方案的药物组合物。在一些实施方案中,癌症是淋巴瘤。在一些实施方案中,癌症是白血病。在一些实施方案中,癌症是霍奇金和非霍奇金淋巴瘤、B细胞淋巴瘤(包括低级/滤泡性非霍奇金淋巴瘤(NHL);小淋巴细胞(SL)NHL;中级/滤泡性NHL;中级弥漫性NHL;高级成免疫细胞NHL;高级成淋巴细胞NHL;高级小非裂解细胞NHL;巨大肿块疾病NHL(bulky diseaseNHL);套细胞淋巴瘤;AIDS相关淋巴瘤;和华氏巨球蛋白血症(Waldenstrom’s Macroglobulinemia);慢性淋巴细胞白血病(CLL);急性成淋巴细胞白血病(ALL);毛细胞白血病;或慢性原粒细胞白血病。在一些实施方案中,癌症是基底细胞癌;胆道癌;膀胱癌;骨癌;脑和中枢神经系统癌症;乳腺癌;腹膜癌;宫颈癌;绒膜癌;结肠和直肠癌;结缔组织癌;消化系统癌;子宫内膜癌;食道癌;眼癌;头颈癌;胃癌(包括胃肠道癌);胶质母细胞瘤;肝癌(hepatic carcinoma);肝细胞瘤(hepatoma);上皮内肿瘤;肾癌;喉癌;白血病;肝脏癌(liver cancer);肺癌(例如,小细胞肺癌、非小细胞肺癌、肺腺癌和肺鳞状细胞癌);黑色素瘤;骨髓瘤;成神经细胞瘤;口腔癌(唇、舌、口和咽);卵巢癌;胰腺癌;前列腺癌;视网膜母细胞瘤;横纹肌肉瘤;直肠癌;呼吸系统癌症;唾液腺癌;肉瘤;皮肤癌;鳞状细胞癌;胃癌;睾丸癌;甲状腺癌;子宫或子宫内膜癌;泌尿系统癌症;外阴癌;淋巴瘤,包括霍奇金和非霍奇金淋巴瘤,以及B细胞淋巴瘤(包括低级/滤泡性非霍奇金淋巴瘤(NHL);小淋巴细胞(SL)NHL;中级/滤泡性NHL;中级弥漫性NHL;高级成免疫细胞NHL;高级成淋巴细胞NHL;高级小非裂解细胞NHL;巨大肿块疾病NHL;套细胞淋巴瘤;AIDS相关淋巴瘤;和华氏巨球蛋白血症;慢性淋巴细胞白血病(CLL);急性成淋巴细胞白血病(ALL);毛细胞白血病;慢性原粒细胞白血病;以及其他癌和肉瘤;和移植后淋巴增殖性疾病(PTLD),以及与母斑细胞病、水肿(例如与脑肿瘤相关的水肿)和梅格斯综合征(Meigs’syndrome)相关的异常血管增殖。在一些实施方案中,癌症是前列腺癌。在一些实施方案中,癌症是上皮来源的癌。在一些实施方案中,已知癌症表达异二聚体蛋白的第二结构域的抗原性靶标。在一些实施方案中,已知癌症含有限制被αβT细胞识别的突变,包括但不限于MHCI、β2微球蛋白、TAP等中的突变。
在一些实施方案中,进一步向受试者施用离体扩增的自体或同种异体γδT细胞。在一些实施方案中,自体或同种异体γδT细胞表达嵌合抗原受体。在一些实施方案中,进一步向受试者施用表达嵌合抗原受体的自体或同种异体T细胞。
在多个实施方案中,本公开涉及癌症和/或肿瘤;例如,治疗或预防癌症和/或肿瘤。如本文别处所描述,癌症的治疗可涉及在各种实施方案中,用本发明的异二聚体蛋白调节免疫系统以有利于免疫刺激而非免疫抑制。
癌症或肿瘤是指细胞不受控制的生长和/或异常增加的细胞存活和/或细胞凋亡的抑制,其干扰身体器官和系统的正常功能。包括良性和恶性癌症、息肉、增生,以及休眠肿瘤或微转移。此外,包括具有不受免疫系统阻碍的异常增殖的细胞。癌症可以是原发性癌症或转移性癌症。原发性癌症可以是在临床可检测的起源部位处的癌细胞区域,并且可以是原发性肿瘤。相反,转移性癌症可以是疾病从一个器官或部分扩散到另一个非相邻器官或部分。转移性癌症可以由获得在局部区域穿透和浸润周围正常组织从而形成新的肿瘤的能力的癌细胞引起,这可以是局部转移。癌症也可以由获得穿透淋巴管和/或血管壁的能力的癌细胞引起,此后癌细胞能够通过血流循环(因此成为循环肿瘤细胞)到体内的其他部位和组织。癌症可以由如淋巴或血原性扩散等过程引起。癌症也可由在另一个部位静止、重新穿透血管或壁、继续增殖并最终形成另一个临床可检测肿瘤的肿瘤细胞引起。癌症可能是这种新肿瘤,也可能是转移性(或继发性)肿瘤。
癌症可由已经转移的肿瘤细胞引起,其可以是继发性或转移性肿瘤。肿瘤的细胞可与原始肿瘤中的细胞相似。例如,如果乳腺癌或结肠癌转移到肝脏,继发性肿瘤虽然存在于肝脏,但由异常的乳腺或结肠细胞组成,而不是由异常的肝细胞组成。因此,肝脏中的肿瘤可以是转移性乳腺癌或转移性结肠癌,而不是肝癌。
癌症可以起源于任何组织。癌症可能源自黑色素瘤、结肠、乳腺或前列腺,因此可能分由最初分别是皮肤、结肠、乳腺或前列腺的细胞组成。癌症也可以是血液恶性肿瘤,其可以是白血病或淋巴瘤。癌症可能会侵入例如肝脏、肺、膀胱或肠道的组织。
本公开的代表性癌症和/或肿瘤包括但不限于基底细胞癌、胆道癌;膀胱癌;骨癌;脑和中枢神经系统癌症;乳腺癌;腹膜癌;宫颈癌;绒膜癌;结肠和直肠癌;结缔组织癌;消化系统癌症;子宫内膜癌;食道癌;眼癌;头颈癌;胃癌(包括胃肠道癌);胶质母细胞瘤;肝癌;肝细胞瘤;上皮内肿瘤;肾癌;喉癌;白血病;肝脏癌;肺癌(例如,小细胞肺癌、非小细胞肺癌、肺腺癌和肺鳞状细胞癌);黑色素瘤;骨髓瘤;成神经细胞瘤;口腔癌(唇、舌、口和咽);卵巢癌;胰腺癌;前列腺癌;视网膜母细胞瘤;横纹肌肉瘤;直肠癌;呼吸系统癌症;唾液腺癌;肉瘤;皮肤癌;鳞状细胞癌;胃癌;睾丸癌;甲状腺癌;子宫或子宫内膜癌;泌尿系统癌症;外阴癌;淋巴瘤,包括霍奇金和非霍奇金淋巴瘤,以及B细胞淋巴瘤(包括低级/滤泡性非霍奇金淋巴瘤(NHL);小淋巴细胞(SL)NHL;中级/滤泡性NHL;中级弥漫性NHL;高级成免疫细胞NHL;高级成淋巴细胞NHL;高级小非裂解细胞NHL;巨大肿块疾病NHL;套细胞淋巴瘤;AIDS相关淋巴瘤;和华氏巨球蛋白血症;慢性淋巴细胞白血病(CLL);急性成淋巴细胞白血病(ALL);毛细胞白血病;慢性原粒细胞白血病;以及其他癌和肉瘤;和移植后淋巴增殖性疾病(PTLD),以及与母斑细胞病(phakomatoses)、水肿(例如与脑肿瘤相关的水肿)和梅格斯综合征相关的异常血管增殖。
在一些实施方案中,癌症是上皮来源的癌。
在一些实施方案中,异二聚体蛋白用于治疗患有难治性(refractory)癌症的受试者。在一些实施方案中,异二聚体蛋白用于治疗对一种或多种免疫调节剂难治的受试者。例如,在一些实施方案中,异二聚体蛋白用于治疗在治疗12周左右后对治疗没有反应或甚至进展的受试者。例如,在一些实施方案中,受试者对PD-1和/或PD-L1和/或PD-L2药剂难治,包括例如纳武单抗(nivolumab)(ONO-4538/BMS-936558、MDX1106、OPDIVO、BRISTOLMYERSSQUIBB)、派姆单抗(pembrolizumab)(KEYTRUDA、MERCK)、匹地利珠单抗(pidilizumab)(CT-011、CURETECH)、MK-3475(MERCK)、BMS936559(BRISTOLMYERSSQUIBB)、依鲁替尼(Ibrutinib)(PHARMACYCLICS/ABBVIE)、阿特朱单抗(atezolizumab)(TECENTRIQ、GENENTECH)和/或MPDL328OA(ROCHE)难治性患者。例如,在一些实施方案中,受试者对抗CTLA-4药剂难治,例如伊匹单抗(ipilimumab)(YERVOY)难治性患者(例如,黑色素瘤患者)。因此,在各种实施方案中,本公开提供拯救对各种治疗、包括一种或多种免疫调节剂的单一疗法无反应的患者的癌症治疗方法。
在各种实施方案中,本公开提供了靶向肿瘤微环境内的细胞或组织的异二聚体蛋白。在一些实施方案中,所述肿瘤微环境内的细胞或组织表达异二聚体蛋白的一种或多种靶标或结合配偶体。肿瘤微环境是指细胞环境,包括肿瘤所在的细胞、分泌蛋白、生理小分子和血管。在一些实施方案中,肿瘤微环境内的细胞或组织是以下中的一种或多种:肿瘤血管;肿瘤浸润淋巴细胞;成纤维细胞网状细胞;内皮祖细胞(EPC);癌症相关成纤维细胞;周细胞;其他基质细胞;胞外基质(ECM)的成分;树突状细胞;抗原呈递细胞;T细胞;调节性T细胞;巨噬细胞;中性粒细胞;和位于肿瘤附近的其他免疫细胞。在各种实施方案中,本发明的异二聚体蛋白靶向癌细胞。在一些实施方案中,癌细胞表达异二聚体蛋白的一种或多种靶标或结合配偶体。
在各种实施方案中,本发明的异二聚体蛋白可以靶向表达如本文所描述的任何受体的细胞(例如,癌细胞或免疫细胞)。例如,本发明的异二聚体蛋白可以靶向表达本文所描述的细胞因子、生长因子和/或激素的任何受体的细胞。
在一些实施方案中,本发明的方法为对另外的药剂难治的患者提供异二聚体蛋白的治疗,这类“另外的药剂”在本文别处描述,包括但不限于本文所描述的各种化疗剂。
在一些方面,本发明的嵌合剂用于激活T细胞的方法,例如通过具有免疫刺激信号的胞外结构域或具有免疫刺激信号的抗体结合结构域(例如CDR3、Fab、scFv结构域等)。
治疗方法和患者选择
在一个方面,本公开涉及一种用于鉴定癌症治疗物的方法,所述方法包括:(a)获得生物样品,所述样品包含一种或多种γ/δT细胞;(b)评估样品中一种或多种γ/δT细胞受体(TCR)链的存在、不存在或水平;(c)选择具有在γ/δTCR处发出信号的能力的癌症治疗物,所述癌症治疗物包含一个或多个嗜乳脂蛋白或其片段。在多个实施方案中,评估包括测量选自Vγ2、Vγ3、Vγ4、Vγ5、Vγ8、Vγ9、Vγ11、Vδ1、Vδ2、Vδ3、Vδ4、Vδ5、Vδ6、Vδ7和Vδ8的一种或多种γ/δT细胞受体(TCR)链的存在、不存在或水平。
在一个方面,本发明涉及一种选择癌症治疗的患者的方法,所述方法包括:(a)获得生物样品,所述样品包含一种或多种γ/δT细胞;(b)评估样品中一种或多种γ/δT细胞受体(TCR)链的存在、不存在或水平;(c)选择具有在γ/δTCR处发出信号的能力的癌症治疗物,所述癌症治疗物包含一个或多个嗜乳脂蛋白或其片段。在多个实施方案中,评估包括测量选自Vγ2、Vγ3、Vγ4、Vγ5、Vγ8、Vγ9、Vγ11、Vδ1、Vδ2、Vδ3、Vδ4、Vδ5、Vδ6、Vδ7和Vδ8的一种或多种γ/δT细胞受体(TCR)链的存在、不存在或水平。
在一个方面,本公开涉及一种制备用于治疗癌症患者的癌症的药剂的方法,包括:(a)获得治疗癌症的药剂,所述获得包括:(i)评估来自癌症患者的生物样品中一种或多种γ/δT细胞受体(TCR)链的存在、不存在或水平;和(ii)选择具有在一种或多种γ/δT细胞受体(TCR)链处发出信号的能力的癌症治疗物,所述癌症治疗物包含一个或多个嗜乳脂蛋白或其片段;(b)配制经鉴定的药剂,用于施用给癌症患者。在多个实施方案中,评估包括测量选自Vγ2、Vγ3、Vγ4、Vγ5、Vγ8、Vγ9、Vγ11、Vδ1、Vδ2、Vδ3、Vδ4、Vδ5、Vδ6、Vδ7和Vδ8的一种或多种γ/δT细胞受体(TCR)链的存在、不存在或水平。
在一个方面,本公开涉及一种鉴定针对肿瘤的癌症治疗的方法,所方法包括:(a)获得生物样品,所述样品包含一种或多种γ/δT细胞;(b)评估样品中一种或多种嗜乳脂蛋白的存在、不存在或水平;和(c)选择具有在γ/δTCR处发出信号的能力的癌症治疗物,所述癌症治疗物包含一个或多个嗜乳脂蛋白或其片段。在多个实施方案中,所述评估包括测量选自BTN1A1、BTN2A1、BTN2A2、BTN2A3、BTN3A1、BTN3A2、BTN3A3、BTNL2、BTNL3、BTNL8、BTNL9、BTNL10和SKINTL的一种或多种嗜乳脂蛋白的存在、不存在或水平。在多个实施方案中,所述评估包括测量选自人BTN1A1、人BTN2A1、人BTN2A2、人BTN2A3、人BTN3A1、人BTN3A2、人BTN3A3、人BTNL2、人BTNL3、人BTNL8、人BTNL9、人BTNL10和人SKINTL的一种或多种嗜乳脂蛋白的存在、不存在或水平。
在一个方面,本发明涉及一种选择癌症治疗的患者的方法,所述方法包括:(a)获得生物样品,所述样品包含一种或多种γ/δT细胞;(b)评估样品中一种或多种嗜乳脂蛋白的存在、不存在或水平;和(c)选择具有在γ/δTCR处发出信号的能力的癌症治疗物,所述癌症治疗物包含一个或多个嗜乳脂蛋白或其片段。在多个实施方案中,所述评估包括测量选自BTN1A1、BTN2A1、BTN2A2、BTN2A3、BTN3A1、BTN3A2、BTN3A3、BTNL2、BTNL3、BTNL8、BTNL9、BTNL10和SKINTL的一种或多种嗜乳脂蛋白的存在、不存在或水平。在多个实施方案中,所述评估包括测量选自人BTN1A1、人BTN2A1、人BTN2A2、人BTN2A3、人BTN3A1、人BTN3A2、人BTN3A3、人BTNL2、人BTNL3、人BTNL8、人BTNL9、人BTNL10和人SKINTL的一种或多种嗜乳脂蛋白的存在、不存在或水平。
在一个方面,本公开涉及一种制备用于治疗癌症患者的癌症的药剂的方法,包括:(a)获得治疗癌症的药剂,所述获得包括:(i)评估来自癌症患者的生物样品中一种或多种嗜乳脂蛋白的存在、不存在或水平;和(ii)选择具有在γ/δTCR处发出信号的能力的癌症治疗物,所述癌症治疗物包含一个或多个嗜乳脂蛋白或其片段;(b)配制所鉴定的药剂,用于施用于癌症患者。在多个实施方案中,所述评估包括测量选自Vγ2、Vγ3、Vγ4、Vγ5、Vγ8、Vγ9、Vγ11、Vδ1、Vδ2、Vδ3、Vδ4、Vδ5、Vδ6、Vδ7和Vδ8的一种或多种γ/δT细胞受体(TCR)链的存在、不存在或水平。
在本文公开的任何实施方案中,生物样品是组织样品。在一些实施方案中,组织样品选自新鲜组织样品、冷冻肿瘤组织标本、培养细胞、循环肿瘤细胞和福尔马林固定的石蜡包埋的肿瘤组织标本。在多个实施方案中,组织样品是活检样品。在多个实施方案中,活检样品选自内窥镜活检、骨髓活检、内窥镜活检(例如膀胱镜检查、支气管镜检查和结肠镜检查)、针吸活检(例如细针抽吸、空心针活检、真空辅助活检)、X射线辅助活检、计算机断层扫描(CT)辅助活检、磁共振成像(MRI)辅助活检和超声辅助活检)、皮肤活检(例如削切活检、穿刺活检和切取活检)和手术活检。在多个实施方案中,组织样品选自骨、骨髓、肺、脑、肝、肾上腺、结肠、肠、食道、胰腺、膀胱、乳房、淋巴结和皮肤。
在本文公开的任何实施方案中,生物样品包含体液,体液选自血液、血浆、血清、泪腺液体(lacrimalfluid)、泪水(tear)、骨髓、血液、血细胞、腹水、组织或细针活检样品、含细胞体液、游离核酸(free floating nucleic acid)、痰液、唾液、尿液、脑脊液、腹膜液、胸水、粪便、淋巴液、妇科液、皮肤拭子、阴道拭子、口腔拭子、鼻拭子、冲洗液或灌洗液如导管灌洗液或支气管肺泡灌洗液、抽吸物、刮取物、骨髓标本、组织活检标本、手术标本、粪便、其他体液、分泌物和/或排泄物、和/或来自其中的细胞。在多个实施方案中,生物样品通过选自刮擦、拭子和活检的技术获得。在多个实施方案中,生物样品通过使用刷子、(棉)拭子、抹刀、漂洗/洗涤液、穿刺活检装置、用针穿刺腔或手术器械来获得。
在本文公开的任何实施方案中,生物样品是肿瘤样品。在多个实施方案中,肿瘤是转移性的。在多个实施方案中,肿瘤已转移至组织或器官。在多个实施方案中,组织或器官选自骨、骨髓、肺、脑、肝、肾上腺、结肠、肠、食道、胰腺、膀胱、乳房、淋巴结和皮肤。在多个实施方案中,肿瘤选自霍奇金淋巴瘤和非霍奇金淋巴瘤、B细胞淋巴瘤(包括低级/滤泡性非霍奇金淋巴瘤(NHL);小淋巴细胞(SL)NHL;中级/滤泡性NHL;中级弥漫性NHL;高级成免疫细胞NHL;高级成淋巴细胞NHL;高级小非裂解细胞NHL;巨大肿块疾病NHL;套细胞淋巴瘤;AIDS相关淋巴瘤;和华氏巨球蛋白血症;慢性淋巴细胞白血病;急性成淋巴细胞白血病(ALL);毛细胞白血病;或慢性原粒细胞白血病。在一些实施方案中,所述癌症是基底细胞癌、胆道癌、膀胱癌、骨癌、脑和中枢神经系统癌症、乳腺癌;腹膜癌;宫颈癌;绒毛膜癌;结肠和直肠癌;结缔组织癌症;消化系统癌症;子宫内膜癌;食道癌;眼癌;头颈癌;胃癌(包括胃肠癌);胶质母细胞瘤;肝癌;肝细胞癌;上皮内肿瘤;肾癌;喉癌;白血病;肝脏癌;肺癌(例如小细胞肺癌、非小细胞肺癌、肺腺癌和肺鳞状细胞癌);黑色素瘤;骨髓瘤;成神经细胞瘤;口腔癌(唇、舌、口和咽);卵巢癌;胰腺癌;前列腺癌;视网膜母细胞瘤;横纹肌肉瘤;直肠癌;呼吸系统癌症;唾液腺癌;肉瘤;皮肤癌;鳞状细胞癌;胃癌;睾丸癌;甲状腺癌;子宫癌或子宫内膜癌;泌尿系统癌症;外阴癌;淋巴瘤,包括霍奇金淋巴瘤和非霍奇金淋巴瘤,以及B细胞淋巴瘤(包括低级/滤泡性非霍奇金淋巴瘤(NHL);小淋巴细胞(SL)NHL;中级/滤泡性NHL;中级弥漫性NHL;高级成免疫细胞NHL;高级成淋巴细胞NHL;高级小非裂解细胞NHL;巨大肿块疾病NHL;套细胞淋巴瘤;AIDS相关淋巴瘤;和华氏巨球蛋白血症;慢性淋巴细胞白血病;急性成淋巴细胞白血病(ALL);毛细胞白血病;慢性原粒细胞白血病;以及其他癌症和肉瘤;和移植后淋巴增殖性疾病(PTLD),以及与母斑细胞病、水肿(例如与脑肿瘤相关)、梅格斯综合征癌相关的异常血管增殖;肾癌;结直肠癌;和肾上腺癌。
在本文公开的任何实施方案中,所述评估通过DNA测序、RNA测序、免疫组织化学染色、蛋白质印迹、细胞内蛋白质印迹、免疫荧光染色、ELISA和荧光激活细胞分选(FACS)或其组合来进行。
在多个实施方案中,所述评估通过使样品与特异性结合选自Vγ2、Vγ3、Vγ4、Vγ5、Vγ8、Vγ9、Vγ11、Vδ1、Vδ2、Vδ3、Vδ4、Vδ5、Vδ6、Vδ7和Vδ8的一种或多种γ/δT细胞受体(TCR)链的药剂接触来进行。在多个实施方案中,特异性结合一种或多种TCR的药剂是抗体或其片段。在多个实施方案中,抗体是重组抗体、单克隆抗体、多克隆抗体或其片段。在多个实施方案中,所述评估通过使样品与特异性结合一种或多种γ/δT细胞受体(TCR)链的抗体或其片段接触,并使用免疫组织化学染色、蛋白质印迹、细胞蛋白质印迹、免疫荧光染色、ELISA和荧光激活细胞分选(FACS)或其组合检测一种或多种γ/δT细胞受体(TCR)链来进行。
在本文公开的任何实施方案中,所述评估通过使样品与特异性结合选自BTN1A1、BTN2A1、BTN2A2、BTN2A3、BTN3A1、BTN3A2、BTN3A3、BTNL2、BTNL3、BTNL8、BTNL9、BTNL10和SKINTL的一种或多种嗜乳脂蛋白的药剂接触来进行。在多个实施方案中,所述评估通过使样品与特异性结合选自人BTN1A1、人BTN2A1、人BTN2A2、人BTN2A3、人BTN3A1、人BTN3A2、人BTN3A3、人BTNL2、人BTNL3、人BTNL8、人BTNL9、人BTNL10和人SKINTL的一种或多种嗜乳脂蛋白的药剂接触来进行。在多个实施方案中,特异性结合一种或多种嗜乳脂蛋白的药剂是抗体或其片段。在多个实施方案中,抗体是重组抗体、单克隆抗体、多克隆抗体或其片段。在多个实施方案中,所述评估通过使样品与特异性结合一种或多种嗜乳脂蛋白的抗体或其片段接触并使用免疫组织化学染色、蛋白质印迹、细胞内蛋白质印迹、免疫荧光染色、ELISA和荧光激活细胞分选(FACS)或其组合检测一种或多种嗜乳脂蛋白来进行。
在本文公开的任何实施方案中,所述评估通过使样品与特异性结合选自Vγ2、Vγ3、Vγ4、Vγ5、Vγ8、Vγ9、Vγ11、Vδ1、Vδ2、Vδ3、Vδ4、Vδ5、Vδ6、Vδ7和Vδ8的一种或多种γ/δT细胞受体(TCR)链的药剂接触来进行。在多个实施方案中,特异性结合一种或多种TCR的药剂是抗体或其片段。在多个实施方案中,抗体是重组抗体、单克隆抗体、多克隆抗体或其片段。
在本文公开的任何实施方案中,一种或多种嗜乳脂蛋白的水平和/或活性通过使样品与特异性结合一种或多种所述核酸的药剂接触来测量。在多个实施方案中,特异性结合一种或多种所述核酸的药剂是核酸引物或探针。
在本文公开的任何实施方案中,一种或多种TCR的水平和/或活性通过使样品与特异性结合一种或多种所述核酸的药剂接触来测量。在多个实施方案中,特异性结合一种或多种核酸的药剂是核酸引物或探针。
在多个实施方案中,当与健康组织或来自健康个体的样品相比,在肿瘤中检测到TCRVγ9δ2的存在或更高水平时,选择包含人BTN2A1、BTN3A1、BTN2A2和/或BTN2A3嗜乳脂蛋白或其片段的癌症治疗物;和/或与健康组织或来自健康个体的样品相比,在肿瘤中检测到TCRVδ4的存在或更高水平时,选择包含人BTNL3嗜乳脂蛋白或其片段的癌症治疗物。
在多个实施方案中,当与健康组织或来自健康个体的样品相比,在肿瘤中检测到人BTN1A1的存在或更高水平时,选择包含人BTN1A1嗜乳脂蛋白或其片段的癌症治疗物;与健康组织或来自健康个体的样品相比,在肿瘤中检测到人BTNL2的存在或更高水平时,选择包含人BTNL2嗜乳脂蛋白或其片段的癌症治疗物;与健康组织或来自健康个体的样品相比,在肿瘤中检测到人BTN2A1的存在或更高水平时,选择包含人BTN2A1嗜乳脂蛋白或其片段的癌症治疗物;与健康组织或来自健康个体的样品相比,在肿瘤中检测到人BTN2A2的存在或更高水平时,选择包含人BTN2A2嗜乳脂蛋白蛋白或其片段的癌症治疗物;与健康组织或来自健康个体的样品相比,在肿瘤中检测到人BTN2A3的存在或更高水平时,选择包含人BTN2A3嗜乳脂蛋白或其片段的癌症治疗物;与健康组织或来自健康个体的样品相比,在肿瘤中检测到人BTN2A3的存在或更高水平时,选择包含人BTN2A3嗜乳脂蛋白或其片段的癌症治疗物;与健康组织或来自健康个体的样品相比,在肿瘤中检测到人BTN3A1的存在或更高水平时,选择包含人BTN3A1嗜乳脂蛋白或其片段的癌症治疗物;与健康组织或来自健康个体的样品相比,在肿瘤中检测到人BTN3A2的存在或更高水平时,选择包含人BTN3A2嗜乳脂蛋白或其片段的癌症治疗物;与健康组织或来自健康个体的样品相比,在肿瘤中检测到人BTN3A3的存在或更高水平时,选择包含人BTN3A3嗜乳脂蛋白或其片段的癌症治疗物;与健康组织或来自健康个体的样品相比,在肿瘤中检测到人BTNL8的存在或更高水平时,选择包含人BTNL8嗜乳脂蛋白或其片段的癌症治疗物;与健康组织或来自健康个体的样品相比,在肿瘤中检测到人BTNL9的存在或更高水平时,选择包含人BTNL9嗜乳脂蛋白或其片段的癌症治疗物;与健康组织或来自健康个体的样品相比,在肿瘤中检测到人BTNL10的存在或更高水平时,选择包含人BTNL10嗜乳脂蛋白或其片段的癌症治疗物;和/或与健康组织或来自健康个体的样品相比,在肿瘤中检测到人SKINTL的存在或更高水平时,选择包含人SKINTL嗜乳脂蛋白或其片段的癌症治疗物。
在多个实施方案中,与另一组织相比,当在一个组织中观察到嗜乳脂蛋白家族蛋白的存在或更高水平时,选择包含嗜乳脂蛋白家族蛋白或其片段的癌症治疗用于治疗在该组织中转移的肿瘤。
在多个实施方案中,当与正常组织或另一种类型的癌症相比,在一种类型的癌症(例如乳腺癌、结直肠癌、胰腺癌、前列腺癌等)中观察到嗜乳脂蛋白家族蛋白的存在或更高水平时,选择包含嗜乳脂蛋白家族蛋白或其片段的治疗来治疗该癌症类型。
在多个实施方案中,与另一组织相比,当在一个组织中观察到特定γδTCR的存在或更高水平时,选择包含与该特定γδTCR结合的一个或多个嗜乳脂蛋白家族蛋白或其片段的癌症治疗物来治疗在该组织中转移的肿瘤。
在多个实施方案中,与正常组织或另一种类型的癌症相比,在一种类型的癌症(例如乳腺癌、结直肠癌、胰腺癌、前列腺癌等)中观察到特定γδTCR的存在或更高水平时,选择包含与该特定γδTCR结合的一个或多个嗜乳脂蛋白家族蛋白或其片段的癌症治疗物来治疗该癌症类型。
在本文公开的任何实施方案中,癌症治疗物包含异二聚体蛋白,所述异二聚体蛋白包含:(a)第一结构域,其包含一个或多个嗜乳脂蛋白家族蛋白或其片段;(b)第二结构域,其包含靶向结构域,所述靶向结构域选自(i)抗体、抗体样分子或其抗原结合片段,和(ii)胞外结构域;和(c)接头,其连接第一结构域和第二结构域。在多个实施方案中,第一结构域包含两个相同的嗜乳脂蛋白家族蛋白。在多个实施方案中,第一结构域包含两个不同的嗜乳脂蛋白家族蛋白。在多个实施方案中,嗜乳脂蛋白家族蛋白或其片段包含Ig样V型结构域。在多个实施方案中,嗜乳脂蛋白家族蛋白或其片段衍生自天然全长蛋白。在多个实施方案中,第一结构域包含嗜乳脂蛋白家族蛋白的一个或多个片段,其中所述片段能够结合γδT细胞受体并且任选地是胞外结构域。
在本文公开的任何实施方案中,所述癌症治疗物包含异二聚体蛋白,所述异二聚体蛋白包含α链和β链,其中α链和β链各自独立地包含(a)第一结构域,其包含嗜乳脂蛋白家族蛋白或其片段;(b)第二结构域,其包含靶向结构域,所述靶向结构域选自(i)抗体、抗体样分子或其抗原结合片段,和(ii)胞外结构域;和(c)接头,其连接第一结构域和第二结构域。在多个实施方案中,第一结构域包含两个相同的嗜乳脂蛋白家族蛋白。在多个实施方案中,第一结构域包含两个不同的嗜乳脂蛋白家族蛋白。在多个实施方案中,嗜乳脂蛋白家族蛋白或其片段包含Ig样V型结构域。在多个实施方案中,嗜乳脂蛋白家族蛋白或其片段衍生自天然全长蛋白。在多个实施方案中,第一结构域包含嗜乳脂蛋白家族蛋白的一个或多个片段,其中所述片段能够结合γδT细胞受体并且任选地是胞外结构域。
在多个实施方案中,第一结构域包含具有以下氨基酸序列的多肽:(a)具有选自氨基酸序列SEQ ID NO:24至45的氨基酸序列的多肽或其片段;(b)具有选自氨基酸序列SEQID NO:24至45的氨基酸序列的多肽或其片段。在多个实施方案中,接头包含具有选自氨基酸序列SEQ ID NO:1-14的氨基酸序列的多肽。在多个实施方案中,接头包含具有选自氨基酸序列SEQ ID NO:15-22的氨基酸序列的多肽。
在多个实施方案中,靶向结构域是抗体或其抗原结合片段。在多个实施方案中,靶向结构域是抗体样分子或其抗原结合片段。在多个实施方案中,抗体样分子选自单链抗体(scFv)、单域抗体、重组仅重链抗体(VHH)、鲨鱼仅重链抗体(VNAR)、微蛋白(半胱氨酸结蛋白,打结素)、DARPin、Tetranectin、Affibody、Transbody、Anticalin、AdNectin、Affilin、Affimer、Microbody、适体、alterase、塑料抗体、phylomer、stradobody、maxibody、evibody、fynomer、犰狳重复蛋白、Kunitz结构域、avimer、atrimer、probody、immunobody、triomab、troybody、pepbody、vaccibody、UniBody、DuoBody、Fv、Fab、Fab'和F(ab')2。在多个实施方案中,抗体样分子是scFv。
在多个实施方案中,靶向结构域是胞外结构域。
在多个实施方案中,靶向结构域能够结合癌细胞表面上的抗原。在多个实施方案中,靶向结构域特异性结合选自以下的蛋白:CLEC12A、CD307、gpA33、间皮素、CDH17、CDH3/P-钙粘蛋白、CEACAM5/CEA、EPHA2、NY-eso-1、GP100、MAGE-A1、MAGE-A4、MSLN、CLDN18.2、Trop-2、ROR1、CD123、CD33、CD20、GPRC5D、GD2、CD276/B7-H3、DLL3、PSMA、CD19、cMet、HER2、A33、TAG72、5T4、CA9、CD70、MUC1、NKG2D、CD133、EpCam、MUC17、EGFRvIII、IL13R、CPC3、GPC3、FAP、BCMA、CD171、SSTR2、FOLR1、MUC16、CD274/PDL1、CD44、KDR/VEGFR2、PDCD1/PD1、TEM1/CD248、LeY、CD133、CELEC12A/CLL1、FLT3、IL1RAP、CD22、CD23、CD30/TNFRSF8、FCRH5、SLAMF7/CS1、CD38、CD4、PRAME、EGFR、PSCA、STEAP1、CD174/FUT3/LeY、L1CAM/CD171、CD22、CD5、LGR5、LGR5、CLL-1、CDH18、EPHA3、NY-eso-2、MAGE-A10、MAGE-A3、MAGE-A7、HER3和GD3。在多个实施方案中,靶向结构域包含LAG-3、PD-1、TIGIT、CD19或PSMA的胞外结构域的部分。在多个实施方案中,靶向结构域特异性结合CD19。在多个实施方案中,靶向结构域特异性结合PSMA。在多个实施方案中,靶向结构域特异性结合CD33。在多个实施方案中,靶向结构域特异性结合CD20。在多个实施方案中,靶向结构域特异性结合DLL3。在多个实施方案中,靶向结构域特异性结合CLL-1。
在多个实施方案中,接头包含(a)第一电荷极化核心结构域,其与嗜乳脂蛋白家族蛋白连接,任选在羧基末端连接,和(b)第二电荷极化核心结构域,其与嗜乳脂蛋白家族蛋白连接,任选在羧基末端连接。在多个实施方案中,接头通过第一和第二电荷极化核心结构域上带正电荷的氨基酸残基和带负电荷的氨基酸残基之间的静电相互作用形成异二聚体。在多个实施方案中,第一和/或第二电荷极化核心结构域包含多肽接头,任选地选自柔性氨基酸序列、IgG铰链区或抗体序列。在多个实施方案中,接头是合成接头,任选地是PEG。在多个实施方案中,接头包含衍生自IgG1,任选地衍生自人IgG1的铰链-CH2-CH3Fc结构域。在多个实施方案中,接头包含衍生自IgG4,任选地衍生自人IgG4的铰链-CH2-CH3Fc结构域。
在多个实施方案中,第一和/或第二电荷极化核心结构域还包含在所述电荷极化核心结构域的氨基和/或羧基末端具有带正电荷和/或带负电荷的氨基酸残基的肽。
在多个实施方案中,带正电荷的氨基酸残基包括选自His、Lys和Arg的一个或多个氨基酸。在多个实施方案中,带正电荷的氨基酸残基存在于在第一和/或第二电荷极化核心结构域中包含带正电荷的氨基酸残基的肽中。在多个实施方案中,包含带正电荷的氨基酸残基的所述肽包含选自以下的序列:YnXnYnXnYn(其中X是带正电荷的氨基酸如精氨酸、组氨酸或赖氨酸,Y是间隔氨基酸如丝氨酸或甘氨酸,并且其中每个n独立地是0至4的整数)(SEQ ID NO:1)、YYnXXnYYnXXnYYn(其中X是带正电荷的氨基酸如精氨酸、组氨酸或赖氨酸,Y是间隔氨基酸如丝氨酸或甘氨酸,并且其中每个n独立地是0至4的整数)(SEQ ID NO:3)和YnXnCYnXnYn(其中X是带正电荷的氨基酸如精氨酸、组氨酸或赖氨酸,Y是间隔氨基酸如丝氨酸或甘氨酸,并且其中每个n独立地是0至4的整数)(SEQ ID NO:5)。在多个实施方案中,其中包含带正电荷的氨基酸残基的所述肽包含序列RKGGKR(SEQ ID NO:11)或GSGSRKGGKRGS(SEQ ID NO:12)。
在多个实施方案中,带负电荷的氨基酸残基可包括选自Asp和Glu的一个或多个氨基酸。在多个实施方案中,带负电荷的氨基酸残基存在于在第一和/或第二电荷极化核心结构域中包含带负电荷的氨基酸残基的肽中。在多个实施方案中,包含带负电荷的氨基酸残基的所述肽包含选自以下的序列:YnZnYnZnYn(其中Z是带负电荷的氨基酸如天冬氨酸或谷氨酸,Y是间隔氨基酸如丝氨酸或甘氨酸,并且其中每个n独立地为0至4的整数)(SEQ IDNO:2)、YYnZZnYYnZZnYYn(其中Z是带负电荷的氨基酸如天冬氨酸或谷氨酸,Y是间隔氨基酸如丝氨酸或甘氨酸,并且其中每个n独立地是0至4的整数)(SEQ ID NO:4)和YnZnCYnZnYn(其中Z是带负电荷的氨基酸如天冬氨酸或谷氨酸,Y是间隔氨基酸如丝氨酸或甘氨酸,并且其中每个n独立地是0至4的整数)(SEQ ID NO:6)。在多个实施方案中,包含带负电荷的氨基酸残基的肽包含序列DEGGED(SEQ ID NO:13)或GSGSDEGGEDGS(SEQ ID NO:14)。
在多个实施方案中,第一结构域和/或异二聚体蛋白调节或能够调节γδ(gammadelta)T细胞。在多个实施方案中,γδT细胞选自表达Vγ4、Vγ9δ2或Vγ7δ4的细胞。在多个实施方案中,γδT细胞的调节是γδT细胞的激活。在多个实施方案中,异二聚体蛋白能够在γδT细胞和肿瘤细胞之间形成突触和/或异二聚体蛋白能够同时激活γδT细胞并将其靶向肿瘤细胞。
组合疗法和缀合
在一些实施方案中,本发明提供异二聚体蛋白和方法,其还包括向受试者施用另外的药剂。在一些实施方案中,本发明涉及共同施用和/或共同配制。可以共同配制和/或共同施用本文所描述的任何组合物。
在一些实施方案中,本文所描述的任何异二聚体蛋白在与另一种药剂共同施用时协同作用并且施用剂量低于在此类剂用作单一疗法时通常采用的剂量。在各种实施方案中,本文提及的任何药剂可与本文所描述的任何异二聚体蛋白组合使用。
在各种实施方案中,本文公开的任何异二聚体蛋白可以与本文公开的另一种异二聚体蛋白共同施用。不希望受理论束缚,认为涉及施用一种或多种诱导先天免疫应答的异二聚体蛋白和一种或多种诱导适应性免疫应答的异二聚体蛋白的组合方案可提供协同效应(例如,协同抗肿瘤效应)。
在各种实施方案中,在本公开中可以利用诱导先天免疫应答的任何异二聚体蛋白。在各种实施方案中,在本公开中可以利用诱导适应性免疫应答的任何异二聚体蛋白。
在一些实施方案中,包括但不限于癌症应用,本公开涉及作为另外的药剂的化疗剂。化疗剂的实例包括但不限于烷化剂,例如噻替哌(thiotepa)和CYTOXAN环磷酰胺(cyclosphosphamide);烷基磺酸盐类,例如白消安(busulfan)、英丙舒凡(improsulfan)、哌泊舒凡(piposulfan);氮丙啶类,例如苯佐多巴(benzodopa)、卡波醌(carboquone)、美托多巴(meturedopa)和乌多巴(uredopa);乙烯亚胺和甲基三聚氰胺,包括六甲三聚氰胺、三亚乙基三聚氰胺、三亚乙基磷酰胺、三亚乙基硫代磷酰胺和三羟甲基三聚氰胺;己酸配质(acetogenins)(例如,布拉它辛(bullatacin)和布拉它辛酮(bullatacinone));喜树碱(camptothecin)(包括合成类似物拓扑替康(topotecan));苔藓抑素(bryostatin);卡莉他汀类药物(callystatin);CC-1065(包括其阿多来新(adozelesin)、卡折来新(carzelesin)和比折来新(bizelesin)合成类似物);隐藻素(cryptophycins)(例如,隐藻素1和隐藻素8);尾海兔素(dolastatin);多卡霉素(duocarmycin)(包括合成类似物KW-2189和CB1-TM1);软珊瑚醇(eleutherobin);水鬼蕉碱(pancratistatin);匍枝珊瑚醇(sarcodictyin);海绵抑制素(spongistatin);氮芥类(nitrogenmustards),例如苯丁酸氮芥(chlorambucil)、萘氮芥(chlornaphazine)、氯磷酰胺(cholophosphamide)、雌莫司汀(estramustine)、异环磷酰胺(ifosfamide)、氮芥(mechlorethamine)、盐酸氧氮芥(mechlorethamineoxidehydrochloride)、美法仑(melphalan)、新恩比兴(novembichin)、苯芥胆甾醇(phenesterine)、泼尼莫司汀(prednimustine)、曲洛磷胺(trofosfamide)、尿嘧啶氮芥(uracilmustard);硝基脲类,例如卡莫司汀(carmustine)、氯脲霉素(chlorozotocin)、福替莫司汀(fotemustine)、洛莫司汀(lomustine)、尼莫司汀(nimustine)和雷尼司汀(ranimnustine);抗生素,例如烯二炔抗生素(例如,卡里奇霉素(calicheamicin),尤其是卡里奇霉素γll和卡里奇霉素Ωll(参见,例如,Agnew,Chem.Intl.Ed.Engl.,33:183-186(1994));达内霉素(dynemicin),包括达内霉素A;双膦酸盐类,例如氯膦酸盐;埃斯佩拉霉素(esperamicin);以及新制癌素发色团(neocarzinostatinchromophore)和相关的色蛋白烯二炔抗生素发色团(relatedchromoproteinenediyneantibioticchromophore)、阿克拉霉素(aclacinomysin)、放线菌素(actinomycin)、安曲霉素(authramycin)、重氮丝氨酸(azaserine)、博来霉素(bleomycin)、放线菌素C(cactinomycin)、卡拉比星(carabicin)、卡米诺霉素(caminomycin)、嗜癌素(carzinophilin)、色霉素(chromomycini)、放线菌素D(dactinomycin)、道诺比星(daunorubicin)、地托比星(detorubicin)、6-重氮-5-氧代-L-正亮氨酸、ADRIAMYCIN多柔比星(doxorubicin)(包括吗啉代多柔比星、氰基吗啉代多柔比星、2-吡咯啉多柔比星和脱氧多柔比星)、表柔比星(epirubicin)、依柔比星(esorubicin)、伊达比星(idarubicin)、麻西罗霉素(marcellomycin)、丝裂霉素(mitomycin)(例如丝裂霉素C)、霉酚酸(mycophenolicacid)、诺加霉素(nogalamycin)、橄榄霉素(olivomycin)、培洛霉素(peplomycin)、泊非霉素(potfiromycin)、嘌呤霉素(puromycin)、三铁阿霉素(quelamycin)、罗多比星(rodorubicin)、链黑菌素(streptonigrin)、链佐星(streptozocin)、杀结核菌素(tubercidin)、乌苯美司(ubenimex)、净司他丁(zinostatin)、佐柔比星(zorubicin);抗代谢药,例如甲氨蝶呤(methotrexate)和5-氟尿嘧啶(5-FU);叶酸类似物,例如二甲叶酸(denopterin)、甲氨蝶呤、蝶罗呤(pteropterin)、曲美沙特(trimetrexate);嘌呤类似物,例如氟达拉滨(fludarabine)、6-巯基嘌呤、硫咪嘌呤(thiamiprine)、硫鸟嘌呤(thioguanine);嘧啶类似物,例如安西他滨(ancitabine)、阿扎胞苷(azacitidine)、6-氮杂尿苷、卡莫氟(carmofur)、阿糖胞苷(cytarabine)、双脱氧尿苷(dideoxyuridine)、多西氟尿苷(doxifluridine)、依西他滨(enocitabine)、氟尿苷(floxuridine);雄激素,例如卡普睾酮(calusterone)、丙酸屈他雄酮(dromostanolonepropionate)、环硫雄醇(epitiostanol)、美雄烷(mepitiostane)、睾内酯(testolactone);抗肾上腺素,例如氨鲁米特(minoglutethimide)、米托坦(mitotane)、曲洛司坦(trilostane);叶酸补充剂,例如亚叶酸(frolinicacid);醋葡醛内酯(aceglatone);醛磷酰胺糖苷(aldophosphamideglycoside);氨基酮戊酸(aminolevulinicacid);恩尿嘧啶(eniluracil)、安吖啶(amsacrine)、贝司他韦(bestrabucil);比生群(bisantrene);依达沙酯(edatraxate);地美可辛(demecolcine);地吖醌(diaziquone);依氟鸟氨酸(elformithine);依利醋铵(elliptiniumacetate);埃博霉素(epothilone);依托格鲁(etoglucid);硝酸镓;羟基脲;香菇多糖(lentinan);洛尼达宁(lonidainine);美登素类(maytansinoids),例如美登素(maytansine)和安丝菌素(ansamitocin);米托胍腙(mitoguazone);米托蒽醌;莫哌达醇(mopidanmol);二胺硝吖啶(nitraerine);喷司他丁(pentostatin);蛋氨氮芥(phenamet);吡柔比星(pirarubicin);洛索蒽醌(losoxantrone);鬼臼酸(podophyllinicacid);2-乙基酰肼;甲基苄肼(procarbazine);PSK多糖复合物(JHSNaturalProducts,Eugene,Oreg.);雷佐生(razoxane);根瘤菌素(rhizoxin);西索菲兰(sizofuran);锗螺胺(spirogermanium);替奴佐酸(tenuazonicacid);三亚胺醌(triaziquone);2,2',2"-三氯三乙胺;单端孢霉烯(trichothecenes)(例如,T-2毒素、维拉库林A(verracurinA)、漆斑菌素A(roridinA)和蛇形菌素(anguidine));乌拉坦(urethan);长春地辛(vindesine);达卡巴嗪(dacarbazine);甘露莫司汀(mannomustine);二溴甘露醇(mitobronitol);二溴卫矛醇(mitolactol);哌泊溴烷(pipobroman);加胞嘧啶(gacytosine);阿拉伯糖苷(arabinoside)(“Ara-C”);环磷酰胺;噻替哌;紫杉醇类(taxoids),例如,TAXOL紫杉醇(paclitaxel)(Bristol-MyersSquibbOncology,Princeton,N.J.)、不含克列莫佛的ABRAXANE、紫杉醇的白蛋白工程纳米粒制剂(American Pharmaceutical Partners,Schaumberg,111.)和TAXOTERE多西紫杉醇(doxetaxel)(Rhone-Poulenc Rorer,Antony,France);苯丁酸氮芥(chloranbucil);GEMZAR吉西他滨(gemcitabine);6-硫鸟嘌呤;巯嘌呤;甲氨蝶呤;铂类似物,例如顺铂(cisplatin)、奥沙利铂(oxaliplatin)和卡铂(carboplatin);长春碱(vinblastine);铂(platinum);依托泊苷(etoposide)(VP-16);异环磷酰胺;米托蒽醌;长春新碱;NAVELBINE长春瑞滨(vinorelbine);诺凡酮(novantrone);替尼泊苷(teniposide);依达曲沙(edatrexate);道诺霉素(daunomycin);氨基蝶呤(aminopterin);希罗达(xeloda);伊班膦酸盐(ibandronate);伊立替康(irinotecan)(Camptosar,CPT-11)(包括伊立替康与5-FU和亚叶酸(leucovorin)的治疗方案);拓扑异构酶抑制剂RFS2000;二氟甲基鸟氨酸(DMFO);类视黄酸,例如视黄酸;卡培他滨(capecitabine);考布他汀(combretastatin);亚叶酸(LV);奥沙利铂,包括奥沙利铂治疗方案(FOLFOX);拉帕替尼(lapatinib)(TYKERB);减少细胞增殖的PKC-α、Raf、H-Ras、EGFR(例如,厄洛替尼(erlotinib)(Tarceva))和VEGF-A的抑制剂以及上述任一种的药学上可接受的盐、酸或衍生物。此外,治疗方法还可包括使用辐射。此外,治疗方法还可包括使用光动力治疗。
在包括但不限于癌症应用在内的各种实施方案中,本发明的另外的剂是一种或多种免疫调节剂,其选自阻断、降低和/或抑制PD-1和PD-L1或PD-L2和/或PD-1与PD-L1或PD-L2的结合的药剂(作为非限制性实例,一种或多种纳武单抗(ONO-4538/BMS-936558、MDX1106、OPDIVO、BRISTOLMYERSSQUIBB)、派姆单抗(KEYTRUDA,Merck)、MK-3475(MERCK)、BMS936559(BRISTOLMYERSSQUIBB)、阿特朱单抗(TECENTRIQ、GENENTECH)、MPDL328OA(ROCHE);增加和/或刺激CD137(4-1BB)和/或CD137(4-1BB)与一种或多种4-1BB配体的结合的剂(作为非限制性实例,乌瑞芦单抗(urelumab)(BMS-663513和抗4-1BB抗体);以及阻断、减少和/或抑制CTLA-4的活性和/或CTLA-4与AP2M1、CD80、CD86、SHP-2和PPP2R5A中的一种或多种的结合和/或OX40与OX40L的结合的剂(作为非限制性实例GBR830(GLENMARK)、MEDI6469(MEDIMMUNE)。
在多个实施方案中,本文所描述的异二聚体蛋白(和/或另外的药剂)包括经修饰的衍生物,即通过将任何类型的分子共价连接至所述物质,使得共价连接不会阻止所述物质的活性。例如,但不作为限制,衍生物包括已经通过尤其是糖基化、脂化、乙酰化、聚乙二醇化、磷酸化、酰胺化、通过已知保护/封闭基团衍生化、蛋白水解裂解、与细胞配体或其他蛋白键联等进行修饰的物质。许多化学修饰中的任何一种都可以通过已知技术进行,包括但不限于特定的化学裂解、乙酰化、甲酰化、衣霉素(turicamycin)的代谢合成等。此外,衍生物可含有一种或多种非经典氨基酸。在其他实施方案中,本文所描述的异二聚体蛋白(和/或另外的药剂)还包括细胞毒性剂,在说明性实施方案中,包括毒素、化疗剂、放射性同位素和引起细胞凋亡或细胞死亡的药剂。此类药剂可与本文所描述的物质缀合。
因此,本文所描述的异二聚体蛋白(和/或另外的药剂)可以在翻译后修饰以添加效应部分例如化学接头、可检测部分例如荧光染料、酶、底物、生物发光材料、放射性材料和化学发光部分或功能部分例如链霉亲和素、亲和素、生物素、细胞毒素、细胞毒性剂和放射性材料。
在一些方面,本公开涉及用于治疗人类受试者的黑色素瘤的方法,其包括向人类受试者施用异二聚体蛋白的步骤,所述异二聚体蛋白包含:(a)第一结构域,其包含能够与γδT细胞受体结合的一个或多个嗜乳脂蛋白家族蛋白或其片段;(b)第二结构域,其包含靶向结构域,所述靶向结构域选自(i)抗体、抗体样分子或其抗原结合片段,和(ii)胞外结构域;和(c)接头,其连接第一结构域和第二结构域。在多个实施方案中,γδT细胞受体包含选自Vγ9、Vγ4、Vγ2、Vγ8、Vγ3和Vγ5的γ链,和选自Vδ2、Vδ1、Vδ3和Vδ5的δ链。在多个实施方案中,γδT细胞受体选自Vg9Vd2(γ9δ2)、Vg9Vd1(γ9δ1)和Vg9Vd3(γ9δ3)。在多个实施方案中,所述一个或多个嗜乳脂蛋白家族蛋白的片段包含胞外结构域和/或可变结构域。在多个实施方案中,异二聚体蛋白包含BTN2A1的部分,其能够结合γδT细胞受体。在多个实施方案中,异二聚体蛋白包含BTN2A1胞外结构域。在多个实施方案中,异二聚体蛋白包含BTN2A1可变结构域。在多个实施方案中,异二聚体蛋白包含BTN3A1的部分,其能够结合γδT细胞受体。在多个实施方案中,异二聚体蛋白包含BTN3A1胞外结构域。在多个实施方案中,异二聚体蛋白包含BTN3A1可变结构域。在多个实施方案中,异二聚体蛋白包含能够结合γδT细胞受体的BTN2A1的部分和/或能够结合γδT细胞受体的BTN3A1的部分。在多个实施方案中,异二聚体蛋白包含胞外结构域BTN2A1和/或BTN3A1。在多个实施方案中,异二聚体蛋白包含可变结构域BTN2A1和/或BTN3A1。
在一些方面,本公开涉及用于治疗人类受试者中的非小细胞肺癌(NSCLC)的方法,其包括向人类受试者施用异二聚体蛋白的步骤,所述异二聚体蛋白包含:(a)第一结构域,其包含能够结合γδT细胞受体的一个或多个嗜乳脂蛋白家族蛋白或其片段;(b)第二结构域,其包含靶向结构域,所述靶向结构域选自(i)抗体、抗体样分子或其抗原结合片段,和(ii)胞外结构域;和(c)接头,其连接第一结构域和第二结构域。在多个实施方案中,γδT细胞受体包含选自Vγ9、Vγ2、Vγ4、Vγ5、Vγ3和Vγ8的γ链,和选自Vδ1、Vδ2、Vδ3、Vδ8和Vδ6的δ链。在多个实施方案中,γδT细胞受体选自Vg9Vd1(γ9δ1)、Vg9Vd2(γ9δ2)和Vg9Vd3(γ9δ3)。在多个实施方案中,所述一个或多个嗜乳脂蛋白家族蛋白的片段包含胞外结构域和/或可变结构域。在多个实施方案中,异二聚体蛋白包含能够结合γδT细胞受体的BTN2A1的部分。在多个实施方案中,异二聚体蛋白包含BTN2A1胞外结构域。在多个实施方案中,异二聚体蛋白包含BTN2A1可变结构域。在多个实施方案中,异二聚体蛋白包含BTN3A1胞外结构域。在多个实施方案中,异二聚体蛋白包含BTN3A1可变结构域。在多个实施方案中,异二聚体蛋白包含能够结合γδT细胞受体的BTN2A1的部分和/或能够结合γδT细胞受体的BTN3A1的部分。在多个实施方案中,异二聚体蛋白包含胞外结构域BTN2A1和/或BTN3A1。在多个实施方案中,异二聚体蛋白包含可变结构域BTN2A1和/或BTN3A1。
在一些方面,本公开涉及一种治疗人类受试者中的结直肠癌的方法,包括向人类受试者施用异二聚体蛋白的步骤,所述异二聚体蛋白包含:(a)第一结构域,其包含能够结合γδT细胞受体的一个或多个嗜乳脂蛋白家族蛋白或其片段;(b)第二结构域,其包含靶向结构域,所述靶向结构域选自(i)抗体、抗体样分子或其抗原结合片段,和(ii)胞外结构域;和(c)接头,其连接第一结构域和第二结构域。在多个实施方案中,γδT细胞受体包含选自Vγ9、Vγ4、Vγ2、Vγ5、Vγ3和Vγ8的γ链,和选自Vδ1、Vδ2、Vδ3和Vδ8的δ链。在多个实施方案中,γδT细胞受体选自Vg9Vd1(γ9δ1)、Vg9Vd2(γ9δ2)和Vg9Vd3(γ9δ3)。在多个实施方案中,所述一个或多个嗜乳脂蛋白家族蛋白的片段包含胞外结构域和/或可变结构域。在多个实施方案中,异二聚体蛋白包含能够结合γδT细胞受体的BTN2A1的部分。在多个实施方案中,异二聚体蛋白包含BTN2A1胞外结构域。在多个实施方案中,异二聚体蛋白包含BTN2A1可变结构域。在多个实施方案中,异二聚体蛋白包含BTN3A1胞外结构域。在多个实施方案中,异二聚体蛋白包含BTN3A1可变结构域。在多个实施方案中,异二聚体蛋白包含能够结合γδT细胞受体的BTN2A1的部分和/或能够结合γδT细胞受体的BTN3A1的部分。在多个实施方案中,异二聚体蛋白包含胞外结构域BTN2A1和/或BTN3A1。在多个实施方案中,异二聚体蛋白包含可变结构域BTN2A1和/或BTN3A1。
制剂
在一个方面,本公开提供了一种药物组合物,其包含本文公开的任何实施方案的异二聚体蛋白。
本文所描述的异二聚体蛋白(和/或另外的药剂)可具有足够碱性的官能团(其可与无机或有机酸反应)或羧基(其可与无机或有机碱反应),以形成药学上可接受的盐。如所属领域中熟知的,药学上可接受的酸加成盐由药学上可接受的酸形成。此类盐包括列于例如Journal of Pharmaceutical Science,66,2-19(1977)和The Handbook ofPharmaceutica lSalts;Properties,Selection,and Use.P.H.Stahl和C.G.Wermuth(编),Verlag,Zurich(瑞士)2002中的药学上可接受的盐,其全部内容通过引用整体并入。
在一些实施方案中,本文所描述的组合物呈药学上可接受的盐形式。
此外,本文所描述的任何异二聚体蛋白(和/或另外的药剂)可以作为包含药学上可接受的载体或媒介物的组合物的组分施用于受试者。此类组合物可任选地包含合适量的药学上可接受的赋形剂以便提供用于适当施用的形式。药用赋形剂可以是液体,例如水和油,包括石油、动物、植物或合成来源的那些油,例如花生油、大豆油、矿物油、芝麻油等。药用赋形剂可以是例如盐水、阿拉伯树胶、明胶、淀粉糊、滑石、角蛋白、胶体二氧化硅、尿素等。另外,可使用辅助剂、稳定剂、增稠剂、润滑剂和着色剂。在一个实施方案中,药学上可接受的赋形剂在施用于受试者时是无菌的。当静脉内施用本文所描述的任何药剂时,水是有用的赋形剂。盐水溶液和葡萄糖和甘油水溶液也可用作液体赋形剂,特别是可注射溶液。适合的药用赋形剂还包括淀粉、葡萄糖、乳糖、蔗糖、明胶、麦芽、米、面粉、白垩、硅胶、硬脂酸钠、单硬脂酸甘油酯、滑石、氯化钠、脱脂奶粉、甘油、丙烯、乙二醇、水、乙醇等。如果需要,本文所描述的任何药剂也可包含少量润湿剂或乳化剂,或pH缓冲剂。
在一些实施方案中,将本文所描述的组合物再悬浮于盐水缓冲液(包括但不限于TBS、PBS等)中。
在各种实施方案中,异二聚体蛋白可与另一种药剂缀合和/或融合以延长半衰期或以其他方式改善药效学和药代动力学特性。在一些实施方案中,异二聚体蛋白可以与PEG、XTEN(例如,作为rPEG)、聚唾液酸(POLYXEN)、白蛋白(例如,人血清白蛋白或HAS)、弹性蛋白样蛋白(ELP)、PAS、HAP、GLK、CTP、转铁蛋白等中的一种或多种融合或缀合。在各种实施方案中,每种单独的异二聚体蛋白与描述于BioDrugs(2015)29:215-239(其全部内容据此通过引用并入)中的一种或多种药剂融合。
施用、剂量和治疗方案
本公开包括各种制剂中的所描述的异二聚体蛋白(和/或另外的药剂)。本文所描述的任何异二聚体蛋白(和/或另外的药剂)可以采用溶液、悬浮液、乳液、滴剂、片剂、丸剂(pill)、弹丸(pellet)、胶囊、含有液体的胶囊、粉末、缓释制剂、栓剂、乳液、气雾剂、喷雾剂、悬浮液或任何其他适合使用的形式。也可以使用编码蛋白序列的DNA或RNA构建体。在一个实施方案中,组合物是胶囊形式(参见例如,美国专利号5,698,155)。合适的药物赋形剂的其他实例描述于通过引用并入的Remington’s Pharmaceutical Sciences1447-1676(Alfonso R.Gennaro eds.,19thed.1995)中。
必要时,包含异二聚体蛋白(和/或另外的药剂)的制剂还可包括增溶剂。此外,所述药剂可以用现有技术已知的合适的媒介物或递送装置递送。本文概述的组合治疗可以在单个递送媒介物或递送装置中共同递送。用于施用的组合物可任选地包括局部麻醉剂,例如利多卡因(lignocaine),以减轻注射部位的疼痛。
包含本公开的异二聚体蛋白(和/或另外的药剂)的制剂可以方便地以单位剂型存在并且可以通过药学领域中熟知的任何方法制备。此类方法通常包括将治疗剂与载体结合的步骤,所述载体构成一种或多种辅助成分。通常,制剂通过将治疗剂与液体载体、细碎的固体载体或两者均匀且紧密地结合,然后,如果需要,将产品成型为所需制剂的剂型(例如,湿法或干法制粒、粉末混合物等,然后使用现有技术已知的常规方法压片)。
在一个实施方案中,本文所描述的任何异二聚体蛋白(和/或另外的药剂)根据常规程序配制为适合本文所描述的施用模式的组合物。
施用途径包括例如:皮内、肌内、腹膜内、静脉内、皮下、鼻内、硬膜外、口服、舌下、鼻内、脑内、阴道内、透皮、直肠、吸入或局部,特别是耳、鼻、眼或皮肤。在一些实施方案中,施用通过口服或肠胃外注射实现。在大多数情况下,施用导致本文所描述的任何药剂释放到血流中。
本文所描述的任何异二聚体蛋白(和/或另外的药剂)可以口服施用。此类异二聚体蛋白(和/或另外的药剂)也可以通过任何其他方便的途径施用,例如通过静脉输注或推注、通过上皮或粘膜皮肤内衬(例如,口腔粘膜、直肠和肠粘膜等)吸收,并且可与另一种生物活性剂一起施用。施用可以是全身的或局部的。各种递送系统是已知的,例如封装在脂质体、微粒、微胶囊、胶囊等中,并且可用于施用。
在特定的实施方案中,可能需要对需要治疗的区域进行局部施用。在一个实施方案中,例如在癌症的治疗中,将异二聚体蛋白(和/或另外的药剂)施用在肿瘤微环境(例如,细胞、分子、胞外基质和/或围绕和/或饲喂肿瘤细胞的血管,包括例如肿瘤血管;肿瘤浸润淋巴细胞;成纤维细胞网状细胞;内皮祖细胞(EPC);癌症相关成纤维细胞;周细胞;其他基质细胞;胞外基质(ECM)的成分;树突状细胞;抗原呈递细胞;T细胞;调节性T细胞;巨噬细胞;中性粒细胞;和位于肿瘤附近的其他免疫细胞)或淋巴结中和/或靶向肿瘤微环境或淋巴结。在各种实施方案中,例如在癌症的治疗中,瘤内施用异二聚体蛋白(和/或另外的药剂)。
在各种实施方案中,本发明的异二聚体蛋白允许提供比常规免疫治疗(例如,用OPDIVO、KEYTRUDA、YERVOY和TECENTRIQ中的一种或多种治疗)中所见更少副作用的双重作用。例如,本发明的异二聚体蛋白减少或预防常见的免疫相关不良事件,所述不良事件影响各种组织和器官,包括皮肤、胃肠道、肾脏、外周和中枢神经系统、肝脏、淋巴结、眼睛、胰腺和内分泌系统;例如垂体炎、结肠炎、肝炎、肺炎、皮疹和风湿病。此外,本发明的局部施用(例如瘤内)避免了标准全身施用(例如IV输注)所见的不良事件,如在与常规免疫疗法(例如,用OPDIVO、KEYTRUDA、YERVOY和TECENTRIQ中的一种或多种治疗)一起使用时。
适用于肠胃外施用(例如,静脉内、肌肉内、腹膜内、皮下和关节内注射和输注)的剂型包括例如溶液、悬浮液、分散液、乳液等。其也可以无菌固体组合物(例如,冻干组合物)的形式制造,其可以在使用前立即溶解或悬浮在无菌可注射介质中。其可以包含例如所属领域已知的悬浮剂或分散剂。
本文所描述的任何异二聚体蛋白(和/或另外的药剂)的剂量以及给药方案可取决于各种参数,包括但不限于所治疗的疾病、受试者的一般健康状况和给药医师的判断。本文所描述的任何异二聚体蛋白可以在施用另外的药剂之前(例如,5分钟、15分钟、30分钟、45分钟、1小时、2小时、4小时、6小时、12小时、24小时、48小时、72小时、96小时、1周、2周、3周、4周、5周、6周、8周或12周之前)、同时或之后(例如,5分钟、15分钟、30分钟、45分钟、1小时、2小时、4小时、6小时、12小时、24小时、48小时、72小时、96小时、1周、2周、3周、4周、5周、6周、8周或12周之后)施用于有需要的受试者。在各种实施方案中,本文所描述的任何异二聚体蛋白和另外的药剂相隔1分钟、相隔10分钟、相隔30分钟、相隔小于1小时、相隔1小时、相隔1小时至2小时、相隔2小时至3小时、相隔3小时至4小时、相隔4小时至5小时、相隔5小时至6小时、相隔6小时至7小时、相隔7小时至8小时、相隔8小时至9小时、相隔9小时至10小时、相隔10小时至11小时、相隔11小时至12小时、相隔1天、相隔2天、相隔3天、相隔4天、相隔5天、相隔6天、相隔1周、相隔2周、相隔3周或相隔4周施用。
在多种实施方案中,本公开涉及共同施用诱导先天免疫应答的异二聚体蛋白和诱导适应性免疫应答的另一种异二聚体蛋白。在此类实施方案中,诱导先天免疫应答的异二聚体蛋白可以在诱导适应性免疫应答的异二聚体蛋白的施用之前、同时或之后施用。例如,异二聚体蛋白可以相隔1分钟、相隔10分钟、相隔30分钟、相隔小于1小时、相隔1小时、相隔1小时至2小时、相隔2小时至3小时、相隔3小时至4小时、相隔4小时至5小时、相隔5小时至6小时、相隔6小时至7小时、相隔7小时至8小时、相隔8小时至9小时、相隔9小时至10小时、相隔10小时至11小时、相隔11小时至12小时、相隔1天、相隔2天、相隔3天、相隔4天、相隔5天、相隔6天、相隔1周、相隔2周、相隔3周或相隔4周施用。在说明性的实施方案中,诱导先天免疫应答的异二聚体蛋白和诱导适应性反应的异二聚体蛋白相隔1周施用,或隔周施用(即,在施用诱导先天免疫应答的异二聚体蛋白的1周后施用诱导适应性免疫应答的异二聚体蛋白,等等)。
本文所描述的任何异二聚体蛋白(和/或另外的药剂)的剂量可取决于若干因素,包括疾病的严重程度、是否要治疗或预防疾病以及要治疗的受试者的年龄、体重和健康状况。此外,关于特定受试者的药物基因组学(基因型对治疗药物的药代动力学、药效学或疗效特征的影响)信息可能会影响使用的剂量。此外,确切的个体剂量可以根据多种因素进行某种程度的调整,包括施用的药剂的特定组合、施用时间、施用途径、制剂的性质、排泄率、正在治疗的特定疾病、病症的严重程度以及病症的解剖学位置。可以预期剂量可有一些变化。
对于通过肠胃外注射施用本文所描述的任何异二聚体蛋白(和/或另外的药剂),剂量可以是每天约0.1mg至约250mg、每天约1mg至约20mg或每天约3mg至约5mg。通常,当口服或肠胃外施用时,本文所描述的任何药剂的剂量可为每天约0.1mg至约1500mg、或每天约0.5mg至约10mg、或每天约0.5mg至约5mg、或每天约200至约1,200mg(例如,每天约200mg、约300mg、约400mg、约500mg、约600mg、约700mg、约800mg、约900mg、约1,000mg、约1,100mg、约1,200mg)。
在一些实施方案中,本文所描述的异二聚体蛋白(和/或另外的药剂)的施用是以每次治疗约0.1mg至约1500mg、或每次治疗约0.5mg至约10mg、或每次治疗约0.5mg至约5mg、或每次治疗约200mg至约1,200mg(例如,每次治疗约200mg、约300mg、约400mg、约500mg、约600mg、约700mg、约800mg、约900mg、约1,000mg、约1,100mg、约1,200mg)的剂量通过肠胃外注射进行。
在一些实施方案中,异二聚体蛋白(和/或另外的药剂)的合适剂量在约0.01mg/kg至约100mg/kg受试者体重或约0.01mg/kg至约10mg/kg受试者体重的范围内,例如约0.01mg/kg、约0.02mg/kg、约0.03mg/kg、约0.04mg/kg、约0.05mg/kg、约0.06mg/kg、约0.07mg/kg、约0.08mg/kg、约0.09mg/kg、约0.1mg/kg、约0.2mg/kg、约0.3mg/kg、约0.4mg/kg、约0.5mg/kg、约0.6mg/kg、约0.7mg/kg、约0.8mg/kg、约0.9mg/kg、约1mg/kg、约1.1mg/kg、约1.2mg/kg、约1.3mg/kg、约1.4mg/kg、约1.5mg/kg、约1.6mg/kg、约1.7mg/kg、约1.8mg/kg、1.9mg/kg、约2mg/kg、约3mg/kg、约4mg/kg、约5mg/kg、约6mg/kg、约7mg/kg、约8mg/kg、约9mg/kg、约10mg/kg体重,包括其间的所有值和范围。
在另一个实施方案中,递送可以在囊泡中,特别是脂质体中(参见Langer,1990,Science249:1527-1533;Treat等人.,在Liposomes in the Therapy of InfectiousDisease and Cancer中,Lopez-Berestein和Fidler(编),Liss,New York,pp.353-365(1989)。
本文所描述的任何异二聚体蛋白(和/或另外的药剂)可以通过控释或缓释方式或通过所属领域普通技术人员熟知的递送装置施用。实例包括但不限于美国专利号3,845,770;3,916,899;3,536,809;3,598,123;4,008,719;5,674,533;5,059,595;5,591,767;5,120,548;5,073,543;5,639,476;5,354,556;和5,733,556中描述的那些,每个都通过引用整体并入本文。此类剂型可用于使用例如羟丙基甲基纤维素、其他聚合物基质、凝胶、可渗透膜、渗透系统、多层包衣、微粒、脂质体、微球或其组合提供一种或多种活性成分的控释或缓释,以提供不同比例的所需释放曲线。活性成分的控释或缓释可以通过各种条件刺激,所述条件包括但不限于pH值变化、温度变化、适当波长的光刺激、酶的浓度或可用性、水的浓度或可用性,或其他生理条件或化合物。
在另一个实施方案中,可以使用聚合物材料(参见Medical Applications ofControlled Release,Langer和Wise(编),CRC Pres.,Boca Raton,Florida(1974);Controlled Drug Bioavailability,Drug Product Design and Performance,Smolen和Ball(编),Wiley,New York(1984);Ranger和Peppas,1983,J.Macromol.Sci.Rev.Macromol.Chem.23:61;还参见Levy等人,1985,Science228:190;During等人,1989,Ann.Neurol.25:351;Howard等人,1989,J.Neurosurg.71:105)。
在另一实施方案中,控释系统可以放置在待治疗的目标区域附近,因此仅需要全身剂量的一部分(参见例如Goodson,Medical Applications of Controlled Release,见前文,vol.2,pp.115-138(1984))。可以使用由Langer,1990,Science249:1527-1533)的评述中讨论的其他控释系统。
本文所描述的任何异二聚体蛋白(和/或另外的药剂)的施用可以独立地为每天一至四次或每月一至四次或每年一至六次或每两年、三年、四年或五年一次。施用可以持续一天或一个月、两个月、三个月、六个月、一年、两年、三年,并且甚至可以持续受试者的一生。
可以根据多种因素来选择利用本文所描述的任何异二聚体蛋白(和/或另外的药剂)的给药方案,所述因素包括受试者的类型、物种、年龄、体重、性别和医学状况;待治疗疾患的严重程度;施用途径;受试者的肾或肝功能;个体的药物基因组构成;和所采用的本发明的特定化合物。本文所描述的任何异二聚体蛋白(和/或另外的药剂)可以每日单剂量施用,或每日总剂量可以每天两次、三次或四次的分剂量施用。此外,本文所描述的任何异二聚体蛋白(和/或另外的药剂)可以在整个给药方案中连续而不是间歇地施用。
细胞和核酸
在一个方面,本公开提供了一种表达载体,其包含编码本文公开的任何实施方案的异二聚体蛋白的第一和/或第二多肽链的核酸。在一些实施方案中,表达载体是哺乳动物表达载体。在一些实施方案中,表达载体包含DNA或RNA。在一些实施方案中,在一个方面,本公开提供一种宿主细胞,其包含本文公开的任一实施方案的表达载体。
在各种实施方案中,本公开提供了表达载体,其包含编码本文所描述的异二聚体蛋白(例如,包含第一和第二多肽链的异二聚体蛋白)的核酸。在多种实施方案中,表达载体包含DNA或RNA。在多种实施方案中,表达载体是哺乳动物表达载体。
原核和真核载体均可用于表达异二聚体蛋白。原核载体包括基于大肠杆菌序列的构建体(参见,例如Makrides,Microbiol Rev 1996,60:512-538)。可以用于在大肠杆菌中表达的调控区的非限制性实例包括lac、trp、lpp、phoA、recA、tac、T3、T7和λP
在一些实施方案中,本发明的表达载体包含至少编码异二聚体蛋白(和/或另外的药剂)的第一和/或第二多肽链或其互补序列的核酸,其有效地连接至在哺乳动物细胞中起作用的表达控制区或其互补序列。表达控制区能够驱动有效连接的阻断剂和/或刺激剂编码核酸的表达,使得阻断剂和/或刺激剂在用表达载体转化的人细胞中产生。
表达控制区是影响有效连接的核酸的表达的调节性多核苷酸(在本文中有时称为元件),例如启动子和增强子。本发明的表达载体的表达控制区能够在人细胞中表达有效连接的编码核酸。在一个实施方案中,细胞是肿瘤细胞。在另一个实施方案中,细胞是非肿瘤细胞。在一个实施方案中,表达控制区赋予有效连接的核酸可调节的表达。信号(有时称为刺激)可以增加或减少与这种表达控制区有效连接的核酸的表达。这种响应信号而增加表达的表达控制区通常被称为诱导型。这种响应信号而降低表达的表达控制区通常被称为阻抑型。通常,这些元件赋予的增加或减少的量与存在的信号的量成正比;信号的量越大,表达的增加或减少就越大。
在一个实施方案中,本公开考虑使用能够响应于信号瞬时实现高水平表达的诱导型启动子。例如,当在肿瘤细胞附近时,用包含这种表达控制序列的异二聚体蛋白(和/或另外的药剂)的表达载体转化的细胞通过将转化的细胞暴露于适当的信号而被诱导瞬时产生高水平的所述药剂。说明性诱导型表达控制区包括那些包含用信号(诸如小分子化合物)刺激的诱导型启动子的诱导型表达控制区。具体的实例可见于例如美国专利号5,989,910、5,935,934、6,015,709和6,004,941中,这些专利各自以引用的方式整体并入本文。
表达控制区和基因座控制区包括全长启动子序列,例如天然启动子和增强子元件,以及保留全部或部分全长或非变体功能的子序列或多核苷酸变体。如本文所用,当用于指核酸序列、子序列或片段时,术语“功能”和其语法变体是指所述序列具有天然核酸序列(例如,非变体或未修饰的序列)的一种或多种功能。
如本文所用,“有效的连接(operable linkage)”是指如此描述的组分的物理并置允许其以其预期的方式起作用。在与核酸有效连接的表达控制元件的实例中,这种关系使得控制元件调节所述核酸的表达。通常,调节转录的表达控制区并置在转录核酸的5’端附近(即,上游)。表达控制区也可以位于转录序列的3’端(即,下游)或转录物内(例如,内含子中)。表达控制元件可位于距转录序列一定距离处(例如,距所述核酸100至500、500至1000、2000至5000或更多个核苷酸)。表达控制元件的一个具体实例是启动子,其通常位于转录序列的5'。表达控制元件的另一个实例是增强子,其可以位于转录序列的5'或3',或位于转录序列内。
在人细胞中起作用的表达系统是所属领域中熟知的,并且包括病毒系统。通常,在人细胞中起作用的启动子是能够结合哺乳动物RNA聚合酶并起始编码序列下游(3')转录为mRNA的任何DNA序列。启动子将具有转录起始区,其通常位于编码序列的5'端附近,并且通常为位于转录起始位点上游25-30个碱基对处的TATA盒。TATA盒被认为会引导RNA聚合酶II在正确的位点处开始RNA合成。启动子通常还包含上游启动子元件(增强子元件),通常位于TATA盒上游100至200个碱基对内。上游启动子元件决定了转录起始的速率,并且可以在任一方向上起作用。特别用作启动子的是来自哺乳动物病毒基因的启动子,因为病毒基因通常高度表达并且具有广泛的宿主范围。实例包括SV40早期启动子、小鼠乳腺肿瘤病毒LTR启动子、腺病毒主要晚期启动子、单纯疱疹病毒启动子和CMV启动子。
通常,哺乳动物细胞识别的转录终止和聚腺苷酸化序列是位于翻译终止密码子的3'端的调节区,并且因此与启动子元件一起位于编码序列的侧翼。成熟mRNA的3'末端由位点特异性翻译后切割和聚腺苷酸化形成。转录终止子和聚腺苷酸化信号的实例包括源自SV40的那些。内含子也可包括在表达构建体中。
存在多种可用于将核酸引入到活细胞中的技术。适用于体外将核酸转移至哺乳动物细胞中的技术包括使用脂质体、电穿孔、显微注射、细胞融合、聚合物基系统、DEAE-葡聚糖、病毒转导、磷酸钙沉淀法等。对于体内基因转移,还可以使用多种技术和试剂,包括脂质体;基于天然聚合物的媒介物,例如壳聚糖和明胶;病毒载体也适用于体内转导。在一些情况下,需要提供靶向剂,诸如对细胞表面膜蛋白具有特异性的抗体或配体。在使用脂质体的情况下,和与胞吞作用相关的细胞表面膜蛋白结合的蛋白可用于靶向和/或促进摄取,例如,对于特定细胞类型有趋向性的衣壳蛋白或其片段、针对在循环过程中发生内化的蛋白的抗体、靶向细胞内定位和延长细胞内半衰期的蛋白。受体介导的内吞作用技术描述于例如Wu等人,J.Biol.Chem.262,4429-4432(1987);和Wagner等人,Proc.Natl.Acad.Sci.USA87,3410-3414(1990)中。
在适当情况下,也可以采用基因递送剂,例如整合序列。许多整合序列是所属领域中已知的(参见,例如,Nunes-Duby等人,NucleicAcidsRes.26:391-406,1998;Sadwoski,J.Bacteriol.,165:341-357,1986;Bestor,Cell,122(3):322-325,2005;Plasterk等人,TIG15:326-332,1999;Kootstra等人,Ann.Rev.Pharm.Toxicol.,43:413-439,2003)。这些包括重组酶和转座酶。实例包括Cre(Sternberg和Hamilton,J.Mol.Biol.,150:467-486,1981),lambda(Nash,Nature,247,543-545,1974),Flp(Broach等人,Cell,29:227-234,1982),R(Matsuzaki等人,J.Bacteriology,172:610-618,1990),cpC31(参见,例如,Groth等人,J.Mol.Biol.335:667-678,2004),水手家族的睡美人转座酶(Plasterk等人,见前文),以及用于整合病毒的组分,例如AAV、逆转录病毒以及具有提供病毒整合的组分的抗病毒,诸如逆转录病毒或慢病毒的LTR序列和AAV的ITR序列(Kootstra等人,Ann.Rev.Pharm.Toxicol.,43:413-439,2003)。此外,直接和靶向遗传整合策略可用于插入编码嵌合融合蛋白的核酸序列,包括CRISPR/CAS9、锌指、TALEN和大范围核酸酶基因编辑技术。
在一个方面,本发明提供的用于表达异二聚体蛋白(和/或另外的药剂)的表达载体是病毒载体。许多可用于基因治疗的病毒载体是已知的(参见,例如,Lundstrom,TrendsBiotechnol.,21:117,122,2003)。说明性病毒载体包括选自抗病毒(LV)、逆转录病毒(RV)、腺病毒(AV)、腺相关病毒(AAV)和α病毒的那些病毒载体,但也可以使用其他病毒载体。对于体内用途,适合使用不整合到宿主基因组中的病毒载体,例如α病毒和腺病毒。α病毒的说明性类型包括辛德毕斯病毒(Sindbis virus)、委内瑞拉马脑炎(Venezuelan equineencephalitis;VEE)病毒和塞姆利基森林病毒(Semliki Forest virus;SFV)。对于体外用途,整合到宿主基因组中的病毒载体是合适的,例如逆转录病毒、AAV和抗病毒。在一个实施方案中,本发明提供了体内转导人细胞的方法,包括使实体瘤在体内与本发明的病毒载体接触。
在多种实施方案中,本公开提供了一种宿主细胞,其包括包含本文所描述的异二聚体蛋白的表达载体。
可以将表达载体引入宿主细胞以产生本发明的异二聚体蛋白。例如,细胞可在体外培养或被基因工程改造。有用的哺乳动物宿主细胞包括但不限于源自人、猴子和啮齿动物的细胞(参见,例如,Kriegler,“Gene Transfer and Expression:A LaboratoryManual,”1990,New York,Freeman&Co.)。这些细胞包括被SV40转化的猴肾细胞系(例如,COS-7、ATCCCRL1651);人胚胎肾细胞系(例如,293、293-EBNA或被亚克隆以便在悬浮培养物中生长的293细胞,Graham等人,J Gen Viro l1977,36:59);幼仓鼠肾细胞(例如,BHK,ATCCCCL 10);中国仓鼠卵巢细胞-DHFR(例如,CHO,Urlaub和Chasin,Proc Natl Acad Sci USA1980,77:4216);DG44CHO细胞,CHO-K1细胞,小鼠支持细胞(Mather,Biol Reprod 1980,23:243-251);小鼠成纤维细胞(例如,NIH-3T3);猴肾细胞(例如,CV1 ATCC CCL 70);非洲绿猴肾细胞(例如,VERO-76,ATCC CRL-1587);人宫颈癌细胞(例如,HELA,ATCC CCL 2);犬肾细胞(例如,MDCK,ATCC CCL 34);水牛大鼠肝细胞(例如,BRL3A,ATCC CRL 1442);人肺细胞(例如,W138,ATCC CCL 75);人肝细胞(例如,Hep G2,HB 8065);以及小鼠乳腺肿瘤细胞(例如,MMT 060562,ATCC CCL51)。用于表达本文所描述的融合蛋白的说明性癌细胞类型包括小鼠成纤维细胞系NIH3T3、小鼠刘易斯(Lewis)肺癌细胞系LLC、小鼠肥大细胞瘤细胞系P815、小鼠淋巴瘤细胞系EL4及其卵清蛋白转染子E.G7、小鼠黑色素瘤细胞系B16F10、小鼠纤维肉瘤细胞系MC57以及人小细胞肺癌细胞系SCLC#2和SCLC#7。
宿主细胞可以从正常受试者或受影响的受试者(包括健康人和癌症患者)、私人实验室存储物、公共培养物保藏中心(例如美国典型培养物保藏中心(American TypeCulture Collection))或商业供应商处获得。
可用于体外、离体和/或体内产生本发明的异二聚体蛋白的细胞包括但不限于上皮细胞、内皮细胞、角质细胞、成纤维细胞、肌肉细胞、肝细胞;血细胞,例如T淋巴细胞、B淋巴细胞、单核细胞、巨噬细胞、嗜中性粒细胞、嗜酸性粒细胞、巨核细胞、粒细胞;各种干细胞或祖细胞,特别是造血干细胞或祖细胞(例如,如从骨髓中获得)、脐带血、外周血、胎肝等。细胞类型的选择取决于所治疗或预防的肿瘤的类型,并且可由所属领域技术人员来确定。
含Fc大分子(例如Fc融合蛋白)的生产和纯化已成为标准化过程,产品之间只需稍作修改。例如,许多含Fc的大分子是由人胚胎肾(HEK)细胞(或其变体)或中国仓鼠卵巢(CHO)细胞(或其变体)或在某些情况下通过细菌或合成方法产生的。生产后,由HEK或CHO细胞分泌的含Fc的大分子通过与蛋白A柱结合进行纯化,然后使用各种方法进行“精制”。通常,将纯化的含Fc的大分子以液体形式储存一段时间,长时间冷冻或在某些情况下冻干。在多种实施方案中,与传统的含Fc的大分子相比,本文考虑的异二聚体蛋白的产生可具有独特的特征。在某些实例中,异二聚体蛋白可以使用特定层析树脂或使用不依赖于蛋白A捕获的层析方法来纯化。在其他实施方案中,异二聚体蛋白可以寡聚状态或以多种寡聚状态纯化,并且使用特定方法富集特定寡聚状态。不受理论束缚,这些方法可包括用包括特定盐浓度、pH和添加剂组合物的特定缓冲液处理。在其他实例中,此类方法可包括相比一种寡聚状态而有利于另一种寡聚状态的处理。在本文获得的异二聚体蛋白可以使用所属领域特定的方法另外“精制(polished)”。在一些实施方案中,异二聚体蛋白高度稳定并且能够耐受宽范围的pH暴露(pH3-12之间),能够耐受大量冻/融应激(大于3个冻/融循环)并且能够耐受高温下的长时间孵育(40摄氏度下超过2周)。在其他实施方案中,异二聚体蛋白显示保持完整,在这类应激条件下没有降解、脱酰胺等的迹象。
受试者和/或动物
在一些实施方案中,受试者和/或动物是哺乳动物,例如,人、小鼠、大鼠、豚鼠、狗、猫、马、牛、猪、兔、羊或非人灵长类动物,例如猴子、黑猩猩或狒狒。在其他实施方案中,受试者和/或动物是非哺乳动物,例如斑马鱼。在一些实施方案中,受试者和/或动物可以包含荧光标记(例如利用GFP标记)的细胞。在一些实施方案中,受试者和/或动物是包含荧光细胞的转基因动物。
在一些实施方案中,受试者和/或动物是人。在一些实施方案中,人是儿童。在其他实施方案中,人是成年人。在其他实施方案中,人是老年人。在其他实施方案中,人可被称为患者。
在某些实施方案中,人的年龄范围为约0个月至约6个月、约6至约12个月、约6至约18个月、约18至约36个月、约1至约5岁、约5至约10岁、约10至约15岁、约15至约20岁、约20至约25岁、约25至约30岁,大约30岁至约35岁、约35岁至约40岁、约40岁至约45、约45岁至约50岁、约50岁至约55岁、约55至约60岁、约60至约65岁,约65至约70岁、约70至约75岁、约75至约80岁、约80至约85岁、约85至约90岁、约90至约95岁或约95至约100岁。
在其他实施方案中,受试者是非人动物,因此本发明涉及兽医用途。在一个具体实施方案中,非人动物是家庭宠物。在另一个具体实施方案中,非人动物是家畜动物。
试剂盒
本发明提供可简化本文所描述的任何药剂的施用的试剂盒。本发明的示例性试剂盒包含单位剂型的本文所描述的任何组合物。在一个实施方案中,单位剂型是容器,例如预装注射器,其可以是无菌的,含有本文所描述的任何药剂和药学上可接受的载体、稀释剂、赋形剂或媒介物。试剂盒还可包括指示使用本文所描述的任何药剂的标签或印刷说明书。试剂盒还可包括开睑器、局部麻醉剂和用于施用位置的清洁剂。试剂盒还可进一步包括一种或多种本文所描述的另外的药剂。在一个实施方案中,试剂盒包括含有有效量的本发明组合物和有效量的另一种组合物(例如本文所描述的那些组合物)的容器。
定义
如本说明书和所附权利要求书中所使用的,单数形式“a”、“an”和“the”包括复数指示物,除非上下文另外明确指出。
除非特别说明或从上下文显而易见,否则如本文所用,术语“或”应理解为包括性的并且涵盖“或”和“和”两者。
除非具体说明或从上下文显而易见,否则如本文所用,术语“约”应理解为在本领域的正常容忍范围内,例如在平均值的2个标准偏差内。“约”理解为在所述值的10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%、0.1%、0.05%或0.01%之内。除非上下文另有明确说明,否则本文提供的所有数值均由术语“约”修饰。
所述范围应理解为所述范围端点之间和端点处的任何值。作为示例,1至5之间的范围包括1、2、3、4和5;1至10之间的范围包括1、2、3、4、5、6、7、8、9和10;1至100之间的范围包括1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99、100。
除非另有定义,否则本文使用的所有技术和科学术语具有与本发明所属领域的普通技术人员通常理解的相同含义。尽管与本文描述的那些类似或等同的其他探针、组合物、方法和试剂盒可以用于本公开的实践,但是本文描述了优选的材料和方法。应当理解,本文中使用的术语仅是出于描述特定实施方案的目的,并且不旨在进行限制。
本文所述的任何方面或实施方案均可以与本文公开的任何其他方面或实施方案组合。
本发明将在以下实施例中进一步描述,这些实施例并不限制权利要求中描述的本发明的范围。
实施例
提供本文的实施例是为了说明本技术的优点和益处,并进一步帮助本领域普通技术人员制备或使用本技术的嵌合蛋白。本文的实施例还为了更充分地说明本技术的优选方面。这些实施例决不应被解释为限制如所附权利要求所定义的本技术的范围。这些实施例可以包括或并入上述的本技术的任何变体、方面或实施方案。上述变体、方面或实施方案还可以进一步各自包括或并入本技术的任何或所有其他变体、方面或实施方案的变体。
实施例1:来自癌症患者的匹配的外周血单核细胞(PBMC)和解离肿瘤组织中的γ和δ链配对
为了比较来自前列腺癌患者的匹配的外周血单核细胞(PBMC)和解离肿瘤组织中的γ和δ链配对,对γ和δ链进行了测序。如图1A所示,从前列腺癌患者获得PBMC和解离肿瘤组织。在对γδTCR进行抗体染色后,通过流式细胞术将样品中的γδT细胞单细胞分选至96孔板中。制备RNA并使用iPAIR PCR技术(iRepertoire)对γ和δ链进行测序。iPair分析仪软件用于在单细胞水平上识别γδ链序列和配对。观察到的δ链数量相对于配对的γ链进行绘图。如图1B所示,患者的PBMC显示出特定γ-δ配对的有限多样性。相比之下,如图1C所示,患者的解离肿瘤样品中的γ和δ链配对显示出更多的多样性。
数据表明,在患者PBMC中,表达Vγ9δ2和Vγ4δ1TCR的GDT细胞存在较多。还检测到表达Vγ8δ1TCR的GDT细胞丰度较低。在解离的肿瘤样品中,观察到GDT细胞中γδ链配对的多样性较高,其中Vγ4δ1最为丰富。因此,与其他γδTCR相比,针对Vγ4δ1的治疗很可能对患者的肿瘤更有效。此外,这些数据表明不同的BTN异二聚体可能会优先激活组织限制的γδT细胞亚群。
实施例2:来自前列腺癌患者的匹配的外周血单核细胞(PBMC)和解离肿瘤组织中抗原特异性γ和δ链的多样性
为了了解肿瘤中观察到的较高多样性的γδ链配对是否与抗原特异性的任何改变相关,对γ链的使用和γ链高变或互补决定区CDR3的序列进行了比较。如图3A所示,解离的肿瘤表现出γ链CDR3序列的一些多样性。前10种CDR3的序列列于图3A中的CDR3树图下方。相比之下,PBMC中CDR3序列的多样性也显示出CDR使用的多样性(图3B)。前10种CDR3的序列列于图3A-图3B中的CDR3树图下方。γ链使用的比较再次证实了肿瘤中γ链使用的多样性较高。
δ链使用的CDR3树图比较显示出与PBMC相似的肿瘤趋势。例如,解离的肿瘤(图4A)和PBMC(图4B)均显示出δ链CDR3序列的多样性。前10种CDR3的序列列于图4A-图4B中的CDR3树图下方。γ链使用的比较再次证实了肿瘤中δ链使用的多样性较高。
数据表明,针对特定γδTCR的治疗会将治疗靶向至患者的肿瘤。因此,与外周血比较分析肿瘤中的γδTCR库的方法可用于鉴定癌症治疗的方法或选择患者进行治疗的方法。
实施例3:来自所选TCGA肿瘤类型的解离肿瘤的γδTCR的单细胞分选和测序
为了进一步扩展该分析,对来自癌症患者的样品进行单细胞测序分析,以确定肿瘤组织和肿瘤浸润淋巴细胞(TIL)中的γ和δ链配对,如图2所示。简言之,机械解离新鲜切除的肿瘤组织以产生肿瘤和肿瘤浸润淋巴细胞(TIL)的单细胞悬浮液。样品中的γδT细胞用泛γδTCR抗体染色,并通过流式细胞术单细胞分选至96孔板中。从细胞中提取RNA,并使用iPAIRPCR技术(iRepertoire)对TCRγ和TCRδ链进行扩增和测序。iPair分析仪软件用于在单细胞水平上识别γ和δ链序列和配对。
为了表征外周血和组织限制性γδT细胞之间的潜在差异,进行了多层分析,包括对来自人类黑色素瘤、前列腺癌和结肠癌患者的配对的外周血和肿瘤组织的γδTTCR和CDR3分析进行单细胞测序。Bolotin等,TCR identification was assessed using MiXCRversion 2.1.6 with custom R scripts.MiXCR:software for comprehensive adaptiveimmunity profiling,Nature Methods 12:380-381(2015)。IMGTTCR库序列参考imgt.201918-4.sv5.json用于促进种系TCRγ和TCRδ基因的比对以及库的组装。Lefranc,IMGT,the International ImMunoGeneTics Information System,Cold Spring HarbProtoc2011(6):595-603(2011)。四种癌症基因组图谱(TCGA)肿瘤类型(COAD、DLBC、SARC和STAD)的批量RNA-seqfastq文件用作输入。为了使捕获TCRγ和TCRδ比对的灵敏度最大化,将MiXCR中的比对功能使用assemblePartial和延伸选项运行。使用Salmon准比对方法进行基因表达的定量。Patro等,Salmon provides fast and bias-aware quantification oftranscript expression,Nature Methods14:417-419(2017)。Gencode GrCH38 v27 CHR转录本用于构建用于Salmon的索引。Frankish等,“GENCODE reference annotation for thehuman and mouse genomes.”Nucleic Acids Research 47(D1):D766-D773(2018)。
使用MiXCR框架分析结直肠腺癌(图5A)、弥漫性大B细胞淋巴瘤(DLBCL)(图5B)、肉瘤(图5C)和胃腺癌(图5D)的TCGA数据集的γδTCR使用。结果显示,所有肿瘤均表达广泛使用的多种Vγ链,而Vδ链仅限于TRDV1、2和3,其中Vδ1在四种肿瘤类型中最为普遍。
实施例4:单细胞RNA测序检测结直肠腺癌患者中匹配的肿瘤和外周血中的γδTCR使用和CDR3多样性
接下来,γδTCR的单细胞RNA测序是从结直肠肿瘤和匹配的外周血中进行的。图6A显示了来自结直肠肿瘤的Vγ链的单细胞RNA测序。图6B显示了来自结直肠肿瘤的Vδ链的单细胞RNA测序。图6C显示了来自匹配的外周血的Vγ链的单细胞RNA测序。图6D显示了来自匹配的外周血的Vδ链的单细胞RNA测序。如图6A至图6D所示,在肿瘤和匹配的外周血之间观察到Vγ链和Vδ链使用的明显不同。肿瘤衍生的γδT细胞表达多种γ链,其中TRGV9和TRGV4最丰富(图6A)。与主要表达TRDV2的外周血γδT细胞相比,结直肠肿瘤衍生的γδT细胞还表达更多的TRDV1(比较图6B和图6D)。
对来自单个患者的外周血和肿瘤中的Vγ和Vδ链的CDR3进行序列分析,并以代表性CDR3树图的形式示出。图6E显示了结直肠癌肿瘤中的Vγ和Vδ链的CDR3序列分析。图6F显示了外周血中的Vγ和Vδ链的CDR3序列分析。如图6E和图6F所示,与肿瘤相比,在外周血中观察到γ和δ链均具有更大的多样性。与外周血相比,在结直肠肿瘤中观察到γδT细胞的克隆扩增。
实施例5:结直肠腺癌中BTN/L与γδTCR表达的关联性
接下来,为了评估BTN/L和γδTCR表达的相关性,通过单细胞RNA测序对结直肠腺癌衍生的γδT细胞中某些BTN或BTNL蛋白的表达进行Spearman关联性分析。显示了BTN3A1(图7A)、BTN2A1(图7B)、BTNL3(图7C)和BTNL8(图7D)的结果。还对γ链(TRGV9)(图7E)和δ链(TRDV1)(图7)的表达进行了类似的分析。尽管BTN3A1表达与TRGV9和TRDV1部分关联,但BTN2A1表达与这些选择的γ和δ链明显缺乏关联性。
这些结果尤其证明了嗜乳脂蛋白表达和γδTCR表达彼此关联。因此,这些结果表明,评估样品中一种或多种γ/δT细胞受体(TCR)链和/或嗜乳脂蛋白的存在、不存在或水平可用于鉴定癌症治疗、选择癌症治疗的患者和/或制备用于治疗癌症患者的癌症的药剂。
实施例6:开发基于Jurkat-76细胞系的体外测定,以筛选可激活使用单细胞RNA测序检测的特定γδTCR的BTN/L配对
为了研究BTN/L配对是否激活特定的γδTCR,开发了一种体外测定。简言之,开发了基于Jurkat-76细胞系的报告系统,来筛选能够激活单细胞RNA测序管道揭示的特定γδTCR的各种BTN/L组合。在一个示例性实施例中,如图8A(上小图)所示,构建了表达γ9δ2T细胞受体(TCR)的Jurkat76细胞。如图8A(下小图)所示,CD69的表达可以用作γδT细胞激活的标志物。为了测试这一点,用板结合的试剂刺激亲本Jurkat-76或表达Vγ9δ2TCR复合物的Jurkat-76,如沿X轴所示,刺激24小时。通过CD69的表面表达来评估细胞活化,如流式细胞术所确定。如图8B所示,显示了板结合的BTN2A1加BTN3A1能够在存在CD28共刺激的情况下激活Vγ9δ2TCR。与GADLEN(或BTN2A1+3A1)和共刺激在激活原代γ/δT细胞中的作用一致,GADLEN或BTN2A1+BTN3A1与抗CD28刺激组合导致了Jurkat-76-Vg9d2+激活。与原代γδT细胞不同,Jurkat-76-Vγ9δ2+不表达NKG2D。因此,在该测定模式中,GADLEN或BTN2A1+BTN3A1与抗NKG2D组合不会导致细胞激活。GADLEN或BTN2A1+BTN3A1介导的Jurkat-76细胞激活仅在Vγ9δ2TCR存在时发生,进一步证实了BTN2A1/3A1与TCR的直接相互作用。
图9显示的非限制性GADLEN设计由通过Fc接头与靶向肿瘤抗原的scFv结构域融合的嗜乳脂蛋白胞外结构域的异二聚体组成。不受理论的束缚,GADLEN通过BTN/L异二聚体结构域激活γδTCR并通过scFv结构域结合表面肿瘤抗原诱来导肿瘤细胞的靶向杀伤(图9)。因此,如图9所示,不受理论的束缚,可以产生通过BTN/L异二聚体结构域激活γδTCR并引起肿瘤细胞的靶向杀伤的GADLEN治疗。
实施例7:黑色素瘤、非小细胞肺癌和结直肠癌肿瘤中的γ(TRGV)和δ(TRDV)链T细胞受体使用
对46个肿瘤(20个结直肠癌肿瘤、20个非小细胞肺癌(NSCLC)和6个黑色素瘤肿瘤)进行γ-δ(γδ)链使用的分析。对患者肿瘤样品中的T细胞进行单细胞测序分析以及γ(TRGV)和δ(TRDV)链的批量RNA测序。
对于单细胞测序分析,简言之,机械解离新鲜切除的肿瘤组织以产生肿瘤和肿瘤浸润淋巴细胞(TIL)的单细胞悬浮液。将样品中的γδT细胞用泛γδTCR抗体染色,并通过流式细胞术单细胞分选至96孔板中。从细胞中提取RNA,并使用iPAIRPCR技术(iRepertoire)对TCRγ和TCRδ链进行扩增和测序。iPair分析仪软件用于在单细胞水平上识别γ和δ链序列和配对。此外,肿瘤浸润免疫细胞中的TCRγ和TCRδ链是从批量肿瘤RNA-seq数据表征的。从这些数据获得的γ(TRGV)和δ(TRDV)链T细胞受体使用如图10A至图10C所示。
如图10A所示,TRGV9是黑色素瘤中最常用的γ链,占使用量的50%以上。在黑色素瘤肿瘤中还检测到TRGV4、TRGV2、TRGV8、TRGV3和TRGV5表达(图10A)。TRDV2占黑色素瘤肿瘤中γ链使用的60%以上,其中TRDV1(超过25%)和TRDV3(约10%)显示出高使用率(图10A)。TRDV5也在黑色素瘤中显示出可检测的使用(图10A)。这些数据尤其表明Vg9Vd2(γ9δ2)、Vg9Vd1(γ9δ1)和Vg9Vd3(γ9δ3)是黑色素瘤中最常见的γδ受体。
如图10B所示,TRGV9是NSCLC肿瘤中最常用的γ链,占使用量的约75%。在NSCLC肿瘤中还检测到TRGV2、TRGV4、TRGV5、TRGV3和TRGV8表达(图10B)。TRDV1占NSCLC肿瘤中γ链使用的约50%,其中TRDV2(超过30%)和TRDV3(约10%)显示出高使用率(图10B)。TRDV8、TRDV6、TRDV5、TRDV4和TRDV7也在NSCLC肿瘤中显示出可检测的使用(图10B)。这些数据尤其表明Vg9Vd1(γ9δ1)、Vg9Vd2(γ9δ2)和Vg9Vd3(γ9δ3)是NSCLC中最常见的γδ受体。
如图10C所示,TRGV9是结直肠肿瘤中最常用的γ链,占使用量的75%以上。在结直肠肿瘤中还检测到TRGV4、TRGV2、TRGV5、TRGV3和TRGV8表达(图10C)。TRDV1占结直肠肿瘤中γ链使用的约50%,其中TRDV2(约35%)和TRDV3(约10%)显示出高使用率(图10C)。TRDV8、TRDV5、TRDV4、TRDV6和TRDV7也在结直肠肿瘤中显示出可检测的使用(图10C)。这些数据尤其表明Vg9Vd1(γ9δ1)、Vg9Vd2(γ9δ2)和Vg9Vd3(γ9δ3)是结直肠癌中最常见的γδ受体。
通过引用并入
本文引用的所有专利和出版物据此通过引用整体并入本文。
本文所讨论的出版物仅为其在本申请的申请日之前的公开而提供。本文中的任何内容都不应被解释为承认本技术无权凭借在先发明先于这种公开。
如本文所用,所有标题仅用于组织并且不旨在以任何方式限制本公开。任何单独部分的内容可能同样适用于所有部分。
等同方案
虽然已经结合本发明的具体实施方案公开了本发明,但是应当理解,本发明能够进一步修改,并且本申请旨在覆盖本发明的任何变化、使用或修改,所述变化、使用或修改通常遵循本发明的原理,并且包括在本发明所属领域的已知或习惯实践内的对本公开的偏离,并且可以应用于上文阐述的并且在所附权利要求的范围内的基本特征。
所属领域技术人员将认识到或能够仅使用常规实验来确定本文具体公开的具体实施方案的许多等效方案。此类等效方案旨在包含在以下权利要求的范围内。
序列表
<110>沙塔克实验室有限公司(Shattuck Labs Inc.)
<120>鉴定γ/δ T细胞调节剂的方法
<130>SHK-037PC/116981-5037
<150>US 63/173,063
<151>2021-04-09
<150>US 63/116,058
<151>2020-11-19
<160>85
<170>PatentIn version 3.5
<210>1
<211>5
<212>PRT
<213>人工序列
<220>
<223>合成序列
<220>
<221>REPEAT
<222>(1)..(1)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<220>
<221>REPEAT
<222>(2)..(2)
<223>带正电荷的氨基酸,例如精氨酸、组氨酸或赖氨酸
<220>
<221>REPEAT
<222>(3)..(3)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<220>
<221>REPEAT
<222>(4)..(4)
<223>带正电荷的氨基酸,例如精氨酸、组氨酸或赖氨酸
<220>
<221>REPEAT
<222>(5)..(5)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<400>1
Xaa Xaa Xaa Xaa Xaa
1 5
<210>2
<211>5
<212>PRT
<213>人工序列
<220>
<223>合成序列
<220>
<221>REPEAT
<222>(1)..(1)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<220>
<221>REPEAT
<222>(2)..(2)
<223>带负电荷的氨基酸,例如天冬氨酸或谷氨酸
<220>
<221>REPEAT
<222>(3)..(3)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<220>
<221>REPEAT
<222>(4)..(4)
<223>带负电荷的氨基酸,例如天冬氨酸或谷氨酸
<220>
<221>REPEAT
<222>(5)..(5)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<400>2
Xaa Xaa Xaa Xaa Xaa
1 5
<210>3
<211>10
<212>PRT
<213>人工序列
<220>
<223>合成序列
<220>
<221>MISC_FEATURE
<222>(1)..(1)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<220>
<221>REPEAT
<222>(2)..(2)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<220>
<221>MISC_FEATURE
<222>(3)..(3)
<223>带正电荷的氨基酸,例如精氨酸、组氨酸或赖氨酸
<220>
<221>REPEAT
<222>(4)..(4)
<223>带正电荷的氨基酸,例如精氨酸、组氨酸或赖氨酸
<220>
<221>MISC_FEATURE
<222>(5)..(5)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<220>
<221>REPEAT
<222>(6)..(6)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<220>
<221>MISC_FEATURE
<222>(7)..(7)
<223>带正电荷的氨基酸,例如精氨酸、组氨酸或赖氨酸
<220>
<221>REPEAT
<222>(8)..(8)
<223>带正电荷的氨基酸,例如精氨酸、组氨酸或赖氨酸
<220>
<221>MISC_FEATURE
<222>(9)..(9)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<220>
<221>REPEAT
<222>(10)..(10)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<400>3
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10
<210>4
<211>10
<212>PRT
<213>人工序列
<220>
<223>合成序列
<220>
<221>MISC_FEATURE
<222>(1)..(1)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<220>
<221>REPEAT
<222>(2)..(2)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<220>
<221>MISC_FEATURE
<222>(3)..(3)
<223>带负电荷的氨基酸,例如天冬氨酸或谷氨酸
<220>
<221>REPEAT
<222>(4)..(4)
<223>带负电荷的氨基酸,例如天冬氨酸或谷氨酸
<220>
<221>MISC_FEATURE
<222>(5)..(5)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<220>
<221>REPEAT
<222>(6)..(6)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<220>
<221>MISC_FEATURE
<222>(7)..(7)
<223>带负电荷的氨基酸,例如天冬氨酸或谷氨酸
<220>
<221>REPEAT
<222>(8)..(8)
<223>带负电荷的氨基酸,例如天冬氨酸或谷氨酸
<220>
<221>MISC_FEATURE
<222>(9)..(9)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<220>
<221>REPEAT
<222>(10)..(10)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<400>4
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10
<210>5
<211>6
<212>PRT
<213>人工序列
<220>
<223>合成序列
<220>
<221>REPEAT
<222>(1)..(1)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<220>
<221>REPEAT
<222>(2)..(2)
<223>带正电荷的氨基酸,例如精氨酸、组氨酸或赖氨酸
<220>
<221>REPEAT
<222>(4)..(4)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<220>
<221>REPEAT
<222>(5)..(5)
<223>带正电荷的氨基酸,例如精氨酸、组氨酸或赖氨酸
<220>
<221>REPEAT
<222>(6)..(6)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<400>5
Xaa Xaa Cys Xaa Xaa Xaa
1 5
<210>6
<211>6
<212>PRT
<213>人工序列
<220>
<223>合成序列
<220>
<221>REPEAT
<222>(1)..(1)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<220>
<221>REPEAT
<222>(2)..(2)
<223>带负电荷的氨基酸,例如天冬氨酸或谷氨酸
<220>
<221>REPEAT
<222>(4)..(4)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<220>
<221>REPEAT
<222>(5)..(5)
<223>带负电荷的氨基酸,例如天冬氨酸或谷氨酸
<220>
<221>REPEAT
<222>(6)..(6)
<223>间隔氨基酸,例如丝氨酸或甘氨酸
<400>6
Xaa Xaa Cys Xaa Xaa Xaa
1 5
<210>7
<211>12
<212>PRT
<213>人工序列
<220>
<223>合成序列
<400>7
Gly Ser Gly Ser Arg Lys Gly Gly Lys Arg Gly Ser
1 5 10
<210>8
<211>12
<212>PRT
<213>人工序列
<220>
<223>合成序列
<400>8
Gly Ser Gly Ser Arg Lys Cys Gly Lys Arg Gly Ser
1 5 10
<210>9
<211>12
<212>PRT
<213>人工序列
<220>
<223>合成序列
<400>9
Gly Ser Gly Ser Asp Glu Gly Gly Glu Asp Gly Ser
1 5 10
<210>10
<211>12
<212>PRT
<213>人工序列
<220>
<223>合成序列
<400>10
Gly Ser Gly Ser Asp Glu Cys Gly Glu Asp Gly Ser
1 5 10
<210>11
<211>6
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>11
Arg Lys Gly Gly Lys Arg
1 5
<210>12
<211>12
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>12
Gly Ser Gly Ser Arg Lys Gly Gly Lys Arg Gly Ser
1 5 10
<210>13
<211>6
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>13
Asp Glu Gly Gly Glu Asp
1 5
<210>14
<211>12
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>14
Gly Ser Gly Ser Asp Glu Gly Gly Glu Asp Gly Ser
1 5 10
<210>15
<211>234
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>15
Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu
1 5 1015
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Gln Leu
202530
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
354045
Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu
505560
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr
65707580
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Ser
859095
Gly Lys Glu Tyr Lys Cys Lys Val Ser Ser Lys Gly Leu Pro Ser Ser
100 105 110
Ile Glu Lys Thr Ile Ser Asn Ala Thr Gly Gln Pro Arg Glu Pro Gln
115 120 125
Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val
130 135 140
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
145 150 155 160
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
165 170 175
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr
180 185 190
Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val
195 200 205
Leu His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
210 215 220
Ser Leu Gly Lys Ile Glu Gly Arg Met Asp
225 230
<210>16
<211>222
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>16
Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe
1 5 1015
Leu Phe Pro Pro Lys Pro Lys Asp Gln Leu Met Ile Ser Arg Thr Pro
202530
Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val
354045
Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
505560
Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val
65707580
Leu Thr Val Leu His Gln Asp Trp Leu Ser Gly Lys Glu Tyr Lys Cys
859095
Lys Val Ser Ser Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser
100 105 110
Asn Ala Thr Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
115 120 125
Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
130 135 140
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
145 150 155 160
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
165 170 175
Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp
180 185 190
Gln Glu Gly Asn Val Phe Ser Cys Ser Val Leu His Glu Ala Leu His
195 200 205
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
210 215 220
<210>17
<211>232
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>17
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 1015
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
202530
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
354045
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
505560
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
65707580
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
859095
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
100 105 110
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
115 120 125
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
130 135 140
Lys Asn Gln Val Ser Leu Tyr Cys Leu Val Lys Gly Phe Tyr Pro Ser
145 150 155 160
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
165 170 175
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
180 185 190
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
195 200 205
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
210 215 220
Ser Leu Ser Leu Ser Pro Gly Lys
225 230
<210>18
<211>232
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>18
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 1015
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
202530
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
354045
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
505560
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
65707580
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
859095
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
100 105 110
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
115 120 125
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
130 135 140
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
145 150 155 160
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
165 170 175
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Thr
180 185 190
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
195 200 205
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
210 215 220
Ser Leu Ser Leu Ser Pro Gly Lys
225 230
<210>19
<211>227
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>19
Val Pro Arg Asp Cys Gly Cys Lys Pro Cys Ile Cys Thr Val Pro Glu
1 5 1015
Val Ser Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Val Leu Thr
202530
Ile Thr Leu Thr Pro Lys Val Thr Cys Val Val Val Asp Ile Ser Lys
354045
Asp Asp Pro Glu Val Gln Phe Ser Trp Phe Val Asp Asp Val Glu Val
505560
His Thr Ala Gln Thr Gln Pro Arg Glu Glu Gln Phe Asn Ser Thr Phe
65707580
Arg Ser Val Ser Glu Leu Pro Ile Met His Gln Asp Trp Leu Asn Gly
859095
Lys Glu Phe Lys Cys Arg Val Asn Ser Ala Ala Phe Pro Ala Pro Ile
100 105 110
Glu Lys Thr Ile Ser Lys Thr Lys Gly Arg Pro Lys Ala Pro Gln Val
115 120 125
Tyr Thr Ile Pro Pro Pro Lys Glu Gln Met Ala Lys Asp Lys Val Ser
130 135 140
Leu Thr Cys Met Ile Thr Asp Phe Phe Pro Glu Asp Ile Thr Val Glu
145 150 155 160
Trp Gln Trp Asn Gly Gln Pro Ala Glu Asn Tyr Lys Asn Thr Gln Pro
165 170 175
Ile Met Asp Thr Asp Gly Ser Tyr Phe Val Tyr Ser Lys Leu Asn Val
180 185 190
Gln Lys Ser Asn Trp Glu Ala Gly Asn Thr Phe Thr Cys Ser Val Leu
195 200 205
His Glu Gly Leu His Asn His His Thr Glu Lys Ser Leu Ser His Ser
210 215 220
Pro Gly Ile
225
<210>20
<211>249
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>20
Gly Ser Gly Ser Arg Lys Gly Gly Lys Arg Gly Ser Lys Tyr Gly Pro
1 5 1015
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
202530
Phe Leu Phe Pro Pro Lys Pro Lys Asp Gln Leu Met Ile Ser Arg Thr
354045
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
505560
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
65707580
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
859095
Val Leu Thr Val Leu His Gln Asp Trp Leu Ser Gly Lys Glu Tyr Lys
100 105 110
Cys Lys Val Ser Ser Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
115 120 125
Ser Asn Ala Thr Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
130 135 140
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
145 150 155 160
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
165 170 175
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
180 185 190
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
195 200 205
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Leu His Glu Ala Leu
210 215 220
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys Asp
225 230 235 240
Glu Gly Gly Glu Asp Gly Ser Gly Ser
245
<210>21
<211>249
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>21
Gly Ser Gly Ser Asp Glu Gly Gly Glu Asp Gly Ser Lys Tyr Gly Pro
1 5 1015
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
202530
Phe Leu Phe Pro Pro Lys Pro Lys Asp Gln Leu Met Ile Ser Arg Thr
354045
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
505560
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
65707580
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
859095
Val Leu Thr Val Leu His Gln Asp Trp Leu Ser Gly Lys Glu Tyr Lys
100 105 110
Cys Lys Val Ser Ser Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
115 120 125
Ser Asn Ala Thr Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
130 135 140
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
145 150 155 160
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
165 170 175
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
180 185 190
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
195 200 205
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Leu His Glu Ala Leu
210 215 220
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys Arg
225 230 235 240
Lys Gly Gly Lys Arg Gly Ser Gly Ser
245
<210>22
<211>222
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>22
Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe
1 5 1015
Leu Phe Pro Pro Lys Pro Lys Asp Gln Leu Met Ile Ser Arg Thr Pro
202530
Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val
354045
Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
505560
Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val
65707580
Leu Thr Val Leu His Gln Asp Trp Leu Ser Gly Lys Glu Tyr Lys Cys
859095
Lys Val Ser Ser Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser
100 105 110
Asn Ala Thr Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
115 120 125
Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
130 135 140
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
145 150 155 160
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
165 170 175
Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp
180 185 190
Gln Glu Gly Asn Val Phe Ser Cys Ser Val Leu His Glu Ala Leu His
195 200 205
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
210 215 220
<210>23
<400>23
000
<210>24
<211>220
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>24
Gln Phe Ile Val Val Gly Pro Thr Asp Pro Ile Leu Ala Thr Val Gly
1 5 1015
Glu Asn Thr Thr Leu Arg Cys His Leu Ser Pro Glu Lys Asn Ala Glu
202530
Asp Met Glu Val Arg Trp Phe Arg Ser Gln Phe Ser Pro Ala Val Phe
354045
Val Tyr Lys Gly Gly Arg Glu Arg Thr Glu Glu Gln Met Glu Glu Tyr
505560
Arg Gly Arg Thr Thr Phe Val Ser Lys Asp Ile Ser Arg Gly Ser Val
65707580
Ala Leu Val Ile His Asn Ile Thr Ala Gln Glu Asn Gly Thr Tyr Arg
859095
Cys Tyr Phe Gln Glu Gly Arg Ser Tyr Asp Glu Ala Ile Leu His Leu
100 105 110
Val Val Ala Gly Leu Gly Ser Lys Pro Leu Ile Ser Met Arg Gly His
115 120 125
Glu Asp Gly Gly Ile Arg Leu Glu Cys Ile Ser Arg Gly Trp Tyr Pro
130 135 140
Lys Pro Leu Thr Val Trp Arg Asp Pro Tyr Gly Gly Val Ala Pro Ala
145 150 155 160
Leu Lys Glu Val Ser Met Pro Asp Ala Asp Gly Leu Phe Met Val Thr
165 170 175
Thr Ala Val Ile Ile Arg Asp Lys Ser Val Arg Asn Met Ser Cys Ser
180 185 190
Ile Asn Asn Thr Leu Leu Gly Gln Lys Lys Glu Ser Val Ile Phe Ile
195 200 205
Pro Glu Ser Phe Met Pro Ser Val Ser Pro Cys Ala
210 215 220
<210>25
<211>113
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>25
Gln Phe Ile Val Val Gly Pro Thr Asp Pro Ile Leu Ala Thr Val Gly
1 5 1015
Glu Asn Thr Thr Leu Arg Cys His Leu Ser Pro Glu Lys Asn Ala Glu
202530
Asp Met Glu Val Arg Trp Phe Arg Ser Gln Phe Ser Pro Ala Val Phe
354045
Val Tyr Lys Gly Gly Arg Glu Arg Thr Glu Glu Gln Met Glu Glu Tyr
505560
Arg Gly Arg Thr Thr Phe Val Ser Lys Asp Ile Ser Arg Gly Ser Val
65707580
Ala Leu Val Ile His Asn Ile Thr Ala Gln Glu Asn Gly Thr Tyr Arg
859095
Cys Tyr Phe Gln Glu Gly Arg Ser Tyr Asp Glu Ala Ile Leu His Leu
100 105 110
Val
<210>26
<211>225
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>26
Gln Phe Ser Val Leu Gly Pro Ser Gly Pro Ile Leu Ala Met Val Gly
1 5 1015
Glu Asp Ala Asp Leu Pro Cys His Leu Phe Pro Thr Met Ser Ala Glu
202530
Thr Met Glu Leu Lys Trp Val Ser Ser Ser Leu Arg Gln Val Val Asn
354045
Val Tyr Ala Asp Gly Lys Glu Val Glu Asp Arg Gln Ser Ala Pro Tyr
505560
Arg Gly Arg Thr Ser Ile Leu Arg Asp Gly Ile Thr Ala Gly Lys Ala
65707580
Ala Leu Arg Ile His Asn Val Thr Ala Ser Asp Ser Gly Lys Tyr Leu
859095
Cys Tyr Phe Gln Asp Gly Asp Phe Tyr Glu Lys Ala Leu Val Glu Leu
100 105 110
Lys Val Ala Ala Leu Gly Ser Asp Leu His Val Asp Val Lys Gly Tyr
115 120 125
Lys Asp Gly Gly Ile His Leu Glu Cys Arg Ser Thr Gly Trp Tyr Pro
130 135 140
Gln Pro Gln Ile Gln Trp Ser Asn Asn Lys Gly Glu Asn Ile Pro Thr
145 150 155 160
Val Glu Ala Pro Val Val Ala Asp Gly Val Gly Leu Tyr Ala Val Ala
165 170 175
Ala Ser Val Ile Met Arg Gly Ser Ser Gly Glu Gly Val Ser Cys Thr
180 185 190
Ile Arg Ser Ser Leu Leu Gly Leu Glu Lys Thr Ala Ser Ile Ser Ile
195 200 205
Ala Asp Pro Phe Phe Arg Ser Ala Gln Arg Trp Ile Ala Ala Leu Ala
210 215 220
Gly
225
<210>27
<211>115
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>27
Gln Phe Ser Val Leu Gly Pro Ser Gly Pro Ile Leu Ala Met Val Gly
1 5 1015
Glu Asp Ala Asp Leu Pro Cys His Leu Phe Pro Thr Met Ser Ala Glu
202530
Thr Met Glu Leu Lys Trp Val Ser Ser Ser Leu Arg Gln Val Val Asn
354045
Val Tyr Ala Asp Gly Lys Glu Val Glu Asp Arg Gln Ser Ala Pro Tyr
505560
Arg Gly Arg Thr Ser Ile Leu Arg Asp Gly Ile Thr Ala Gly Lys Ala
65707580
Ala Leu Arg Ile His Asn Val Thr Ala Ser Asp Ser Gly Lys Tyr Leu
859095
Cys Tyr Phe Gln Asp Gly Asp Phe Tyr Glu Lys Ala Leu Val Glu Leu
100 105 110
Lys Val Ala
115
<210>28
<211>223
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>28
Glu Val Ser Trp Phe Ser Val Lys Gly Pro Ala Glu Pro Ile Thr Val
1 5 1015
Leu Leu Gly Thr Glu Ala Thr Leu Pro Cys Gln Leu Ser Pro Glu Gln
202530
Ser Ala Ala Arg Met His Ile Arg Trp Tyr Arg Ala Gln Pro Thr Pro
354045
Ala Val Leu Val Phe His Asn Gly Gln Glu Gln Gly Glu Val Gln Met
505560
Pro Glu Tyr Arg Gly Arg Thr Gln Met Val Arg Gln Ala Ile Asp Met
65707580
Gly Ser Val Ala Leu Gln Ile Gln Gln Val Gln Ala Ser Asp Asp Gly
859095
Leu Tyr His Cys Gln Phe Thr Asp Gly Phe Thr Ser Gln Glu Val Ser
100 105 110
Met Glu Leu Arg Val Ile Gly Leu Gly Ser Ala Pro Leu Val His Met
115 120 125
Thr Gly Pro Glu Asn Asp Gly Ile Arg Val Leu Cys Ser Ser Ser Gly
130 135 140
Trp Phe Pro Lys Pro Lys Val Gln Trp Arg Asp Thr Ser Gly Asn Met
145 150 155 160
Leu Leu Ser Ser Ser Glu Leu Gln Thr Gln Asp Arg Glu Gly Leu Phe
165 170 175
Gln Val Glu Val Ser Leu Leu Val Thr Asp Arg Ala Ile Gly Asn Val
180 185 190
Ile Cys Ser Ile Gln Asn Pro Met Tyr Asp Gln Glu Lys Ser Lys Ala
195 200 205
Ile Leu Leu Pro Glu Pro Phe Phe Pro Lys Thr Cys Pro Trp Lys
210 215 220
<210>29
<211>163
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>29
Glu Gln Leu Pro Glu Tyr Ser Gln Arg Thr Ser Leu Val Lys Glu Gln
1 5 1015
Phe His Gln Gly Thr Ala Ala Val Arg Ile Leu Asn Val Gln Ala Pro
202530
Asp Ser Gly Ile Tyr Ile Cys His Phe Lys Gln Gly Val Phe Tyr Glu
354045
Glu Ala Ile Leu Glu Leu Lys Val Ala Ala Met Gly Ser Val Pro Glu
505560
Val Tyr Ile Lys Gly Pro Glu Asp Gly Gly Val Cys Val Val Cys Ile
65707580
Thr Ser Gly Trp Tyr Pro Glu Pro Gln Val His Trp Lys Asp Ser Arg
859095
Gly Glu Lys Leu Thr Ala Ser Leu Glu Ile His Ser Glu Asp Ala Gln
100 105 110
Gly Leu Phe Arg Thr Glu Thr Ser Leu Val Val Arg Asp Ser Ser Val
115 120 125
Arg Asn Val Thr Cys Ser Thr Phe Asn Pro Ile Leu Gly Gln Glu Lys
130 135 140
Ala Met Ala Met Phe Leu Pro Glu Pro Phe Phe Pro Lys Val Ser Pro
145 150 155 160
Trp Lys Pro
<210>30
<211>220
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>30
Gln Trp Gln Val Thr Gly Pro Gly Lys Phe Val Gln Ala Leu Val Gly
1 5 1015
Glu Asp Ala Val Phe Ser Cys Ser Leu Phe Pro Glu Thr Ser Ala Glu
202530
Ala Met Glu Val Arg Phe Phe Arg Asn Gln Phe His Ala Val Val His
354045
Leu Tyr Arg Asp Gly Glu Asp Trp Glu Ser Lys Gln Met Pro Gln Tyr
505560
Arg Gly Arg Thr Glu Phe Val Lys Asp Ser Ile Ala Gly Gly Arg Val
65707580
Ser Leu Arg Leu Lys Asn Ile Thr Pro Ser Asp Ile Gly Leu Tyr Gly
859095
Cys Trp Phe Ser Ser Gln Ile Tyr Asp Glu Glu Ala Thr Trp Glu Leu
100 105 110
Arg Val Ala Ala Leu Gly Ser Leu Pro Leu Ile Ser Ile Val Gly Tyr
115 120 125
Val Asp Gly Gly Ile Gln Leu Leu Cys Leu Ser Ser Gly Trp Phe Pro
130 135 140
Gln Pro Thr Ala Lys Trp Lys Gly Pro Gln Gly Gln Asp Leu Ser Ser
145 150 155 160
Asp Ser Arg Ala Asn Ala Asp Gly Tyr Ser Leu Tyr Asp Val Glu Ile
165 170 175
Ser Ile Ile Val Gln Glu Asn Ala Gly Ser Ile Leu Cys Ser Ile His
180 185 190
Leu Ala Glu Gln Ser His Glu Val Glu Ser Lys Val Leu Ile Gly Glu
195 200 205
Thr Phe Phe Gln Pro Ser Pro Trp Arg Leu Ala Ser
210 215 220
<210>31
<211>219
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>31
Gln Phe Ser Val Leu Gly Pro Ser Gly Pro Ile Leu Ala Met Val Gly
1 5 1015
Glu Asp Ala Asp Leu Pro Cys His Leu Phe Pro Thr Met Ser Ala Glu
202530
Thr Met Glu Leu Lys Trp Val Ser Ser Ser Leu Arg Gln Val Val Asn
354045
Val Tyr Ala Asp Gly Lys Glu Val Glu Asp Arg Gln Ser Ala Pro Tyr
505560
Arg Gly Arg Thr Ser Ile Leu Arg Asp Gly Ile Thr Ala Gly Lys Ala
65707580
Ala Leu Arg Ile His Asn Val Thr Ala Ser Asp Ser Gly Lys Tyr Leu
859095
Cys Tyr Phe Gln Asp Gly Asp Phe Tyr Glu Lys Ala Leu Val Glu Leu
100 105 110
Lys Val Ala Ala Leu Gly Ser Asn Leu His Val Glu Val Lys Gly Tyr
115 120 125
Glu Asp Gly Gly Ile His Leu Glu Cys Arg Ser Thr Gly Trp Tyr Pro
130 135 140
Gln Pro Gln Ile Gln Trp Ser Asn Ala Lys Gly Glu Asn Ile Pro Ala
145 150 155 160
Val Glu Ala Pro Val Val Ala Asp Gly Val Gly Leu Tyr Glu Val Ala
165 170 175
Ala Ser Val Ile Met Arg Gly Gly Ser Gly Glu Gly Val Ser Cys Ile
180 185 190
Ile Arg Asn Ser Leu Leu Gly Leu Glu Lys Thr Ala Ser Ile Ser Ile
195 200 205
Ala Asp Pro Phe Phe Arg Ser Ala Gln Pro Trp
210 215
<210>32
<211>221
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>32
Gln Trp Gln Val Phe Gly Pro Asp Lys Pro Val Gln Ala Leu Val Gly
1 5 1015
Glu Asp Ala Ala Phe Ser Cys Phe Leu Ser Pro Lys Thr Asn Ala Glu
202530
Ala Met Glu Val Arg Phe Phe Arg Gly Gln Phe Ser Ser Val Val His
354045
Leu Tyr Arg Asp Gly Lys Asp Gln Pro Phe Met Gln Met Pro Gln Tyr
505560
Gln Gly Arg Thr Lys Leu Val Lys Asp Ser Ile Ala Glu Gly Arg Ile
65707580
Ser Leu Arg Leu Glu Asn Ile Thr Val Leu Asp Ala Gly Leu Tyr Gly
859095
Cys Arg Ile Ser Ser Gln Ser Tyr Tyr Gln Lys Ala Ile Trp Glu Leu
100 105 110
Gln Val Ser Ala Leu Gly Ser Val Pro Leu Ile Ser Ile Thr Gly Tyr
115 120 125
Val Asp Arg Asp Ile Gln Leu Leu Cys Gln Ser Ser Gly Trp Phe Pro
130 135 140
Arg Pro Thr Ala Lys Trp Lys Gly Pro Gln Gly Gln Asp Leu Ser Thr
145 150 155 160
Asp Ser Arg Thr Asn Arg Asp Met His Gly Leu Phe Asp Val Glu Ile
165 170 175
Ser Leu Thr Val Gln Glu Asn Ala Gly Ser Ile Ser Cys Ser Met Arg
180 185 190
His Ala His Leu Ser Arg Glu Val Glu Ser Arg Val Gln Ile Gly Asp
195 200 205
Thr Phe Phe Glu Pro Ile Ser Trp His Leu Ala Thr Lys
210 215 220
<210>33
<211>216
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>33
Ala Pro Phe Asp Val Ile Gly Pro Pro Glu Pro Ile Leu Ala Val Val
1 5 1015
Gly Glu Asp Ala Glu Leu Pro Cys Arg Leu Ser Pro Asn Ala Ser Ala
202530
Glu His Leu Glu Leu Arg Trp Phe Arg Lys Lys Val Ser Pro Ala Val
354045
Leu Val His Arg Asp Gly Arg Glu Gln Glu Ala Glu Gln Met Pro Glu
505560
Tyr Arg Gly Arg Ala Thr Leu Val Gln Asp Gly Ile Ala Lys Gly Arg
65707580
Val Ala Leu Arg Ile Arg Gly Val Arg Val Ser Asp Asp Gly Glu Tyr
859095
Thr Cys Phe Phe Arg Glu Asp Gly Ser Tyr Glu Glu Ala Leu Val His
100 105 110
Leu Lys Val Ala Ala Leu Gly Ser Asp Pro His Ile Ser Met Gln Val
115 120 125
Gln Glu Asn Gly Glu Ile Cys Leu Glu Cys Thr Ser Val Gly Trp Tyr
130 135 140
Pro Glu Pro Gln Val Gln Trp Arg Thr Ser Lys Gly Glu Lys Phe Pro
145 150 155 160
Ser Thr Ser Glu Ser Arg Asn Pro Asp Glu Glu Gly Leu Phe Thr Val
165 170 175
Ala Ala Ser Val Ile Ile Arg Asp Thr Ser Ala Lys Asn Val Ser Cys
180 185 190
Tyr Ile Gln Asn Leu Leu Leu Gly Gln Glu Lys Lys Val Glu Ile Ser
195 200 205
Ile Pro Ala Ser Ser Leu Pro Arg
210 215
<210>34
<211>215
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>34
Ala Pro Phe Asp Val Ile Gly Pro Pro Glu Pro Ile Leu Ala Val Val
1 5 1015
Gly Glu Asp Ala Glu Leu Pro Cys Arg Leu Ser Pro Asn Ala Ser Ala
202530
Glu His Leu Glu Leu Arg Trp Phe Arg Lys Lys Val Ser Pro Ala Val
354045
Leu Val His Arg Asp Gly Arg Glu Gln Glu Ala Glu Gln Met Pro Glu
505560
Tyr Arg Gly Arg Ala Thr Leu Val Gln Asp Gly Ile Ala Lys Gly Arg
65707580
Val Ala Leu Arg Ile Arg Gly Val Arg Val Ser Asp Asp Gly Glu Tyr
859095
Thr Cys Phe Phe Arg Glu Asp Gly Ser Tyr Glu Glu Ala Leu Val His
100 105 110
Leu Lys Val Ala Ala Leu Gly Ser Asp Pro His Ile Ser Met Gln Val
115 120 125
Gln Glu Asn Gly Glu Ile Cys Leu Glu Cys Thr Ser Val Gly Trp Tyr
130 135 140
Pro Glu Pro Gln Val Gln Trp Arg Thr Ser Lys Gly Glu Lys Phe Pro
145 150 155 160
Ser Thr Ser Glu Ser Arg Asn Pro Asp Glu Glu Gly Leu Phe Thr Val
165 170 175
Ala Ala Ser Val Ile Ile Arg Asp Thr Ser Ala Lys Asn Val Ser Cys
180 185 190
Tyr Ile Gln Asn Leu Leu Leu Gly Gln Glu Lys Lys Val Glu Ile Ser
195 200 205
Ile Pro Ala Ser Ser Leu Pro
210 215
<210>35
<211>432
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>35
Lys Gln Ser Glu Asp Phe Arg Val Ile Gly Pro Ala His Pro Ile Leu
1 5 1015
Ala Gly Val Gly Glu Asp Ala Leu Leu Thr Cys Gln Leu Leu Pro Lys
202530
Arg Thr Thr Met His Val Glu Val Arg Trp Tyr Arg Ser Glu Pro Ser
354045
Thr Pro Val Phe Val His Arg Asp Gly Val Glu Val Thr Glu Met Gln
505560
Met Glu Glu Tyr Arg Gly Trp Val Glu Trp Ile Glu Asn Gly Ile Ala
65707580
Lys Gly Asn Val Ala Leu Lys Ile His Asn Ile Gln Pro Ser Asp Asn
859095
Gly Gln Tyr Trp Cys His Phe Gln Asp Gly Asn Tyr Cys Gly Glu Thr
100 105 110
Ser Leu Leu Leu Lys Val Ala Gly Leu Gly Ser Ala Pro Ser Ile His
115 120 125
Met Glu Gly Pro Gly Glu Ser Gly Val Gln Leu Val Cys Thr Ala Arg
130 135 140
Gly Trp Phe Pro Glu Pro Gln Val Tyr Trp Glu Asp Ile Arg Gly Glu
145 150 155 160
Lys Leu Leu Ala Val Ser Glu His Arg Ile Gln Asp Lys Asp Gly Leu
165 170 175
Phe Tyr Ala Glu Ala Thr Leu Val Val Arg Asn Ala Ser Ala Glu Ser
180 185 190
Val Ser Cys Leu Val His Asn Pro Val Leu Thr Glu Glu Lys Gly Ser
195 200 205
Val Ile Ser Leu Pro Glu Lys Leu Gln Thr Glu Leu Ala Ser Leu Lys
210 215 220
Val Asn Gly Pro Ser Gln Pro Ile Leu Val Arg Val Gly Glu Asp Ile
225 230 235 240
Gln Leu Thr Cys Tyr Leu Ser Pro Lys Ala Asn Ala Gln Ser Met Glu
245 250 255
Val Arg Trp Asp Arg Ser His Arg Tyr Pro Ala Val His Val Tyr Met
260 265 270
Asp Gly Asp His Val Ala Gly Glu Gln Met Ala Glu Tyr Arg Gly Arg
275 280 285
Thr Val Leu Val Ser Asp Ala Ile Asp Glu Gly Arg Leu Thr Leu Gln
290 295 300
Ile Leu Ser Ala Arg Pro Ser Asp Asp Gly Gln Tyr Arg Cys Leu Phe
305 310 315 320
Glu Lys Asp Asp Val Tyr Gln Glu Ala Ser Leu Asp Leu Lys Val Val
325 330 335
Ser Leu Gly Ser Ser Pro Leu Ile Thr Val Glu Gly Gln Glu Asp Gly
340 345 350
Glu Met Gln Pro Met Cys Ser Ser Asp Gly Trp Phe Pro Gln Pro His
355 360 365
Val Pro Trp Arg Asp Met Glu Gly Lys Thr Ile Pro Ser Ser Ser Gln
370 375 380
Ala Leu Thr Gln Gly Ser His Gly Leu Phe His Val Gln Thr Leu Leu
385 390 395 400
Arg Val Thr Asn Ile Ser Ala Val Asp Val Thr Cys Ser Ile Ser Ile
405 410 415
Pro Phe Leu Gly Glu Glu Lys Ile Ala Thr Phe Ser Leu Ser Gly Trp
420 425 430
<210>36
<211>220
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>36
Gln Phe Ile Val Val Gly Pro Thr Asp Pro Ile Leu Ala Thr Val Gly
1 5 1015
Glu Asn Thr Thr Leu Arg Cys His Leu Ser Pro Glu Lys Asn Ala Glu
202530
Asp Met Glu Val Arg Trp Phe Arg Ser Gln Phe Ser Pro Ala Val Phe
354045
Val Tyr Lys Gly Gly Arg Glu Arg Thr Glu Glu Gln Met Glu Glu Tyr
505560
Arg Gly Arg Thr Thr Phe Val Ser Lys Asp Ile Ser Arg Gly Ser Val
65707580
Ala Leu Val Ile His Asn Ile Thr Ala Gln Glu Asn Gly Thr Tyr Arg
859095
Cys Tyr Phe Gln Glu Gly Arg Ser Tyr Asp Glu Ala Ile Leu His Leu
100 105 110
Val Val Ala Gly Leu Gly Ser Lys Pro Leu Ile Ser Met Arg Gly His
115 120 125
Glu Asp Gly Gly Ile Arg Leu Glu Cys Ile Ser Arg Gly Trp Tyr Pro
130 135 140
Lys Pro Leu Thr Val Trp Arg Asp Pro Tyr Gly Gly Val Ala Pro Ala
145 150 155 160
Leu Lys Glu Val Ser Met Pro Asp Ala Asp Gly Leu Phe Met Val Thr
165 170 175
Thr Ala Val Ile Ile Arg Asp Lys Ser Val Arg Asn Met Ser Cys Ser
180 185 190
Ile Asn Asn Thr Leu Leu Gly Gln Lys Lys Glu Ser Val Ile Phe Ile
195 200 205
Pro Glu Ser Phe Met Pro Ser Val Ser Pro Cys Ala
210 215 220
<210>37
<211>233
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>37
Gln Phe Thr Val Val Gly Pro Ala Asn Pro Ile Leu Ala Met Val Gly
1 5 1015
Glu Asn Thr Thr Leu Arg Cys His Leu Ser Pro Glu Lys Asn Ala Glu
202530
Asp Met Glu Val Arg Trp Phe Arg Ser Gln Phe Ser Pro Ala Val Phe
354045
Val Tyr Lys Gly Gly Arg Glu Arg Thr Glu Glu Gln Met Glu Glu Tyr
505560
Arg Gly Arg Ile Thr Phe Val Ser Lys Asp Ile Asn Arg Gly Ser Val
65707580
Ala Leu Val Ile His Asn Val Thr Ala Gln Glu Asn Gly Ile Tyr Arg
859095
Cys Tyr Phe Gln Glu Gly Arg Ser Tyr Asp Glu Ala Ile Leu Arg Leu
100 105 110
Val Val Ala Gly Leu Gly Ser Lys Pro Leu Ile Glu Ile Lys Ala Gln
115 120 125
Glu Asp Gly Ser Ile Trp Leu Glu Cys Ile Ser Gly Gly Trp Tyr Pro
130 135 140
Glu Pro Leu Thr Val Trp Arg Asp Pro Tyr Gly Glu Val Val Pro Ala
145 150 155 160
Leu Lys Glu Val Ser Ile Ala Asp Ala Asp Gly Leu Phe Met Val Thr
165 170 175
Thr Ala Val Ile Ile Arg Asp Lys Tyr Val Arg Asn Val Ser Cys Ser
180 185 190
Val Asn Asn Thr Leu Leu Gly Gln Glu Lys Glu Thr Val Ile Phe Ile
195 200 205
Pro Glu Ser Phe Met Pro Ser Ala Ser Pro Trp Met Val Ala Leu Ala
210 215 220
Val Ile Leu Thr Ala Ser Pro Trp Met
225 230
<210>38
<211>219
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>38
Gln Val Thr Val Val Gly Pro Thr Asp Pro Ile Leu Ala Met Val Gly
1 5 1015
Glu Asn Thr Thr Leu Arg Cys Cys Leu Ser Pro Glu Glu Asn Ala Glu
202530
Asp Met Glu Val Arg Trp Phe Gln Ser Gln Phe Ser Pro Ala Val Phe
354045
Val Tyr Lys Gly Gly Arg Glu Arg Thr Glu Glu Gln Lys Glu Glu Tyr
505560
Arg Gly Arg Thr Thr Phe Val Ser Lys Asp Ser Arg Gly Ser Val Ala
65707580
Leu Ile Ile His Asn Val Thr Ala Glu Asp Asn Gly Ile Tyr Gln Cys
859095
Tyr Phe Gln Glu Gly Arg Ser Cys Asn Glu Ala Ile Leu His Leu Val
100 105 110
Val Ala Gly Leu Asp Ser Glu Pro Val Ile Glu Met Arg Asp His Glu
115 120 125
Asp Gly Gly Ile Gln Leu Glu Cys Ile Ser Gly Gly Trp Tyr Pro Lys
130 135 140
Pro Leu Thr Val Trp Arg Asp Pro Tyr Gly Glu Val Val Pro Ala Leu
145 150 155 160
Lys Glu Val Ser Thr Pro Asp Ala Asp Ser Leu Phe Met Val Thr Thr
165 170 175
Ala Val Ile Ile Arg Asp Lys Ser Val Arg Asn Val Ser Cys Ser Ile
180 185 190
Asn Asp Thr Leu Leu Gly Gln Lys Lys Glu Ser Val Ile Phe Ile Pro
195 200 205
Glu Ser Phe Met Pro Ser Arg Ser Pro Cys Val
210 215
<210>39
<211>220
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>39
Gln Trp Gln Val Thr Gly Pro Gly Lys Phe Val Gln Ala Leu Val Gly
1 5 1015
Glu Asp Ala Val Phe Ser Cys Ser Leu Phe Pro Glu Thr Ser Ala Glu
202530
Ala Met Glu Val Arg Phe Phe Arg Asn Gln Phe His Ala Val Val His
354045
Leu Tyr Arg Asp Gly Glu Asp Trp Glu Ser Lys Gln Met Pro Gln Tyr
505560
Arg Gly Arg Thr Glu Phe Val Lys Asp Ser Ile Ala Gly Gly Arg Val
65707580
Ser Leu Arg Leu Lys Asn Ile Thr Pro Ser Asp Ile Gly Leu Tyr Gly
859095
Cys Trp Phe Ser Ser Gln Ile Tyr Asp Glu Glu Ala Thr Trp Glu Leu
100 105 110
Arg Val Ala Ala Leu Gly Ser Leu Pro Leu Ile Ser Ile Val Gly Tyr
115 120 125
Val Asp Gly Gly Ile Gln Leu Leu Cys Leu Ser Ser Gly Trp Phe Pro
130 135 140
Gln Pro Thr Ala Lys Trp Lys Gly Pro Gln Gly Gln Asp Leu Ser Ser
145 150 155 160
Asp Ser Arg Ala Asn Ala Asp Gly Tyr Ser Leu Tyr Asp Val Glu Ile
165 170 175
Ser Ile Ile Val Gln Glu Asn Ala Gly Ser Ile Leu Cys Ser Ile His
180 185 190
Leu Ala Glu Gln Ser His Glu Val Glu Ser Lys Val Leu Ile Gly Glu
195 200 205
Thr Phe Phe Gln Pro Ser Pro Trp Arg Leu Ala Ser
210 215 220
<210>40
<211>225
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>40
Gln Phe Ser Val Leu Gly Pro Ser Gly Pro Ile Leu Ala Met Val Gly
1 5 1015
Glu Asp Ala Asp Leu Pro Cys His Leu Phe Pro Thr Met Ser Ala Glu
202530
Thr Met Glu Leu Lys Trp Val Ser Ser Ser Leu Arg Gln Val Val Asn
354045
Val Tyr Ala Asp Gly Lys Glu Val Glu Asp Arg Gln Ser Ala Pro Tyr
505560
Arg Gly Arg Thr Ser Ile Leu Arg Asp Gly Ile Thr Ala Gly Lys Ala
65707580
Ala Leu Arg Ile His Asn Val Thr Ala Ser Asp Ser Gly Lys Tyr Leu
859095
Cys Tyr Phe Gln Asp Gly Asp Phe Tyr Glu Lys Ala Leu Val Glu Leu
100 105 110
Lys Val Ala Ala Leu Gly Ser Asp Leu His Val Asp Val Lys Gly Tyr
115 120 125
Lys Asp Gly Gly Ile His Leu Glu Cys Arg Ser Thr Gly Trp Tyr Pro
130 135 140
Gln Pro Gln Ile Gln Trp Ser Asn Asn Lys Gly Glu Asn Ile Pro Thr
145 150 155 160
Val Glu Ala Pro Val Val Ala Asp Gly Val Gly Leu Tyr Ala Val Ala
165 170 175
Ala Ser Val Ile Met Arg Gly Ser Ser Gly Glu Gly Val Ser Cys Thr
180 185 190
Ile Arg Ser Ser Leu Leu Gly Leu Glu Lys Thr Ala Ser Ile Ser Ile
195 200 205
Ala Asp Pro Phe Phe Arg Ser Ala Gln Arg Trp Ile Ala Ala Leu Ala
210 215 220
Gly
225
<210>41
<211>219
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>41
Gln Phe Ser Val Leu Gly Pro Ser Gly Pro Ile Leu Ala Met Val Gly
1 5 1015
Glu Asp Ala Asp Leu Pro Cys His Leu Phe Pro Thr Met Ser Ala Glu
202530
Thr Met Glu Leu Lys Trp Val Ser Ser Ser Leu Arg Gln Val Val Asn
354045
Val Tyr Ala Asp Gly Lys Glu Val Glu Asp Arg Gln Ser Ala Pro Tyr
505560
Arg Gly Arg Thr Ser Ile Leu Arg Asp Gly Ile Thr Ala Gly Lys Ala
65707580
Ala Leu Arg Ile His Asn Val Thr Ala Ser Asp Ser Gly Lys Tyr Leu
859095
Cys Tyr Phe Gln Asp Gly Asp Phe Tyr Glu Lys Ala Leu Val Glu Leu
100 105 110
Lys Val Ala Ala Leu Gly Ser Asn Leu His Val Glu Val Lys Gly Tyr
115 120 125
Glu Asp Gly Gly Ile His Leu Glu Cys Arg Ser Thr Gly Trp Tyr Pro
130 135 140
Gln Pro Gln Ile Gln Trp Ser Asn Ala Lys Gly Glu Asn Ile Pro Ala
145 150 155 160
Val Glu Ala Pro Val Val Ala Asp Gly Val Gly Leu Tyr Glu Val Ala
165 170 175
Ala Ser Val Ile Met Arg Gly Gly Ser Gly Glu Gly Val Ser Cys Ile
180 185 190
Ile Arg Asn Ser Leu Leu Gly Leu Glu Lys Thr Ala Ser Ile Ser Ile
195 200 205
Ala Asp Pro Phe Phe Arg Ser Ala Gln Pro Trp
210 215
<210>42
<211>219
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>42
Gln Phe Ser Val Leu Gly Pro Ser Gly Pro Ile Leu Ala Met Val Gly
1 5 1015
Glu Asp Ala Asp Leu Pro Cys His Leu Phe Pro Thr Met Ser Ala Glu
202530
Thr Met Glu Leu Arg Trp Val Ser Ser Ser Leu Arg Gln Val Val Asn
354045
Val Tyr Ala Asp Gly Lys Glu Val Glu Asp Arg Gln Ser Ala Pro Tyr
505560
Arg Gly Arg Thr Ser Ile Leu Arg Asp Gly Ile Thr Ala Gly Lys Ala
65707580
Ala Leu Arg Ile His Asn Val Thr Ala Ser Asp Ser Gly Lys Tyr Leu
859095
Cys Tyr Phe Gln Asp Gly Asp Phe Tyr Glu Lys Ala Leu Val Glu Leu
100 105 110
Lys Val Ala Ala Leu Gly Ser Asp Leu His Ile Glu Val Lys Gly Tyr
115 120 125
Glu Asp Gly Gly Ile His Leu Glu Cys Arg Ser Thr Gly Trp Tyr Pro
130 135 140
Gln Pro Gln Ile Lys Trp Ser Asp Thr Lys Gly Glu Asn Ile Pro Ala
145 150 155 160
Val Glu Ala Pro Val Val Ala Asp Gly Val Gly Leu Tyr Ala Val Ala
165 170 175
Ala Ser Val Ile Met Arg Gly Ser Ser Gly Gly Gly Val Ser Cys Ile
180 185 190
Ile Arg Asn Ser Leu Leu Gly Leu Glu Lys Thr Ala Ser Ile Ser Ile
195 200 205
Ala Asp Pro Phe Phe Arg Ser Ala Gln Pro Trp
210 215
<210>43
<211>221
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>43
Gln Trp Gln Val Phe Gly Pro Asp Lys Pro Val Gln Ala Leu Val Gly
1 5 1015
Glu Asp Ala Ala Phe Ser Cys Phe Leu Ser Pro Lys Thr Asn Ala Glu
202530
Ala Met Glu Val Arg Phe Phe Arg Gly Gln Phe Ser Ser Val Val His
354045
Leu Tyr Arg Asp Gly Lys Asp Gln Pro Phe Met Gln Met Pro Gln Tyr
505560
Gln Gly Arg Thr Lys Leu Val Lys Asp Ser Ile Ala Glu Gly Arg Ile
65707580
Ser Leu Arg Leu Glu Asn Ile Thr Val Leu Asp Ala Gly Leu Tyr Gly
859095
Cys Arg Ile Ser Ser Gln Ser Tyr Tyr Gln Lys Ala Ile Trp Glu Leu
100 105 110
Gln Val Ser Ala Leu Gly Ser Val Pro Leu Ile Ser Ile Thr Gly Tyr
115 120 125
Val Asp Arg Asp Ile Gln Leu Leu Cys Gln Ser Ser Gly Trp Phe Pro
130 135 140
Arg Pro Thr Ala Lys Trp Lys Gly Pro Gln Gly Gln Asp Leu Ser Thr
145 150 155 160
Asp Ser Arg Thr Asn Arg Asp Met His Gly Leu Phe Asp Val Glu Ile
165 170 175
Ser Leu Thr Val Gln Glu Asn Ala Gly Ser Ile Ser Cys Ser Met Arg
180 185 190
His Ala His Leu Ser Arg Glu Val Glu Ser Arg Val Gln Ile Gly Asp
195 200 205
Thr Phe Phe Glu Pro Ile Ser Trp His Leu Ala Thr Lys
210 215 220
<210>44
<211>222
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>44
Ser Ser Glu Val Lys Val Leu Gly Pro Glu Tyr Pro Ile Leu Ala Leu
1 5 1015
Val Gly Glu Glu Val Glu Phe Pro Cys His Leu Trp Pro Gln Leu Asp
202530
Ala Gln Gln Met Glu Ile Arg Trp Phe Arg Ser Gln Thr Phe Asn Val
354045
Val His Leu Tyr Gln Glu Gln Gln Glu Leu Pro Gly Arg Gln Met Pro
505560
Ala Phe Arg Asn Arg Thr Lys Leu Val Lys Asp Asp Ile Ala Tyr Gly
65707580
Ser Val Val Leu Gln Leu His Ser Ile Ile Pro Ser Asp Lys Gly Thr
859095
Tyr Gly Cys Arg Phe His Ser Asp Asn Phe Ser Gly Glu Ala Leu Trp
100 105 110
Glu Leu Glu Val Ala Gly Leu Gly Ser Asp Pro His Leu Ser Leu Glu
115 120 125
Gly Phe Lys Glu Gly Gly Ile Gln Leu Arg Leu Arg Ser Ser Gly Trp
130 135 140
Tyr Pro Lys Pro Lys Val Gln Trp Arg Asp His Gln Gly Gln Cys Leu
145 150 155 160
Pro Pro Glu Phe Glu Ala Ile Val Trp Asp Ala Gln Asp Leu Phe Ser
165 170 175
Leu Glu Thr Ser Val Val Val Arg Ala Gly Ala Leu Ser Asn Val Ser
180 185 190
Val Ser Ile Gln Asn Leu Leu Leu Ser Gln Lys Lys Glu Leu Val Val
195 200 205
Gln Ile Ala Asp Val Phe Val Pro Gly Ala Ser Ala Trp Lys
210 215 220
<210>45
<211>228
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>45
Ser Ile Trp Lys Ala Asp Phe Asp Val Thr Gly Pro His Ala Pro Ile
1 5 1015
Leu Ala Met Ala Gly Gly His Val Glu Leu Gln Cys Gln Leu Phe Pro
202530
Asn Ile Ser Ala Glu Asp Met Glu Leu Arg Trp Tyr Arg Cys Gln Pro
354045
Ser Leu Ala Val His Met His Glu Arg Gly Met Asp Met Asp Gly Glu
505560
Gln Lys Trp Gln Tyr Arg Gly Arg Thr Thr Phe Met Ser Asp His Val
65707580
Ala Arg Gly Lys Ala Met Val Arg Ser His Arg Val Thr Thr Phe Asp
859095
Asn Arg Thr Tyr Cys Cys Arg Phe Lys Asp Gly Val Lys Phe Gly Glu
100 105 110
Ala Thr Val Gln Val Gln Val Ala Gly Leu Gly Arg Glu Pro Arg Ile
115 120 125
Gln Val Thr Asp Gln Gln Asp Gly Val Arg Ala Glu Cys Thr Ser Ala
130 135 140
Gly Cys Phe Pro Lys Ser Trp Val Glu Arg Arg Asp Phe Arg Gly Gln
145 150 155 160
Ala Arg Pro Ala Val Thr Asn Leu Ser Ala Ser Ala Thr Thr Arg Leu
165 170 175
Trp Ala Val Ala Ser Ser Leu Thr Leu Trp Asp Arg Ala Val Glu Gly
180 185 190
Leu Ser Cys Ser Ile Ser Ser Pro Leu Leu Pro Glu Arg Arg Lys Val
195 200 205
Ala Glu Ser His Leu Pro Ala Thr Phe Ser Arg Ser Ser Gln Phe Thr
210 215 220
Ala Trp Lys Ala
225
<210>46
<211>14
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>46
Ala Leu Trp Glu Pro Gly Tyr Ser Ser Asp Trp Ile Lys Thr
1 5 10
<210>47
<211>13
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>47
Ala Leu Trp Glu Asp Val Gly Asp Tyr Tyr Lys Lys Leu
1 5 10
<210>48
<211>12
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>48
Ala Leu Trp Glu Phe Glu Ser Phe Tyr Lys Lys Leu
1 5 10
<210>49
<211>13
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>49
Ala Thr Trp Asp Gly Trp Ala Phe Tyr Tyr Lys Lys Leu
1 5 10
<210>50
<211>6
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>50
Ala Pro His Lys Lys Leu
1 5
<210>51
<211>12
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>51
Ala Thr Trp Ser Pro Thr Leu Tyr Tyr Lys Lys Leu
1 5 10
<210>52
<211>10
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>52
Ala Thr Trp Asp Val Glu Arg Lys Lys Leu
1 5 10
<210>53
<211>13
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>53
Ala Thr Trp Asp Gly Ile Ser Ser Asp Trp Ile Lys Thr
1 5 10
<210>54
<211>13
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>54
Ala Thr Trp Asp Gly Pro Lys Asn Tyr Tyr Lys Lys Leu
1 5 10
<210>55
<211>11
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>55
Ala Thr Trp Asp Gly Gln Tyr Tyr Lys Lys Leu
1 5 10
<210>56
<211>11
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>56
Ala Thr Trp Asp Ala Asn Tyr Tyr Lys Lys Leu
1 5 10
<210>57
<211>14
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>57
Ala Ile Tyr Pro Gly Pro Gly Pro Ser Gly Trp Phe Lys Ile
1 5 10
<210>58
<211>12
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>58
Ala Thr Trp Asp Tyr Ser Thr Gly Trp Phe Lys Ile
1 5 10
<210>59
<211>10
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>59
Ala Thr Trp Asp Gly Arg Asp Lys Lys Leu
1 5 10
<210>60
<211>15
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>60
Ala Leu Trp Glu Glu Pro Gln Glu Leu Gly Lys Lys Ile Lys Val
1 5 1015
<210>61
<211>10
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>61
Ala Leu Trp Phe Phe Arg Trp Phe Lys Ile
1 5 10
<210>62
<211>14
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>62
Ala Leu Trp Glu Val Gln Glu Leu Gly Lys Lys Ile Lys Val
1 5 10
<210>63
<211>17
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>63
Ala Leu Trp Glu Thr Thr Phe Trp Gly Glu Leu Gly Lys Lys Ile Lys
1 5 1015
Val
<210>64
<211>10
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>64
Ala Leu Trp Glu Pro Gln Asp Lys Lys Leu
1 5 10
<210>65
<211>14
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>65
Ala Leu Trp Glu Pro Gln Glu Leu Gly Lys Lys Ile Lys Val
1 5 10
<210>66
<211>19
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>66
Ala Met Arg Ala Phe Thr Phe Pro Arg Tyr Trp Gly Trp Asp Thr Asp
1 5 1015
Lys Leu Ile
<210>67
<211>21
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>67
Ala Tyr Arg Ser Leu Leu Thr Leu Pro Trp Met Gly Asp Thr Pro Tyr
1 5 1015
Thr Asp Lys Leu Ile
20
<210>68
<211>9
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>68
Ala Leu Gly Gly Phe Gly Arg Leu Ile
1 5
<210>69
<211>22
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>69
Ala Leu Gly Glu Leu Thr Thr Pro Leu Ser Leu Pro Trp Gly Ile Leu
1 5 1015
Asn Thr Asp Lys Leu Ile
20
<210>70
<211>17
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>70
Ala Leu Gly Glu Leu Pro Pro Phe Leu Gly Trp Ser Thr Asp Lys Leu
1 5 1015
Ile
<210>71
<211>23
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>71
Ala Leu Val Gly Pro Phe Leu Phe Leu Pro Gly Gly Tyr Thr Val Pro
1 5 1015
Thr Asp Thr Asp Lys Leu Ile
20
<210>72
<211>18
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>72
Ala Leu Gly Val Thr Ile Phe Leu Pro Trp Gly Gly His Thr Asp Lys
1 5 1015
Leu Ile
<210>73
<211>21
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>73
Ala Leu Gly Glu Leu Ser Asn Phe Leu Arg Gly Thr Gly Ile Gly Glu
1 5 1015
Thr Asp Lys Leu Ile
20
<210>74
<211>19
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>74
Ala Leu Gly Asp Pro Leu Ile Leu Pro Trp Gly Ile Arg Asp Thr Asp
1 5 1015
Lys Leu Ile
<210>75
<211>15
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>75
Ala Ala Thr Ala Pro Thr Leu Ser Gly Gly Ser Asp Lys Leu Ile
1 5 1015
<210>76
<211>27
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>76
Ala Leu Gly Glu Leu Leu Val Pro Thr Tyr Trp Gly Ile Gln Phe Ser
1 5 1015
Tyr Ser His Pro Pro Tyr Thr Asp Lys Leu Ile
2025
<210>77
<211>13
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>77
Ala Phe Gly Tyr Thr Gly Glu Tyr Thr Asp Lys Leu Ile
1 5 10
<210>78
<211>22
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>78
Ala Leu Gly Glu Asn Lys Trp Gly Leu Pro Ser Leu Val Leu Gly Ile
1 5 1015
Arg Ser Asp Lys Leu Ile
20
<210>79
<211>16
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>79
Ala Leu Gly Glu Leu Leu Trp Pro Ser Tyr Ala Gly Asp Lys Leu Ile
1 5 1015
<210>80
<211>27
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>80
Thr Leu Gly Glu Leu Leu Val Pro Thr Tyr Trp Gly Ile Gln Phe Ser
1 5 1015
Tyr Ser His Pro Pro Tyr Thr Asp Lys Leu Ile
2025
<210>81
<211>27
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>81
Thr Leu Gly Glu Leu Leu Val Pro Ala Cys Trp Gly Ile Gln Phe Ser
1 5 1015
Tyr Ser His Pro Pro Tyr Thr Asp Lys Leu Ile
2025
<210>82
<211>22
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>82
Asp Leu Gly Glu Asn Lys Trp Gly Leu Pro Ser Leu Val Leu Gly Ile
1 5 1015
Arg Ser Asp Lys Leu Ile
20
<210>83
<211>22
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>83
Asp Leu Glu Glu Asn Lys Trp Gly Leu Pro Ser Leu Val Leu Gly Ile
1 5 1015
Arg Ser Asp Lys Leu Ile
20
<210>84
<211>27
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>84
Ala Leu Gly Lys Leu Leu Gly Pro Thr Tyr Trp Gly Ile Gln Phe Ser
1 5 1015
Tyr Ser His Pro Pro Tyr Thr Asp Lys Leu Ile
2025
<210>85
<211>27
<212>PRT
<213>人工序列
<220>
<223>合成聚合物.
<400>85
Ala Leu Gly Glu Leu Leu Val Pro Thr Tyr Trp Gly Thr Gln Phe Ser
1 5 1015
Tyr Ser His Pro Pro Tyr Thr Asp Lys Leu Ile
2025
- 一种水牛精原干细胞样细胞纯化过程中细胞类型的鉴定方法
- 检测和/或定量细胞中靶蛋白候选物的表达的方法和鉴定小分子调节剂的靶蛋白的方法
- 用于鉴定味觉调节剂的模式味觉细胞和方法
