生物标志物在预测肺癌预后中的应用、相关产品
文献发布时间:2024-07-23 01:35:21
技术领域
本申请属于细胞生物学及医药技术领域,涉及一种生物标志物在预测肺癌预后中的应用、相关产品。
背景技术
肺癌是我国发病率和死亡率较高的一种疾病。其中,非小细胞肺癌(Non-smallcell lung cancer,NSCLC)约占所有肺癌的85%,严重威胁了人民的生命健康。近年来,以程序性死亡受体1(Programmed cell death protein 1,PD-1)为主的免疫检查点治疗在多种肿瘤治疗中取得了良好的治疗疗效。然而,临床实践中部分肺癌患者无应答或长期应答率较低。
这种检测指标具有较大的局限性,仅限于指导特定的PD-1单抗临床治疗,如帕博利珠单抗和纳武单抗等,普适性低。另外,大部分晚期NSCLC患者具有病灶多发转移特征,临床对患者肿瘤组织进行活检时通过只进行局部采样,导致肿瘤组织中PD-L1表达的检测并不准确。
临床还发现PD-1单抗治疗效果与PD-L1的表达量并没有足够的相关性,这进一步表明了现有的预测体系不能有效且精准地反映临床免疫治疗效果,这提示了肿瘤中存在其他因素限制了PD-1单抗治疗效果。
近年来,越来越多的研究对PD-1单抗治疗耐药因素进行了深入分析,结果表明,在接受PD-1单抗治疗的肺癌患者中,肺癌组织突变负荷高的患者具有较高的临床有效率。另外,肺癌患者肿瘤组织RNA测序数据分析显示免疫相关的差异特征,如干扰素反应基因、趋化因子的表达、细胞毒性反应基因等,与PD-1单抗治疗有效率具有一定的联系。此外,肿瘤中MHC分子功能障碍、T细胞抗肿瘤功能确实以及肿瘤组织中免疫抑制细胞的存在等均介导了PD-1单抗治疗耐药。这些研究结果表明了影响PD-1单抗治疗耐药的因素非常复杂。但是,这些研究具有局限性,相关指标缺乏大量临床样本的验证,临床预测价值不明确。
发明内容
为了克服现有技术的不足,本申请的目的在于提供一种生物标志物在预测肺癌预后中的应用、相关产品,以更便捷、准确地预测肺癌患者在接受化疗联合PD-1单抗免疫治疗后的预后效果。
本申请第一方面提供了检测生物标志物的试剂或方法在制备用于预测肺癌预后的产品的应用,所述生物标志物为苯丙氨酸。
在一些实施方式中,所述检测生物标志物的试剂或方法用于检测肺癌患者血液中所述苯丙氨酸的浓度。
在一些实施方式中,治疗后所述苯丙氨酸的浓度升高的患者预后比所述苯丙氨酸的浓度降低的患者预后差。
在一些实施方式中,苯丙氨酸变化差异=(治疗后所述苯丙氨酸的浓度-治疗前所述苯丙氨酸的浓度)/治疗前所述苯丙氨酸的浓度,所述苯丙氨酸变化差异大于17.11的患者预后比所述苯丙氨酸变化差异小于17.11的患者预后差。
在一些实施方式中,苯丙氨酸变化差异大于10.79的患者预后比苯丙氨酸变化差异小于10.79的患者预后差。
在一些实施方式中,所述肺癌治疗的方法为肺癌PD-1单抗治疗。
在一些实施方式中,所述肺癌治疗的方法为化疗联合PD-1单抗治疗。
本申请第二方面提供了一种用于肺癌预后的产品,所述产品包括本申请第一方面所述的检测生物标志物的试剂或检测生物标志物的方法涉及的试剂。
在一些实施方式中,所述产品用于检测化疗联合PD-1单抗治疗的肺癌患者血液中所述苯丙氨酸的浓度。
在一些实施方式中,所述产品为试剂盒。
相比现有技术,本申请的有益效果在于:
本申请提供了一种检测生物标志物的试剂或方法在制备用于预测肺癌预后的产品的应用及一种用于肺癌预后的产品,该生物标志物为苯丙氨酸。本申请通过非靶标代谢组学筛选与化疗联合PD-1单抗免疫治疗疗效相关的代谢物,结合现有的临床疗效评估标准,发现联合治疗前后苯丙氨酸的变化比例能够有效预测肺癌患者的临床疗效,能够早于影像学检测预测患者的临床疗效,且检测取材简单、耗时短、检测费用低。
附图说明
图1示出了化疗组和化疗联合PD-1单抗组中差异代谢物通路分析:其中,图1A、图1B示出了接受化疗联合PD-1单抗(图1A)或化疗(图1B)的肺癌患者血浆中差异代谢物;图1C--图1E示出了接受化疗联合PD-1单抗治疗有效组治疗前后(图1C),以及化疗有效组治疗前后(图1D)和无效组治疗前后(图1E)的肺癌患者血浆差异代谢物的通路富集分析;图1F、图1G示出了精氨酸在化疗或化疗联合PD-1单抗的肺癌患者血浆中的变化;图1H、图1I示出了苯丙氨酸在化疗或化疗联合PD-1单抗的肺癌患者血浆中的变化;R是临床治疗有效患者,NR是临床治疗无效患者,Pre是临床治疗前,Post是临床治疗后;
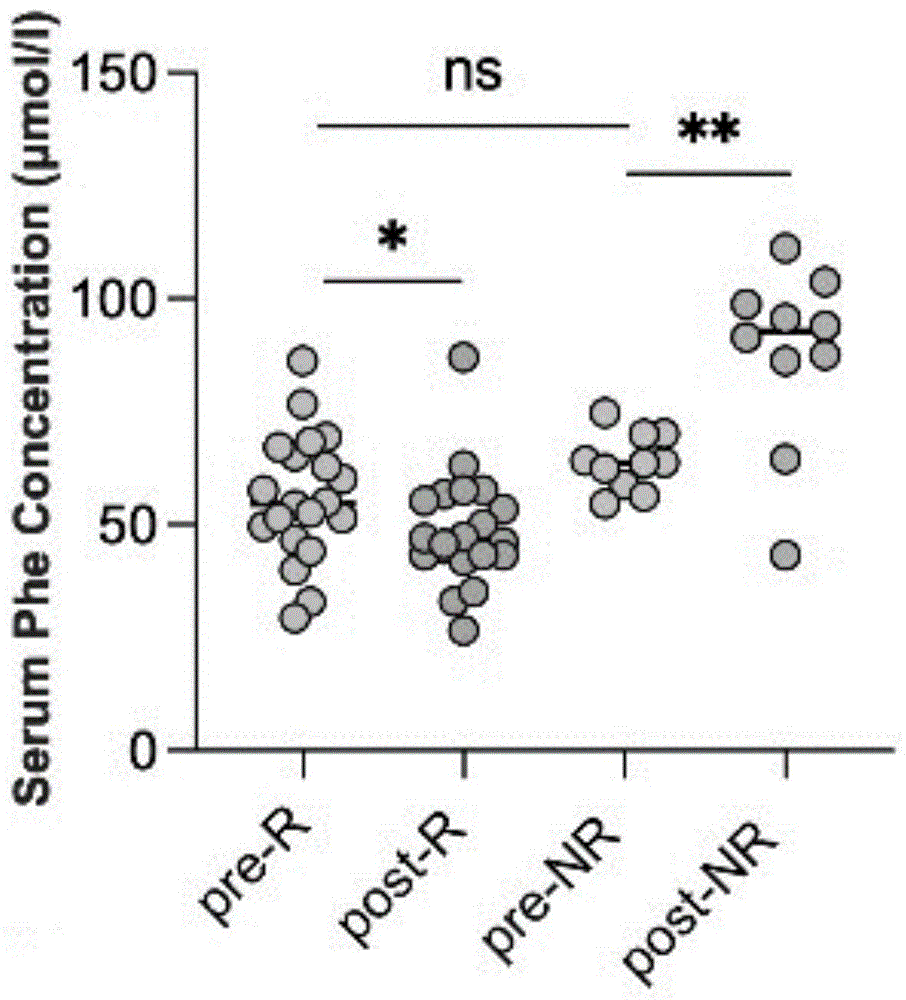
图2示出了化疗联合PD-1单抗治疗基线和4周期的苯丙氨酸变化的临床预后分析:其中,图2A示出了接受化疗联合PD-1单抗的肺癌患者血浆中苯丙氨酸含量检测,pre-R为有效组治疗前,post-R为有效组治疗后,pre-NR为无效组治疗前,post-NR为无效组治疗后;图2B示出了化疗联合PD-1单抗治疗基线和4周期的肺癌患者苯丙氨酸变化比例,R为有效组,NR为无效组;图2C示出了苯丙氨酸变化比例与化疗联合PD-1单抗治疗肺癌患者预后的ROC分析;图2D示出了化疗联合PD-1单抗治疗的肺癌患者治疗后肿瘤体积变化;图2E示出了不同治疗疗效组中高于或低于最佳苯丙氨酸变化比例的患者人数统计;图2F示出了高于或低于最佳苯丙氨酸变化比例的肺癌患者CT影像结果,白色虚线圈内显示为肿瘤,灰色区域减少表示肿瘤体积缩小,灰色区域增加代表肿瘤体积增加;图2G示出了高于或低于最佳苯丙氨酸变化比例的肺癌患者无疾病生存期和生存期分析;
图3示出了化疗联合PD-1单抗治疗基线和1周期的苯丙氨酸变化的临床预后分析;其中,图3A示出了验证集1中接受化疗联合PD-1单抗的肺癌患者血浆中苯丙氨酸含量检测;图3B示出了不同治疗疗效组中高于或低于最佳苯丙氨酸变化比例(4周期)的患者人数统计;图3C示出了高于或低于最佳苯丙氨酸变化比例(4周期)的肺癌患者无疾病生存期和生存期分析;图3D示出了验证集1中化疗联合PD-1单抗治疗不同时间点肺癌患者血浆中苯丙氨酸含量变化,BL是治疗基线,last cycle是复发前最后一次PD-1治疗;图3E示出了验证集1中化疗联合PD-1单抗治疗基线和1周期的肺癌患者苯丙氨酸变化比例,R有效组,NR无效组;图3F示出了1周期苯丙氨酸变化比例与化疗联合PD-1单抗治疗肺癌患者预后的ROC分析;图3G示出了不同治疗疗效组中高于或低于最佳苯丙氨酸变化比例(1周期)的患者人数统计;图3H示出了高于或低于最佳苯丙氨酸变化比例(1周期)的肺癌患者CT影像结果,白色虚线圈内显示为肿瘤,灰色区域减少表示肿瘤体积缩小,灰色区域增加代表肿瘤体积增加;图3I示出了化疗联合PD-1单抗治疗的肺癌患者治疗后肿瘤体积变化;图3J示出了高于或低于最佳苯丙氨酸变化比例(1周期)的肺癌患者无疾病生存期和生存期分析;
图4示出了验证集2中化疗联合PD-1单抗治疗基线和1周期的苯丙氨酸变化的临床预后分析;其中,图4A示出了化疗联合PD-1单抗治疗的肺癌患者治疗后肿瘤体积变化;图4B示出了不同治疗疗效组中高于或低于最佳苯丙氨酸变化比例(1周期)的患者人数统计;图4C示出了高于或低于最佳苯丙氨酸变化比例(1周期)的肺癌患者CT影像结果,白色虚线圈内显示为肿瘤,灰色区域减少表示肿瘤体积缩小,灰色区域增加代表肿瘤体积增加;图4D示出了高于或低于最佳苯丙氨酸变化比例(1周期)的肺癌患者无疾病生存期和生存期分析。
具体实施方式
下面,结合附图以及具体实施方式,对本申请做进一步描述,需要说明的是,在不相冲突的前提下,以下描述的各实施例之间或各技术特征之间可以任意组合形成新的实施例。
现有技术中通常采用影像学检测、PD-L1表达检测、肿瘤突变负荷检测用于肺癌诊断和治疗、预后的效果评估。但是,影像学检测是临床评估疗效的金标准,但其检测时间受临床化疗联合PD-1治疗疗程限制。PD-L1表达主要通过对肺癌患者的肿瘤组织进行染色,对于大部分肺癌患者肿瘤取材较为困难;这种检测方法在治疗前筛选可能响应PD-1单抗治疗疗效的患者,忽略了治疗过程中的影响;现有PD-L1表达预测效果适用于只接受PD-1单抗治疗的肺癌,不适用于接受化疗联合PD-1单抗治疗的肺癌患者。肿瘤突变负荷的检测方法与PD-L1表达一样,需要获取患者的肿瘤组织,取材难;且在治疗前筛选可能响应PD-1单抗治疗疗效的患者,忽略了治疗过程中的影响。
为了解决现有技术存在的问题,下面结合附图对本申请一种生物标志物在预测肺癌预后中的应用、相关产品做进一步阐述。
实施例
1.1肺癌患者入组:收集接受化疗联合PD-1单抗治疗的NSCLC患者治疗前和治疗后不同周期的外周血。在本申请实施例中,选取的患者入组年龄在50岁至70岁之间,入组者的病理诊断均为非小细胞癌,且临床治疗方案一致。在本实施例中,要求入组患者没有其他合并症、有可评估病灶,预估生存期超过半年,申请人能够定期随访患者以做病情记录。需要指出的是,本申请中涉及的入组患者知情并同意参与本项目,本项目已经获得郑州大学第一附属医院伦理委员会批准。
本申请实施例通过医院病历系统查询已经收集的患者临床资料,如性别、年龄、肿瘤分期、转移以及相关实验室检测和影像学资料。并根据RECIST1.1标准,评估患者的临床反应,长期跟踪患者的疾病进展。
1.2外周血标本处理:本申请使用无菌抗凝管收集患者外周血5mL,冰上运输至实验室。使用离心机将外周血在3000rpm转速下离心10min,收集上清液,即得血浆样本。
1.3非靶代谢组学分析:取50L血浆样品至EP管中,加入200L提取液,该提取液中甲醇与乙腈体积比为1:1,且该提取液中含同位素标记内标混合物。涡旋混匀30s,接着在冰水浴中超声10min,-40℃环境下静置1h;接着将样品于4℃环境下以12000rpm转速离心15min;取上清于进样瓶中上机检测,所有样品另取等量上清混合并上机检测。
使用Vanquish(Thermo Fisher Scientific)超高效液相色谱仪,通过WatersACQUITY UPLC BEH Amide(2.1mm×100mm,1.7m)液相色谱柱对目标化合物进行色谱分离。液相色谱A相为水相,含25mmol/L乙酸铵和25mmol/L氨水,B相为乙腈。样品盘温度为4℃,进样体积为3L。Thermo Q Exactive HFX质谱仪能够在控制软件(Xcalibur,Thermo)控制下进行一级、二级质谱数据采集。详细参数如下:鞘气流速:30Arb,辅助气体流速:25Arb,毛细管温度:350℃,全ms分辨率:60000,MS/MS分辨率:7500,碰撞能量:10/30/60在NCE模式,喷雾电压:3.6kV(positive)或-3.2kV(negative)。原始数据经ProteoWizard软件转成mzXML格式后,使用自主编写的R程序包(内核为XCMS)进行峰识别、峰提取、峰对齐和积分等处理,然后与BiotreeDB(V2.1)自建二级质谱数据库匹配进行物质注释,算法打分的Cutoff值设为0.3。
1.4苯丙氨酸定量检测:本申请使用10KD旋转柱除去入组患者血浆中的大分子量蛋白,离心后取上清液,并转移至新的离心管中,每个样本取出10μL加入到ELISA板中,再加入90μL苯丙氨酸测定缓冲液。同时,将不同浓度的苯丙氨酸标准品依次加到不同的测试孔,每孔100μL。最后在每个孔中添加100μL的反应液混匀。于37℃避光孵育30min,使用酶标仪检测450nm的吸光度值。
实验结果:
1)肺癌患者标本收集及分组
本申请实施例收集了化疗及化疗联合PD-1单抗治疗的肺癌患者外周血标本,记录患者的临床信息及预后。根据实体肿瘤临床疗效评估标准(RECIST1.1),结合肺癌患者的影像学结果对患者的临床治疗疗效进行评估。临床疗效主要分为:有效组:完全缓解(Complete response,CR)、部分缓解(Partial response,PR)和疾病稳定(Stabledisease,SD)和无效组:疾病进展(Progressive disease,PD)。
本申请分别在肺癌患者治疗的不同周期收集患者的外周血,离心获得血浆。本申请共收集了170例肺癌患者,其中3例患者失访,最终167例患者成功入组。入组患者中126例患者的治疗方案为化疗联合PD-1单抗治疗,41例患者的治疗方案为化疗。本申请分别对这两组患者进行随访,最终纳入本研究的患者为119例,这些患者的治疗方案为化疗联合PD-1单抗治疗的记为化疗联合PD-1单抗组;35例患者的治疗方案为化疗的记为化疗组。选取接受化疗联合PD-1单抗治疗的119例患者中49例用于非靶代谢组学分析,余下40例和30例患者作为验证集1和验证集2分别用于验证非靶代谢组学的分析结果。
2)化疗组和化疗联合PD-1单抗组中差异代谢物通路分析
根据不同治疗疗效组的差异代谢物,本申请分析了该差异代谢物参与的信号通路,结果如图1A至图1E所示。通过对比分析这些差异代谢物参与的信号通路,申请人发现在化疗联合PD-1单抗组中,差异代谢物参与的信号通路主要有精氨酸和脯氨酸代谢、苯丙氨酸,酪氨酸和色氨酸合成及苯丙氨酸代谢等;在化疗组中,差异代谢物参与的信号通路主要有精氨酸和脯氨酸代谢、苯丙氨酸,酪氨酸和色氨酸合成及苯丙氨酸代谢等。
基于上述差异代谢物的信号通路富集分析,申请人进一步分析了苯丙氨酸和精氨酸在化疗及化疗联合PD-1单抗治疗有效组和无效组的变化。如图1F、图1G所示,在化疗联合PD-1单抗治疗中,相较于治疗前,有效组患者的血浆中的精氨酸含量在治疗后下降;但是在化疗中,无效组患者血浆中的精氨酸含量下降。如图1H、图1I所示,在化疗联合PD-1单抗治疗的有效组中,相较于治疗前,患者血浆中的苯丙氨酸含量在治疗后下降。但是在化疗联合PD-1单抗治疗的无效组中,患者血浆中的苯丙氨酸的含量在治疗后升高。化疗组的患者血浆中的苯丙氨酸未发生改变,这表明了苯丙氨酸的浓度变化与化疗联合PD-1单抗治疗疗效相关。
3)化疗联合PD-1单抗治疗基线和4周期的苯丙氨酸变化的临床预后分析
基于代谢组学分析结果,本申请进一步通过ELISA检测了30例用于代谢组学分析的肺癌患者血浆中的苯丙氨酸浓度,该30例均为接受化疗联合PD-1单抗治疗的患者。结果如图2A至图2G所示。如图2A至图2G所示,治疗有效组的患者血浆中苯丙氨酸的浓度降低,而治疗无效组的苯丙氨酸浓度升高,这与代谢组学的结果一致(如图2A所示)。为了更好的显示苯丙氨酸变化差异对患者临床预后的指示作用,申请人对患者在化疗联合PD-1单抗治疗前后的血浆中的苯丙氨酸变化差异进行了量化分析,该苯丙氨酸变化差异用(治疗后苯丙氨酸浓度-治疗前苯丙氨酸浓度)/治疗前苯丙氨酸浓度表示。结果如图2B所示,治疗无效组的肺癌患者苯丙氨酸的变化差异大于0,表明治疗后患者血浆中的苯丙氨酸浓度上升,患者的临床疗效差。
进一步,本申请通过ROC曲线分析患者血浆中苯丙氨酸的变化差异与临床疗效之间的关系。本申请将入组患者的苯丙氨酸变化差异值作为预测结果,同时将患者的治疗效果作为二元变量(NR=1,R=0)分别存储于两个向量中,运行pROC包。使用ROC函数来创建ROC对象,其中response作为真实标签向量,predictor为预测结果向量,使用plot函数来绘制ROC曲线并获得最佳阈值,使用AUC函数计算曲线下面积(AUC)作为衡量预测模型性能的指标。AUC越接近于1,则表示预测性能越好。
结果如图2C所示,当患者血浆中的苯丙氨酸变化差异在17.11时能够较好的预测患者的临床疗效。基于上述分析,本申请将上述ELISA检测的30例患者分为两组,一组患者血浆中苯丙氨酸的变化差异大于等于17.11,一组患者血浆中苯丙氨酸的变化差异小于17.11。通过随访发现,如图2D至图2F所示,血浆中苯丙氨酸变化差异大于等于17.11组中81.82%的患者临床治疗无效,然而在苯丙氨酸变化差异小于17.11组中仅有5.26%的患者临床治疗无效。进一步,申请人对这些患者的无疾病生存期和生存进行随访,结果如图2G所示,血浆中的苯丙氨酸浓度变化差异大于等于17.11组的肺癌患者无疾病生存期和生存期均小于血浆中苯丙氨酸变化差异小于17.11组的肺癌患者。
4)化疗联合PD-1单抗治疗基线和1周期的苯丙氨酸变化的临床预后分析
本申请从实施例收集的170例中选取了40例接受化疗联合PD-1单抗治疗的肺癌患者,用于验证前期试验结果。结果如图3A至图3C所示,验证集1中,血浆中苯丙氨酸变化差异大于等于17.11组的肺癌患者无疾病生存期和生存期也小于血浆中苯丙氨酸变化差异小于17.11组的肺癌患者。
由于目前临床上评估患者的治疗疗效的金标准为影像学结果,患者一般在接收一个疗程后的治疗后通过影像结果分析肿瘤体积变化,进而评判临床疗效。接受化疗联合PD-1单抗治疗的肺癌患者,临床上通常在治疗4个周期后进行影像学评估。因此,为了验证苯丙氨酸浓度变化与临床疗效的相关性,进一步,本申请动态分析了验证集1中肺癌患者接受化疗联合PD-1单抗治疗后不同时间点时血浆中的苯丙氨酸浓度变化。结果如图3D所示,随着治疗周期的变化,患者血浆中苯丙氨酸的浓度在有效组中逐渐下降,在无效组在逐渐上升,结果表明治疗后1周期的苯丙氨酸浓度变化已经能够有效预测患者的临床疗效。
本申请进一步量化了上述40例肺癌患者治疗1周期后血浆中的苯丙氨酸浓度变化。如图3E、图3F所示,治疗无效组的肺癌患者血浆中苯丙氨酸的变化差异仍大于0,ROC曲线分析显示治疗后1周期苯丙氨酸变化差异在10.79的时候能够较好的预测患者的临床疗效。根据治疗后1周期苯丙氨酸的变化差异值,本申请将上述患者分为两组,一组1周期苯丙氨酸的变化差异值大于等于10.79,一组1周期苯丙氨酸的变化差异值小于10.79。结果表明,如图3G至图3I所示,1周期苯丙氨酸的变化差异值大于等于10.79组中87.5%的患者临床治疗无效,然而在1周期苯丙氨酸的变化差异值小于10.79组中仅有25%的患者临床治疗无效。进一步,本申请对上述患者的无疾病生存期和生存进行随访,如图3J所示,1周期苯丙氨酸的变化差异值大于等于10.79组的肺癌患者无疾病生存期和生存期均小于1周期苯丙氨酸的变化差异值小于10.79组的肺癌患者。
5)验证集2中化疗联合PD-1单抗治疗基线和1周期的苯丙氨酸变化的临床预后分析
本申请收集了30例肺癌患者的治疗及疾病数据用于验证化疗联合PD-1单抗治疗1周期后患者血浆中的苯丙氨酸变化对临床疗效的预测作用。在本实验中,该30例肺癌患者用于前瞻性队列分析。根据患者的临床影像学资料对患者临床疗效进行评估。将上述患者分为两组,一组1周期苯丙氨酸的变化差异值大于等于10.79,一组1周期苯丙氨酸的变化差异值小于10.79。如图4A至图4C所示,1周期苯丙氨酸的变化差异值大于等于10.79组中73.3%的患者临床治疗无效,1周期苯丙氨酸的变化差异值小于10.79组中仅有26.7%的患者临床治疗无效。如图4D所示,与1周期苯丙氨酸的变化差异值小于10.79组的肺癌患者相比,苯丙氨酸变化差异大于等于10.79组的肺癌患者无疾病生存期和生存期较长。
上述实施方式仅为本申请的优选实施方式,不能以此来限定本申请保护的范围,本领域的技术人员在本申请的基础上所做的任何非实质性的变化及替换均属于本申请所要求保护的范围。
- 与肺癌生存期相关的生物标志物及其在预测肺癌预后中的应用
- 基于生物标志物的预测肺癌预后的产品及相关应用
