使用即时检测装置进行病原体富集和核酸提取的方法
文献发布时间:2023-06-19 10:32:14
技术领域
本发明涉及使用即时检测装置进行病原体富集和核酸提取的方法。
背景技术
病原体诊断在全球健康问题中非常重要,特别是在资源受限的环境中、如中央实验室技术。迄今为止,细胞培养、血液化学、流式细胞术、免疫分析和核酸检测(NAT)等多种方法已被开发用于病原体的诊断,细胞培养被广泛应用于临床诊断,但其缺点是需要耗时的过程、高成本、物种特异性方案,实验室环境和设备。另一方面,核酸检测因其具有相对快速和通用的方案以及在诊断测试(如窗口期诊断、免疫突变病毒检测和免疫沉默/隐性感染鉴定)方面的应用而受到人们的关注。然而,基于核酸检测的传统分析具有下述缺点,即市售产品和实验室开发的分析方法通常都很复杂。因此,需要进行复杂的预处理,该预处理须进行基于实验室的工作,例如熟练的技术人员、特定的设备和多个步骤。这些需求限制了核酸检测在即时检测(point-of-care testing;POCT)中的使用。
基于核酸检测的即时检测包括样品制备、模板扩增和信号检测三个主要方面。已经进行的研究集中于简单有效的扩增和检测,来作为对基于核酸检测的即时检测加以改进的方法,但也进行了集中于初始样品制备阶段的研究。已经开发出了一种基于核酸的即时检测方法,该方法可以直接从样品进行扩增,且不需要太多的提取,但由于灵敏度低、成本高,该方法仍然受到限制。包括从生物基质中提取核酸和去除化学抑制剂在内的样品制备非常重要,因为高质量的核酸是所有后续分析的基础。特别是,这一步骤应针对开放环境(而非实验室条件)进行定制,以消除无菌实验室与资源受限环境的界限。
与发达国家不同的是,由于永久性集成设施的高成本和熟练技术人员的限制,基于中央实验室的大规模诊断不适合于资源受限的环境。因此,一次性的即时分析方法可以成为资源受限的环境的解决方案。近10年来,免疫层析试纸条(ICS)检测是成功用于资源受限环境的诊断分析方法之一,但其缺点是在深度样品分析方面受限。
对于即时诊断用途而言,分析应当简化(即很少有制造和应用工艺、设施或培训方面的要求),并且应快速、可靠(物流和储存方面)并优化以降低成本。特别是,有必要将这种分析方法应用于常见的临床样本(如尿液、血液和痰)。然而,这一应用存在难度,原因在于PCR抑制剂在生物样品以及从样品提取病原体中被广泛刺激。因此,将病原体富集和核酸样品制备加以整合的应用解决方案可有助于临床检测和即时分析。此外,在包括非洲在内的欠发达国家,基于实验室的设备的使用由于供电困难而受到限制,因此,无需使用电(电力)即可富集病原体和提取核酸的即时分析具有在资源受限的环境中广泛使用的优势。
发明内容
技术问题
本发明的目的是提供用于即时检测的病原体富集和核酸提取装置。
本发明的另一个目的是提供使用上述装置的病原体富集和核酸提取方法。
技术手段
本发明提供了一种用于即时检测的病原体富集和核酸提取装置,该装置包括:进口;连接至进口的反应单元,该反应单元将通过进口引入的含有病原体的样品、交联剂和用硅烷化合物改性的硅藻土混合;连接至反应单元的过滤器单元,该过滤器单元能够阻挡含有病原体的样品、交联剂和用硅烷化合物改性的硅藻土,并使得具有与核酸对应尺寸的物质通过;连接至过滤器单元的出口单元,该出口单元对核酸进行分离。
并且,本发明还提供了一种病原体富集和核酸提取方法,该方法包括:第一步,提供用于即时检测的病原体富集和核酸提取装置;第二步,通过该装置的进口引入含有病原体的样品、交联剂和用硅烷化合物改性的硅藻土;第三步,在该装置的反应单元中,通过交联剂将病原体固定在用硅烷化合物改性的硅藻土表面;第四步,通过该装置的进口引入裂解缓冲溶液;第五步,在该装置的反应单元中,将从病原体中提取的核酸固定到用硅烷化合物改性的硅藻土表面;第六步,通过该装置的进口引入洗脱缓冲液;第七步,通过该装置的过滤器单元分离核酸,并通过出口单元获得核酸。
有益效果
本发明涉及一种使用胺官能化硅藻土和作为交联剂的辛二亚氨酸二甲酯(dimethyl suberimidate)来富集病原体和提取核酸的方法,其中带负电荷的病原体通过交联剂被电吸附在带正电荷的硅藻土表面,细胞裂解后释放的核酸可通过与硅藻土的胺基团发生可逆交联而在硅藻土上固定并分离。上述方法可以用作即时检测,原因在于其可以作为一体式装置同时富集病原体和提取核酸,而无需使用专用设备和电(电力),并且在时间和成本节约方面都优于传统方法,所提取的核酸具有可用于疾病诊断和治疗的优点。
附图说明
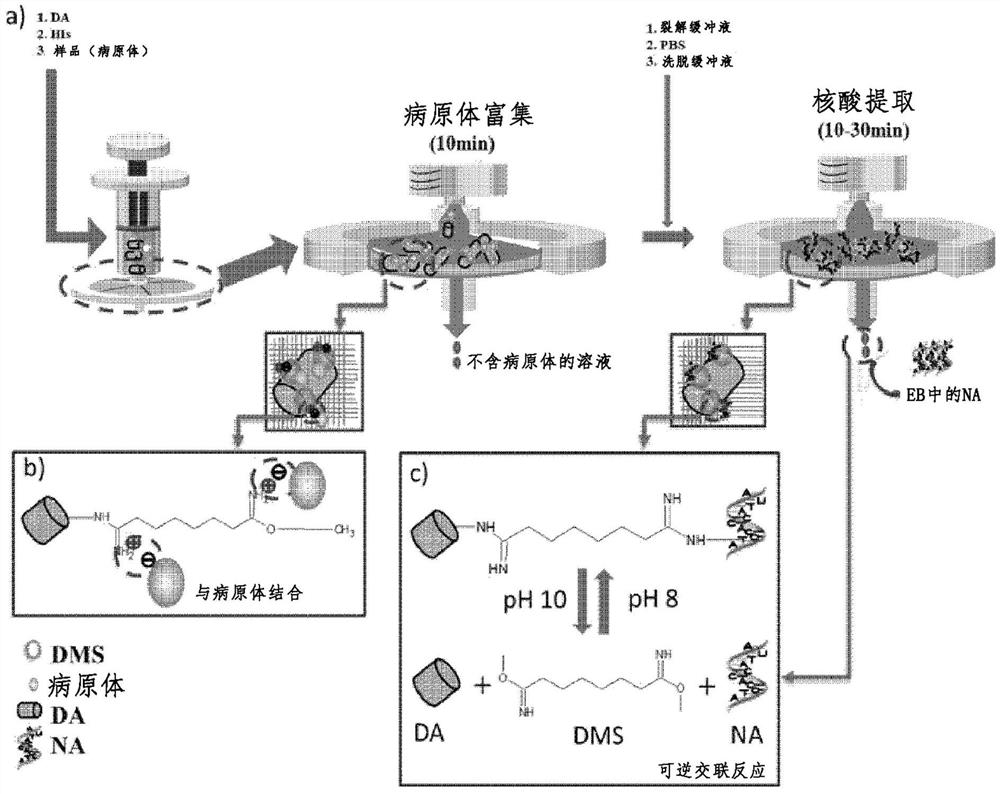
图1是示出使用胺官能化硅藻土(DA)和辛二亚氨酸二甲酯(DMS),通过便携注射器过滤器装置来富集病原体和提取核酸的方法的图:(a)在注射器中混合DA、病原体和DMS;(b)病原体富集过程,其中通过DMS将病原体吸附在DA表面,随后被过滤器阻挡;以及(c)通过DA的胺基团和核酸(由溶解的病原体所释放)之间的可逆交联反应来分离核酸。
图2是示出注射器过滤器的顶面和侧面的视图。
图3示出用于优化核酸分离过程的实时定量PCR的结果:(a)优化用于DA生产的硅烷化合物;(b)优化同种型的双官能亚氨基酯;(c)优化DA浓度;(d)优化DMS浓度;(e)优化用于RNA分离的培育时间;以及(f)在优化条件下分离的DNA模板的评价(以C
图4示出使用优化的核酸分离过程捕获DNA和RNA的效率。
图5示出用于评价DA-DMS试管体系的实时定量PCR的结果:(a)评价使用DA-DMS试管体系和商业试剂盒体系从病原体样品中分离的RNA模板;以及(b)评价从不同样品和体积中分离的RNA模板(以C
图6示出用于评价DA-DMS过滤器体系的实时定量PCR的结果:(a)评价注射器过滤器的类型;以及(b)评价使用DA-DMS过滤器体系和商业试剂盒体系从病原体样品中分离的RNA(以C
图7示出用于评价DA-DMS过滤器体系的大样品处理能力的实时定量PCR的结果:(a)评价从不同体积的样品中分离的RNA模板;以及(b)评价从不同样品中分离的RNA模板(以C
具体实施方式
本发明的发明人提供了一种病原体富集和核酸提取的方法,该方法可以容易地集成到其他分析中,并且该方法是设计成简化整个过程的集成装置,可以用于即时检测。在胺官能化硅藻土(DA)和辛二亚氨酸二甲酯(DMS)的存在下,可以通过注射器过滤器富集病原体,而无需额外的设备即可提取核酸。
在水性环境中,带正电荷的硅藻土可与带负电荷的病原体发生电结合。但是,能与硅藻土的胺基团结合的辛二亚氨酸二甲酯的存在可形成更多的正电荷,从而强化病原体的富集过程。因此,带负电荷的病原体可以在1mL的样品中直接被硅藻土吸附,或者在大样品(50mL)中通过短时培育直接被吸附。同时,辛二亚氨酸二甲酯已知为核酸或蛋白质的胺基团的可逆反应所用的交联剂。由于反应在受控的pH下可发生逆转,因此可通过注入其他缓冲液来容易地实现用于诊断的核酸样品的提取,本发明的诊断方法尤其具有适于各种临床样品的优点。
图1为本发明的集成分析方法的示意图,便携注射器过滤器装置能有效地富集病原体和分离核酸,其优点是分析生产和操作程序简单,成本低,总的工作时间可以缩短到低达20分钟。此外,该方法不需要实验室设施,可以为各种临床样品提供通用方案。
因此,本发明提供一种用于即时检测的病原体富集和核酸提取装置,该装置包括:进口;连接至进口的反应单元,该反应单元对通过进口引入的含有病原体的样品、交联剂和用硅烷化合物改性的硅藻土进行混合;连接至反应单元的过滤器单元,该过滤器单元能够阻挡含有病原体的样品、交联剂和用硅烷化合物改性的硅藻土,并且使得具有与核酸对应尺寸的物质通过;以及连接至过滤器单元的出口单元,该出口单元对核酸进行分离。
过滤器可以具有平均直径为0.5-1μm的孔,并且可以具有10-30mm的直径和1-10mm的厚度,但不限于此。
过滤器可选自于由纳米和微米滤膜过滤器、反渗透过滤器、中空纤维膜过滤器和超滤膜过滤器所组成的组,但不限于此。
此外,本发明提供了一种病原体富集和核酸提取的方法,该方法包括:第一步,提供用于即时检测的病原体富集和核酸提取装置;第二步,通过该装置的进口引入含有病原体的样品、交联剂和用硅烷化合物改性的硅藻土;第三步,在该装置的反应单元中,通过交联剂将病原体固定在用硅烷化合物改性的硅藻土表面;第四步,通过该装置的进口引入裂解缓冲溶液;第五步,在该装置的反应单元中,将从病原体中提取的核酸固定到用硅烷化合物改性的硅藻土表面;第六步,通过该装置的进口引入洗脱缓冲液;以及第七步,通过该装置的过滤器单元分离核酸,并通过出口单元获得核酸。
第二步中含有病原体的样品可以是选自于由疑似感染病原体的对象的粪便、尿液、泪液、唾液、皮肤外分泌物、呼吸道外分泌物、肠道外分泌物、消化道外分泌物、血浆、血清、血液、脊髓液、淋巴液、体液和组织所组成的组中的任一种,但不限于此。
第二步中的病原体可以是微生物,该微生物可以是病毒、细菌、真菌、原生动物、立克次氏体(Rickettsia)或螺旋体(spirochaete),但不限于此。
第二步中的交联剂可选自于由辛二亚氨酸二甲酯(DMS)、己二亚氨酸二甲酯(DMA)、庚二亚氨酸二甲酯(DMP)和3,3′-二硫代双丙亚氨酸二甲酯(DTBP)所组成的组,但不限于此。
第二步中的硅烷化合物可以是选自于由3-氨基丙基(二乙氧基)甲基硅烷(APDMS)、(3-氨基丙基)三乙氧基硅烷(APTES)、(3-氨基丙基)三甲氧基硅烷、(1-氨基甲基)三乙氧基硅烷、(2-氨基乙基)三乙氧基硅烷、(4-氨基丁基)三乙氧基硅烷、(5-氨基戊基)三乙氧基硅烷、(6-氨基己基)三乙氧基硅烷、N-[3-(三甲氧基硅烷基)丙基]乙二胺、N-[3-(三甲氧基硅烷基)丙基]二亚乙基三胺、[3-(2-氨基乙基氨基)丙基]三甲氧基硅烷(AEAPTMS)和3-[(三甲氧基硅烷基)丙基]二亚乙基三胺(TMPTA)所组成的组中的任一种,但不限于此。
在第三步中,可以通过静电结合作用将带负电荷的病原体由交联剂固定到用带正电荷的硅烷化合物改性的硅藻土表面。
在第五步中,通过与用硅烷化合物改性的硅藻土的胺基团发生可逆交联,可将从病原体中提取的核酸固定在硅藻土表面。
病原体富集和核酸提取可在15-30分钟内完成。
核酸可选自于由DNA、RNA、循环肿瘤DNA(ctDNA)和无细胞DNA(cfDNA)所组成的组,但不限于此。
cfDNA是一种循环游离核酸,是指在血液中循环的DNA。循环游离核酸具体包括循环游离DNA和循环游离RNA等,优选可以是循环游离DNA,但不限于此。循环游离核酸在血浆或血清中的长度通常为1000bp以下(DNA)、100nt以下(RNA),但不限于此。
ctDNA是指从癌细胞中分离出来并在血液中循环的DNA。它既有肿瘤特异性突变,也有表观遗传(epigenetic)突变,占血液中总循环DNA的极少量。循环肿瘤DNA的尺寸从50bp到250bp不等,但不限于此。
实施例
下文中,将详细描述实施例以帮助理解本发明。然而,以下实施例仅旨在对本发明加以说明,本发明的范围并不限于以下实施例。提供本发明的实施例是为了向本领域技术人员更完整地解释本发明。
实施例1:材料
硅藻土(DE)、(3-氨基丙基)三乙氧基硅烷(APTES,99%)、3-氨基丙基(二乙氧基)甲基硅烷(APDMS,97%)、3-(2-氨基乙基氨基)丙基]三甲氧基硅烷(AEAPTMS,80%)和N1-(3-三甲氧基硅烷基丙基)二亚乙基三胺(TPDA)均购自Sigma Aldrich。
实施例2:胺官能化硅藻土的制备
将硅藻土(DE)用蒸馏水(DW)剧烈搅拌洗涤30分钟,然后离心去除含有杂质的沉淀。将胺官能化的DE(DA)用作富集和提取基质,通过与硅烷化合物的胺基团发生反应来合成经洗涤的DE的表面。按如下方式制备DA。简言之,将5mL硅烷滴加到含有100mL 5%(v/v)蒸馏水的乙醇混合物中,并用乙酸(pH 5)酸化。在剧烈搅拌下加入2g经洗涤的DE,并在室温下反应4h。将DA用乙醇洗涤,然后真空干燥过夜并储存,直至用于进一步分析。
实施例3:细胞培养
用羊布鲁氏菌(ATCC 25840)进行致病性诊断的评价。在37℃和5%CO
实施例4:病原体富集——基于试管
根据优化后的工艺,选择DA和辛二亚氨酸二甲酯(DMS,Sigma-Aldrich)作为富集和提取基质。首先,向样品中添加120μL APDMS-DE悬浮液(50mg/mL,在DW中)和100μL DMS溶液(200mg/mL,在DW中)。利用99rpm旋转混合器(拓普森仪器有限公司,中国宁波)在室温下反应1-30分钟,基于通过同双官能团亚氨酸酯(homobifunctional immidoester,HI)基团进行的可逆交联反应,将病原体附着到APDMS-DE表面。通过在1000rpm下离心1分钟去除上清液,来收集吸附了病原体的APDMS-DE。随后,用1mL磷酸盐缓冲盐水洗涤混合物,再次离心去除上清液,获得100μL含有病原体的样品。
实施例5:核酸提取——基于试管
为了从富集后的样品中分离核酸,向样品中加入20μL蛋白酶K、150μL自裂解缓冲液(100mM Tris-HCl(pH 8.0)、10mM乙二胺四乙酸、1%十二烷基硫酸钠和10%Triton X-100)、30μL溶菌酶溶液(30mg/mL,在DW中,Sigma-Aldrich)和10μL无RNA酶的DNA酶溶液(用于RNA,Qiagen)。随后,通过使用搅拌器在室温下以850rpm在56℃培育30分钟(对于DNA)或10分钟(对于RNA),然后离心去除上清液。用200μL磷酸盐缓冲盐水将与核酸结合的APDMS-DE洗涤两次,并通过轻缓地移液将所有溶液混合。然后,将100μL洗脱缓冲液(EB)(10mM碳酸氢钠,pH>10,用NaOH调节,Sigma-Aldrich)添加到溶液中,在室温下培育1分钟,然后离心并将含有核酸的上清液转移到1.5mL试管中,并在-20℃下储存。此外,将商业试剂盒(QIAampDNA迷你试剂盒和QNagen RNeasy迷你试剂盒)用作阳性对照样品,并根据推荐方案提取核酸。
实施例6:病原体富集——基于过滤器
使用注射器过滤器和DA-HI体系的病原体富集过程的示意图如图1b所示。向样品中添加120μL APDMS-DE悬浮液(50mg/mL,在DW中)和100μL DMS溶液(200mg/mL,在DW中)。使用99rpm旋转混合器(拓普森仪器有限公司,中国宁波)在室温下反应1-30分钟,基于通过HI基团进行的可逆交联反应将病原体附着到APDMS-DE的表面。使吸附有病原体的APDMS-DE混合物通过聚四氟乙烯(PTFE)注射器过滤器(Whatman,USA),过滤器的空隙为1.0μm。然后,通过1mL磷酸盐缓冲盐水洗涤其中捕获有病原体的过滤器。最后,用力按压注入有空气的注射器的柱塞,从过滤器中去除溶液。
实施例7:核酸提取——基于过滤器
为了从富集后的样品中分离核酸,将20μL蛋白酶K、150μL自裂解缓冲液、30μL溶菌酶溶液和10μL无RNA酶的DNA酶溶液注入注射器过滤器。接下来,轻缓地旋转注射器过滤器,在56℃(对于DNA)或室温(对于RNA)下培育,然后用1mL磷酸盐缓冲盐水通过过滤器两次,对捕获有核酸的过滤器进行洗涤。用力按压注入有空气的注射器的柱塞,去除过滤器中的溶液,再将100μL洗脱缓冲液注入过滤器中,随后在室温下反应1分钟。最后,通过用力按压注入有空气的注射器的柱塞,来洗脱含有核酸的溶液,并将其储存在-20℃下。
实施例8:实时PCR
为了检验所分离的DNA的质量,进行了PCR和实时PCR,并进行了RT-PCR和实时RT-PCR来验证所提取的RNA的质量。实验中使用的引物如下表1所示。
[表1]
试验例1:一体式(all-in-one)便携分析装置的制备
用于从不同样品中收集核酸模板的分析方法以商用PTFE注射器过滤器为基础,并如图1a所示用注射器进行泵送。DA和DMS的使用改善了病原体的富集。作为亚氨酸酯的DMS与DA的胺基团相连,形成带正电荷的亚胺键,该亚胺键可直接吸引带负电荷的病原体。此外,具有纳米孔结构的DA表现出很强的吸附能力和很高的反应面积,这有助于提高性能。用注射器过滤器分离所吸附的病原体和DA。因此,通过在溶液中将DMS和DA与病原体混合,然后将其注射到过滤器中,可以容易地进行如图1b所示的富集过程。
洗涤后,过滤器内的病原体原位溶解。已知DNA和RNA是通过可逆的交联反应分离的。DMS在核酸和DA的胺基团之间起到交联剂的作用。也就是说,核酸在反应缓冲液pH下通过交联反应固定在DA表面,而高pH的洗脱缓冲液则逆转该反应,随后释放所捕获的核酸。因此,如图1c所示,仅通过调节所注入的缓冲液的pH就可以容易地提取核酸模板。本发明的分析方法尤其在RNA分离中显示出良好的功效。由于RNA和DA之间有很强的共价键,所捕获的RNA足够稳定以抵抗降解。本发明的分析方法不需要额外的设备或预处理来去除RNA酶,可容易地应用于即时体系。
试验例2:一体式便携分析方法的优化
在采用该方法之前,必须对所有相关因素进行单独优化。因此,在图3中,通过定量RT-PCR(qRT-PCR)的循环阈值(C
图3a还分析了不同的硅烷化合物。C
试验例3:使用试管的一体式方法的评价
为了确认使用本发明的体系进行即时样品制备的能力,使用1mL(10
试验例4:一体式便携分析方法的性能评价
为了完全克服对实验室的依赖,将本发明的方法与注射器过滤器进行集成。在优化条件下对几种商用过滤器进行了分析,图6a示出了不同过滤器类型(醋酸纤维素(CA)、聚醚砜(PES)、聚偏氟乙烯(PVDF)和聚四氟乙烯(PTFE))的富集结果。在PTFE过滤器中尤其观察到快速C
此外,本发明的分析方法可通过使用注射器的简单装载步骤容易地处理大样品。如图7a所示,对直至多达50mL的样品进行了测试,并确认从不同体积的样品中稳定地进行了富集和核酸提取。此外,如图7b所示,在其他生物基质中验证了本发明的分析性能,确认富集和核酸提取在尿液样品中效果良好。
虽然已经参照具体实施方式对本发明进行了特别描述,但显而易见的是,该具体描述仅仅是优选实施方式,并且对于本领域技术人员而言本发明的范围并不限于此。也就是说,本发明的实际范围由所附权利要求及其等同方式限定。
本发明的范围由后文所述的权利要求加以指明,并且由权利要求的含义和范围及其等同概念所衍生的全部变化或修改形式应被解释为包括在本发明的范围内。
<110> INFUSION TECH
<120> 使用即时检测装置进行病原体富集和核酸提取的方法
<130> AOP-2019-0059/PCT/CN
<160> 4
<170> KoPatentIn 3.0
<210> 1
<211> 20
<212> DNA
<213> 人工序列
<220>
<223> IS711 正向
<400> 1
gcttgaagct tgcggacagt 20
<210> 2
<211> 17
<212> DNA
<213> 人工序列
<220>
<223> IS711 反向
<400> 2
ggcctaccgc tgcgaat 17
<210> 3
<211> 19
<212> DNA
<213> 人工序列
<220>
<223> invA 正向
<400> 3
tatcgccacg ttcgggcaa 19
<210> 4
<211> 19
<212> DNA
<213> 人工序列
<220>
<223> invA 反向
<400> 4
tcgcaccgtc aaaggaacc 19
- 使用即时检测装置进行病原体富集和核酸提取的方法
- 使用血培养阳性标本直接进行病原体鉴定及药敏检测的方法
